以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料生产铝和氮化铝的一种工艺流程如下【已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀】。
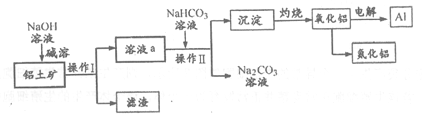
(1)操作I、Ⅱ的名称为____________ 。
(2)用氧化物的形式表示铝硅酸钠的化学式_____________ 。
(3)溶液a中加入NaHCO3后,生成沉淀的离子方程式为____________ 。
(4)Al2O3比另外一种铝的化合物AlCl3熔点高出很多,原因是_________ ; 有人考虑用熔融态AlCl3电解制备铝,你觉得是否可行,____ (选填“可行”或“不可行”),试分析原因_________ 。
(5)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。打开K2,加入NaOH浓溶液,至不再产生NH3。打开K1,通入N2一段时间。
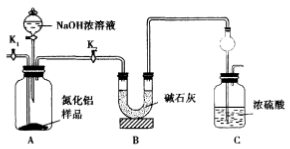
①实验中需要测定的数据是___________ 。
②由于装置存在缺陷,导致测定结果偏高,请提出改进方法:___________ 。

(1)操作I、Ⅱ的名称为
(2)用氧化物的形式表示铝硅酸钠的化学式
(3)溶液a中加入NaHCO3后,生成沉淀的离子方程式为
(4)Al2O3比另外一种铝的化合物AlCl3熔点高出很多,原因是
(5)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。打开K2,加入NaOH浓溶液,至不再产生NH3。打开K1,通入N2一段时间。

①实验中需要测定的数据是
②由于装置存在缺陷,导致测定结果偏高,请提出改进方法:
更新时间:2017-12-12 15:45:48
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】2019年诺贝尔化学奖颁给了日本吉野彰等三人,以表彰他们对锂离子电池研发的卓越贡献。
(1)自然界中主要的锂矿物为锂辉石、锂云母、透锂长石和磷锂铝石等。为鉴定某矿石中是否含有锂元素,可以采用焰色反应来进行鉴定,当观察到火焰呈________ ,可以认为存在锂元素。
A.紫红色 B.紫色 C.黄色
(2)工业中利用锂辉石(主要成分为LiAlSi2O6,还含有FeO、CaO、MgO等)制备钴酸锂(LiCoO2)的流程如下:
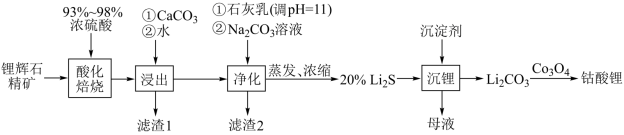
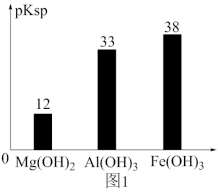
已知:部分金属氢氧化物的pKsp(pKsp=-lgKsp)的柱状图如图1。
回答下列问题:
①锂辉石的主要成分为LiAlSi2O6,其氧化物的形式为________ 。
②为提高“酸化焙烧”效率,常采取的措施是________ 。
③向“浸出液”中加入CaCO3,其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、A13+完全沉淀,则pH至少为_______ 。(已知:完全沉淀后离子浓度低于1×l0-5)mol/L)
④“沉锂”过程所获得的“母液”中仍含有大量的Li+,可将其加入到“___________ ”步骤中。
⑤Li2CO3与Co3O4在敞口容器中高温下焙烧生成钴酸锂的化学方程式为__________
(3)利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LiCoO2+C6 LixC6+Li1-xCoO2 ,其工作原理如图2。
LixC6+Li1-xCoO2 ,其工作原理如图2。

下列关于该电池的说法正确的是___________ (填字母)。
A.电池反应式中过程1为放电过程
B.该电池若用隔膜可选用质子交换膜
C.石墨烯电池的优点是提高电池的储锂容量进而提高能量密度
D.充电时,LiCoO2极发生的电极反应为LiCoO2-xe-=xLi++Li1-xCoO2
E.对废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收
(1)自然界中主要的锂矿物为锂辉石、锂云母、透锂长石和磷锂铝石等。为鉴定某矿石中是否含有锂元素,可以采用焰色反应来进行鉴定,当观察到火焰呈
A.紫红色 B.紫色 C.黄色
(2)工业中利用锂辉石(主要成分为LiAlSi2O6,还含有FeO、CaO、MgO等)制备钴酸锂(LiCoO2)的流程如下:

已知:部分金属氢氧化物的pKsp(pKsp=-lgKsp)的柱状图如图1。

回答下列问题:
①锂辉石的主要成分为LiAlSi2O6,其氧化物的形式为
②为提高“酸化焙烧”效率,常采取的措施是
③向“浸出液”中加入CaCO3,其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、A13+完全沉淀,则pH至少为
④“沉锂”过程所获得的“母液”中仍含有大量的Li+,可将其加入到“
⑤Li2CO3与Co3O4在敞口容器中高温下焙烧生成钴酸锂的化学方程式为
(3)利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LiCoO2+C6
 LixC6+Li1-xCoO2 ,其工作原理如图2。
LixC6+Li1-xCoO2 ,其工作原理如图2。
下列关于该电池的说法正确的是
A.电池反应式中过程1为放电过程
B.该电池若用隔膜可选用质子交换膜
C.石墨烯电池的优点是提高电池的储锂容量进而提高能量密度
D.充电时,LiCoO2极发生的电极反应为LiCoO2-xe-=xLi++Li1-xCoO2
E.对废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】本月4日,谷歌公司宣布:以60胜O负1平的战绩横扫众多围棋高手的神秘棋手“Master”乃是其人工智能产品AlpbaGo的升级版,人工智能再次成为热门话题。其中,高纯度硅是一种重要的基础材料。以下是工业上制取纯硅的一种方法:

请回答下列问题(各元素用相应的元素符号表示):
(1)在上述生产过程中,属于置换反应的有 1 (填反应代号)。
(2)写出反应①的化学方程式: 2 ;在反应①发生的同时,会发生副反应:SiO2+3C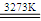 SiC+CO↑。若产品中单质硅与碳化硅的物质的最之比为l: l,则参加反应的C和SiO2的物质的量之比为
SiC+CO↑。若产品中单质硅与碳化硅的物质的最之比为l: l,则参加反应的C和SiO2的物质的量之比为 3 。
(3)写出反应③的化学方程式 4 。
(4)整个制备过程中必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质。写出该反应的化学方程式 5 。
(5)硅的化合物用途也很广泛,将石英砂和纯碱按一定比例混合加热至1373~1623K反应,生成化合物W,其化学方程式是 6 ;

请回答下列问题(各元素用相应的元素符号表示):
(1)在上述生产过程中,属于置换反应的有
(2)写出反应①的化学方程式:
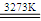 SiC+CO↑。若产品中单质硅与碳化硅的物质的最之比为l: l,则参加反应的C和SiO2的物质的量之比为
SiC+CO↑。若产品中单质硅与碳化硅的物质的最之比为l: l,则参加反应的C和SiO2的物质的量之比为(3)写出反应③的化学方程式
(4)整个制备过程中必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质。写出该反应的化学方程式
(5)硅的化合物用途也很广泛,将石英砂和纯碱按一定比例混合加热至1373~1623K反应,生成化合物W,其化学方程式是
| A. | B.C几种气体在“节能减排”中作为减排目标的一种气体是_____(填化学式);将该气体通入化合物W的水溶液中的现象为____。 (6)工业上:常将硅酸盐的化学式表示为氧化物的形式,如:Na2SiO3可表示为Na2O·SiO2 ,正长石的化学式为KAlSi3Ox,则x=____,将正长石的化学式改写为氧化物的形式________。 |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】钒、钛、铝组成的金属合金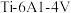 常用于飞机发动机、宇航船舱骨架、导弹、军舰的水翼等。钒精矿可表示为
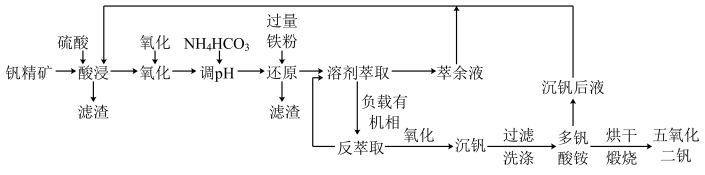
常用于飞机发动机、宇航船舱骨架、导弹、军舰的水翼等。钒精矿可表示为 ,还含有其他难溶硫酸盐杂质。“萃取”钒工艺流程路线图如下:
,还含有其他难溶硫酸盐杂质。“萃取”钒工艺流程路线图如下:
已知:①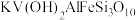 中
中 为
为 价。
价。
②“氧化”后的溶液中钒以 存在,反萃取后的溶液中钒以
存在,反萃取后的溶液中钒以 存在。
存在。
③ 为萃取剂。
为萃取剂。
回答下列问题:
(1)将钒精矿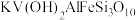 写成氧化物的形式
写成氧化物的形式____________________________ 。
(2)写出“氧化”过程中反应的离子方程式____________________________ 。
(3)加入 调节溶液
调节溶液 的目的是
的目的是____________________________ 。
(4)“还原”过程中主要反应的离子反应方程式为____________________________ 。
(5)为了提高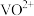 的产率,反萃取剂应该呈
的产率,反萃取剂应该呈_________ (填“酸性”“碱性”或“中性”)。
(6)若用氧化剂 “氧化沉钒”时,生成
“氧化沉钒”时,生成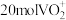 ,至少需要
,至少需要
_________ 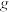 。
。
(7)写出煅烧多钒酸铵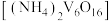 的化学反应方程式
的化学反应方程式__________________ 。
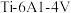 常用于飞机发动机、宇航船舱骨架、导弹、军舰的水翼等。钒精矿可表示为
常用于飞机发动机、宇航船舱骨架、导弹、军舰的水翼等。钒精矿可表示为 ,还含有其他难溶硫酸盐杂质。“萃取”钒工艺流程路线图如下:
,还含有其他难溶硫酸盐杂质。“萃取”钒工艺流程路线图如下:
已知:①
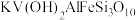 中
中 为
为 价。
价。②“氧化”后的溶液中钒以
 存在,反萃取后的溶液中钒以
存在,反萃取后的溶液中钒以 存在。
存在。③
 为萃取剂。
为萃取剂。回答下列问题:
(1)将钒精矿
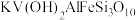 写成氧化物的形式
写成氧化物的形式(2)写出“氧化”过程中反应的离子方程式
(3)加入
 调节溶液
调节溶液 的目的是
的目的是(4)“还原”过程中主要反应的离子反应方程式为
(5)为了提高
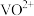 的产率,反萃取剂应该呈
的产率,反萃取剂应该呈(6)若用氧化剂
 “氧化沉钒”时,生成
“氧化沉钒”时,生成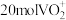 ,至少需要
,至少需要
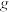 。
。(7)写出煅烧多钒酸铵
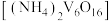 的化学反应方程式
的化学反应方程式
您最近一年使用:0次
【推荐1】一种利用硫铁矿(主要成分是FeS2,含少量Al2O3、SiO2和Fe3O4)制备新能源汽车电池电极LiFePO4的工艺流程如下:
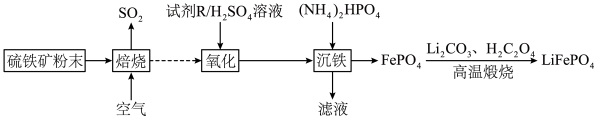
①已知室温下难溶物溶度积常数如下表,离子浓度小于10-5mol/L,认为沉淀完全。
②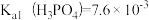 ,
,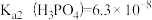 ,
,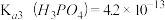
回答下列问题:
(1)从“焙烧”到“氧化”要经历“酸浸→还原→过滤一除铝”4道工序。
①若“酸浸”工序用硫酸,“还原”工序加入FeS。“还原”工序的离子方程式为_________________ ,滤渣的成分是_________________ (填化学式)。
②“除铝”工序可加入的难溶物质是________________ (填化学式),除净铝离子需要调节的最小pH为_________________ (结果保留一位小数)。
(2)“氧化”步骤中,加入的试剂“R”最佳是_________________ (填标号),
A.HNO3 B.H2O2 C.Ca(ClO)2 D.KMnO4
判断是否氧化彻底的试剂名称为_________________ 。
(3)“沉铁”步骤反应的平衡常数为_________________ 。
(4)“高温煅烧”时,发生的主要反应的化学方程式为_________________ 。

①已知室温下难溶物溶度积常数如下表,离子浓度小于10-5mol/L,认为沉淀完全。
| 难溶物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | FePO4 |
| Ksp | 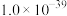 | 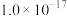 | 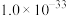 | 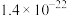 |
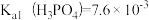 ,
,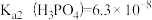 ,
,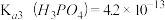
回答下列问题:
(1)从“焙烧”到“氧化”要经历“酸浸→还原→过滤一除铝”4道工序。
①若“酸浸”工序用硫酸,“还原”工序加入FeS。“还原”工序的离子方程式为
②“除铝”工序可加入的难溶物质是
(2)“氧化”步骤中,加入的试剂“R”最佳是
A.HNO3 B.H2O2 C.Ca(ClO)2 D.KMnO4
判断是否氧化彻底的试剂名称为
(3)“沉铁”步骤反应的平衡常数为
(4)“高温煅烧”时,发生的主要反应的化学方程式为
您最近一年使用:0次
【推荐2】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与金属铜发生反应的化学方程式:______________________ 。
(2)某工程师为了从使用过的腐蚀废液(主要含CuCl2、FeCl3溶液等)中回收铜,并重新获得纯净的FeCl3溶液,准备采用如图所示流程:(已知:加过量①为Fe;加过量④为稀盐酸;通入⑥为Cl2)
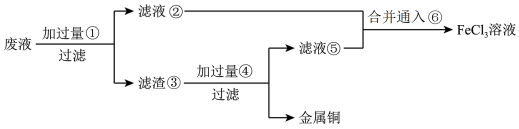
①上述实验中滤渣③的主要物质为___________________ (填化学式),写出向②⑤的合并液中通入⑥的离子方程式:______________________________ 。
②配制并保存FeCl2溶液时,需加入铁屑,其目的是_______________________________ 。
③要证明FeCl3溶液是否含有Fe2+,可选择下列选项中的______________ (已知:加入该物质后,生成蓝色沉淀)。
A.加入 K3[Fe(CN)6]溶液 B.加入NaOH溶液 C.加入KSCN溶液
(3)现有1.2 L含3 mol FeCl2的酸性溶液恰好与0.6 mol HIO3完全反应,还原产物为_______ (填化学式,已知该物质遇淀粉溶液变蓝),该反应离子方程式为___________________________________ 。
(1)写出FeCl3溶液与金属铜发生反应的化学方程式:
(2)某工程师为了从使用过的腐蚀废液(主要含CuCl2、FeCl3溶液等)中回收铜,并重新获得纯净的FeCl3溶液,准备采用如图所示流程:(已知:加过量①为Fe;加过量④为稀盐酸;通入⑥为Cl2)

①上述实验中滤渣③的主要物质为
②配制并保存FeCl2溶液时,需加入铁屑,其目的是
③要证明FeCl3溶液是否含有Fe2+,可选择下列选项中的
A.加入 K3[Fe(CN)6]溶液 B.加入NaOH溶液 C.加入KSCN溶液
(3)现有1.2 L含3 mol FeCl2的酸性溶液恰好与0.6 mol HIO3完全反应,还原产物为
您最近一年使用:0次
【推荐3】硫酸亚铁作为补血剂,可促进动物的生长发育,增强抗病能力。以钛白副产绿矾(成分为 、
、 、FeO、PbO、CuO)为原料制备绿矾(
、FeO、PbO、CuO)为原料制备绿矾( )并测定其纯度。
)并测定其纯度。
Ⅰ.制备绿矾的工艺流程如下:

(1)写出两条可提高“酸浸”效率的措施:_______ 。
(2)检验“酸浸”后的溶液中是否含 的试剂是
的试剂是_______ 。
(3)“还原”时溶液中含铁物质发生反应的化学方程式为_______ 。
(4)“一系列操作”包括蒸发浓缩、_______ 、过滤、洗涤、干燥。干燥时温度不宜过高,其原因是_______ 。
Ⅱ. 纯度的测定:
纯度的测定:
实验步骤:
①称取5.0g绿矾,溶解于水中,配成250mL溶液;
②量取25.00mL待测液于锥形瓶中;
③用0.01mol/L的酸性标准液滴定至终点,再重复滴定两次,消耗酸性标准液的平均体积为35.00mL。
(5)酸性 标准液盛放在
标准液盛放在_______ (填“A”或“B”)中。
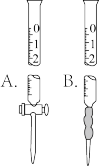
(6)滴定时反应的离子方程式为_______ 。
(7) 的纯度为
的纯度为_______ 。
 、
、 、FeO、PbO、CuO)为原料制备绿矾(
、FeO、PbO、CuO)为原料制备绿矾( )并测定其纯度。
)并测定其纯度。Ⅰ.制备绿矾的工艺流程如下:

(1)写出两条可提高“酸浸”效率的措施:
(2)检验“酸浸”后的溶液中是否含
 的试剂是
的试剂是(3)“还原”时溶液中含铁物质发生反应的化学方程式为
(4)“一系列操作”包括蒸发浓缩、
Ⅱ.
 纯度的测定:
纯度的测定:实验步骤:
①称取5.0g绿矾,溶解于水中,配成250mL溶液;
②量取25.00mL待测液于锥形瓶中;
③用0.01mol/L的酸性标准液滴定至终点,再重复滴定两次,消耗酸性标准液的平均体积为35.00mL。
(5)酸性
 标准液盛放在
标准液盛放在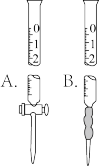
(6)滴定时反应的离子方程式为
(7)
 的纯度为
的纯度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】Ⅰ.工业上用铝土矿(主要成分为Al2O3、Fe2O3、SiO2)提取氧化铝做冶炼铝的原料,提取的操作流程如下:
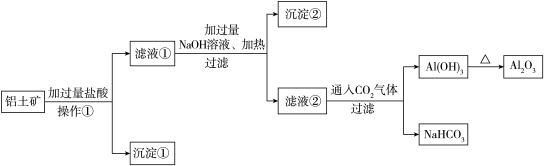
请回答下列问题:
(1)操作①的名称:____________ ;
(2) 沉淀②的化学式:____________ ;
(3)写出沉淀①与NaOH溶液反应的化学方程式:__________ ;
(4)写出滤液②里通入过量CO2后生成沉淀的离子方程式:______ ,能否将滤液②中通入过量CO2换成加入过量盐酸? ____ (填 能 或 不能),其理由是_______ (用化学方程式表示)。
Ⅱ.无水AlCl3易升华,可用作有机合成的催化剂等。工业上以铝土矿为原料制备无水AlCl3的工艺流程如下:
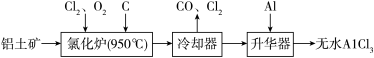
(1)铝在空气中有较强的抗腐蚀性,原因是___________________________ 。
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式为___________________________ 。
(3)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16g无水AlCl3样品溶于过量的NaOH溶液中,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,得其质量为0.32g。
①写出上述除杂过程中涉及的离子方程式______________ 、_______________ 。
②产品中AlCl3的质量分数为___________ 。(保留两位有效数字)

请回答下列问题:
(1)操作①的名称:
(2) 沉淀②的化学式:
(3)写出沉淀①与NaOH溶液反应的化学方程式:
(4)写出滤液②里通入过量CO2后生成沉淀的离子方程式:
Ⅱ.无水AlCl3易升华,可用作有机合成的催化剂等。工业上以铝土矿为原料制备无水AlCl3的工艺流程如下:

(1)铝在空气中有较强的抗腐蚀性,原因是
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式为
(3)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16g无水AlCl3样品溶于过量的NaOH溶液中,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,得其质量为0.32g。
①写出上述除杂过程中涉及的离子方程式
②产品中AlCl3的质量分数为
您最近一年使用:0次
【推荐2】工业上用铝土矿(主要成分为氧化铝,含少量氧化铁)制取铝的过程如图所示:
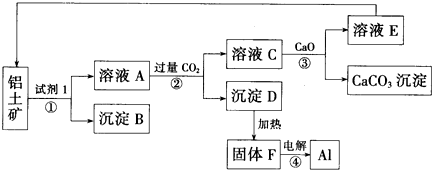
请回答:
(1)试剂1为_______ (填化学式),①~④转化中属于氧化还原反应的是_______ (填序号);
(2)沉淀B的化学式为_______ ,写出该物质发生铝热反应的化学方程式_______ ;(3)电解F,当转移0.6mol电子时,可制得铝 _______ g;
(4)沉淀D是药物“胃舒平”的主要成分,可用于治疗胃酸(稀盐酸)过多,写出该反应的离子方程式_______ ;
(5)②中发生反应的离子方程式为_______ 。

请回答:
(1)试剂1为
(2)沉淀B的化学式为
(4)沉淀D是药物“胃舒平”的主要成分,可用于治疗胃酸(稀盐酸)过多,写出该反应的离子方程式
(5)②中发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】以铝土矿(主要成分为Al2O3和杂质)为原料制备铝的一种工艺流程如下:

注:反应Ⅰ“碱溶”时杂质转化为沉淀
(1)反应Ⅰ,发生反应生成偏铝酸钠的离子方程式__________ 。
(2)电解Ⅰ是电解熔融的冰晶石和Al2O3的混合物,电解过程中作阳极的石墨易消耗,原因是___________ 。
(3)反应Ⅱ,用一定浓度的NaHCO3溶液处理过滤Ⅰ后的滤液,所得溶液pH和生成Al(OH)3的量随加入NaHCO3溶液体积变化的曲线如下:
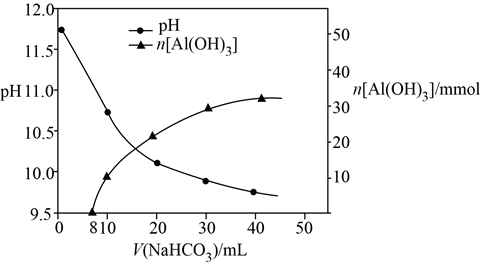
①加入NaHCO3溶液体积小于8 mL时,发生主要反应的离子方程式__________ 。
②反应Ⅱ中生成Al(OH)3的离子方程式__________ 。
(4)电解Ⅱ是电解Na2CO3溶液,得到含NaHCO3的阳极液,原理如下图所示。

阴极产生的物质A的化学式为____________ 。
(5)以铝材为阳极,在H2SO4溶液中电解,可在铝材表面形成致密氧化膜,阳极电极反应式为_______________ 。

注:反应Ⅰ“碱溶”时杂质转化为沉淀
(1)反应Ⅰ,发生反应生成偏铝酸钠的离子方程式
(2)电解Ⅰ是电解熔融的冰晶石和Al2O3的混合物,电解过程中作阳极的石墨易消耗,原因是
(3)反应Ⅱ,用一定浓度的NaHCO3溶液处理过滤Ⅰ后的滤液,所得溶液pH和生成Al(OH)3的量随加入NaHCO3溶液体积变化的曲线如下:
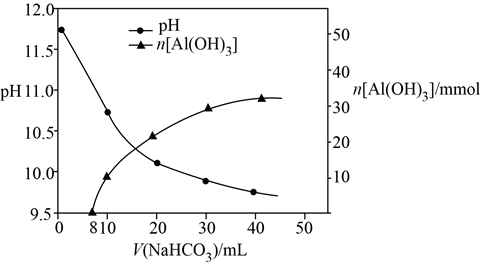
①加入NaHCO3溶液体积小于8 mL时,发生主要反应的离子方程式
②反应Ⅱ中生成Al(OH)3的离子方程式
(4)电解Ⅱ是电解Na2CO3溶液,得到含NaHCO3的阳极液,原理如下图所示。

阴极产生的物质A的化学式为
(5)以铝材为阳极,在H2SO4溶液中电解,可在铝材表面形成致密氧化膜,阳极电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】叠氮化钠(NaN3)是白色固体;易溶于水,微溶于乙醇,不溶于乙醚;常用在汽车行业和有机合成中。已知:① 有强氧化性,不与酸碱反应:
有强氧化性,不与酸碱反应:
②氨基钠(NaNH2)熔点210℃,易氧化、潮解,能与强酸反应生成叠氮酸,叠氮酸不稳定,易爆炸。
Ⅰ.制备

制备 过程涉及以下两个反应:
过程涉及以下两个反应:

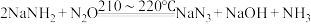 。
。
(1)仪器a的名称是___________ ,装置B中的试剂为___________ 。
(2)A中反应一段时间后再加热C的目的是___________ 。
(3)充分反应后,对C中所得固体混合物进行以下操作,得到 固体:
固体:
C中固体混合物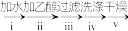 NaN3固体
NaN3固体
操作ⅱ的目的是___________ ,操作ⅳ选用的最佳试剂为___________ 。
Ⅱ.纯度测定
(4)称取4.0g叠氮化钠试样配成溶液,向其中加入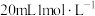 六硝酸铈铵[
六硝酸铈铵[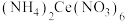 ]溶液恰好完全反应,反应方程式为
]溶液恰好完全反应,反应方程式为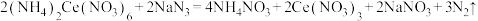 ,假设杂质均不参与反应,计算叠氮化钠的质量分数为
,假设杂质均不参与反应,计算叠氮化钠的质量分数为___________ 。
Ⅲ.废弃物处理
(5)①用装置E将尾气 转化为
转化为 ,反应过程中产生的沉淀经过滤、洗涤可获得
,反应过程中产生的沉淀经过滤、洗涤可获得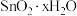 ,请简述检验沉淀是否洗涤干净的方法
,请简述检验沉淀是否洗涤干净的方法___________ 。
②多余的 常使用次氯酸钠溶液处理,在酸性条件下,二者反应可生成无毒的气体。请写出该反应的离子方程式
常使用次氯酸钠溶液处理,在酸性条件下,二者反应可生成无毒的气体。请写出该反应的离子方程式___________ 。
 有强氧化性,不与酸碱反应:
有强氧化性,不与酸碱反应:②氨基钠(NaNH2)熔点210℃,易氧化、潮解,能与强酸反应生成叠氮酸,叠氮酸不稳定,易爆炸。
Ⅰ.制备


制备
 过程涉及以下两个反应:
过程涉及以下两个反应:
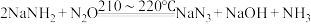 。
。(1)仪器a的名称是
(2)A中反应一段时间后再加热C的目的是
(3)充分反应后,对C中所得固体混合物进行以下操作,得到
 固体:
固体:C中固体混合物
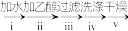 NaN3固体
NaN3固体操作ⅱ的目的是
Ⅱ.纯度测定
(4)称取4.0g叠氮化钠试样配成溶液,向其中加入
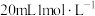 六硝酸铈铵[
六硝酸铈铵[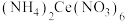 ]溶液恰好完全反应,反应方程式为
]溶液恰好完全反应,反应方程式为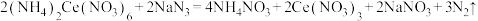 ,假设杂质均不参与反应,计算叠氮化钠的质量分数为
,假设杂质均不参与反应,计算叠氮化钠的质量分数为Ⅲ.废弃物处理
(5)①用装置E将尾气
 转化为
转化为 ,反应过程中产生的沉淀经过滤、洗涤可获得
,反应过程中产生的沉淀经过滤、洗涤可获得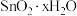 ,请简述检验沉淀是否洗涤干净的方法
,请简述检验沉淀是否洗涤干净的方法②多余的
 常使用次氯酸钠溶液处理,在酸性条件下,二者反应可生成无毒的气体。请写出该反应的离子方程式
常使用次氯酸钠溶液处理,在酸性条件下,二者反应可生成无毒的气体。请写出该反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】过氧化钙(CaO2)是一种白色晶体,无臭无味,能潮解,难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。通常利用CaCl2在碱性条件下与H2O2反应制得。某化学兴趣小组在实验室制备CaO2的实验方案和装置示意图 如下:
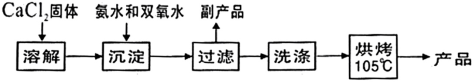
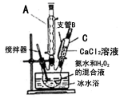
已知:CaO2的制备原理:CaCl2+H2O2+2NH3•H2O+6H2O= CaO2•8H2O↓+2NH4Cl
请回答下列问题:
(1)仪器A的名称为__________ ,仪器C支管B的作用____________ ;
(2)加入氨水的作用是_______ ;(从化学平衡移动的原理分析)
(3)过滤后洗涤沉淀的试剂最好用_______ ;
A.水 B.浓盐酸 C.无水乙醇 D.CaCl2溶液
(4)沉淀反应时常用冰水浴控制温度在O℃左右,其可能原因是_________ 、_______ (写出两种)。
(5)已知CaO2在350℃时能迅速分解,生成CaO和O2。该小组采用如图所示的装置测定刚才制备的产品中CaO2的纯度(设杂质不分解产生气体)
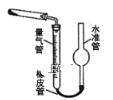
①检查该装置气密性的方法是:________________ ;
②准确称取0.50g样品,置于试管中加热使其完全分解,收集到44.80mL(已换算为标准状况)气体,则产品中过氧化钙的质量分数为________ (保留4位有效数字);


已知:CaO2的制备原理:CaCl2+H2O2+2NH3•H2O+6H2O= CaO2•8H2O↓+2NH4Cl
请回答下列问题:
(1)仪器A的名称为
(2)加入氨水的作用是
(3)过滤后洗涤沉淀的试剂最好用
A.水 B.浓盐酸 C.无水乙醇 D.CaCl2溶液
(4)沉淀反应时常用冰水浴控制温度在O℃左右,其可能原因是
(5)已知CaO2在350℃时能迅速分解,生成CaO和O2。该小组采用如图所示的装置测定刚才制备的产品中CaO2的纯度(设杂质不分解产生气体)

①检查该装置气密性的方法是:
②准确称取0.50g样品,置于试管中加热使其完全分解,收集到44.80mL(已换算为标准状况)气体,则产品中过氧化钙的质量分数为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业。实验室制备亚硝酰硫酸的方法如下:将SO2通入盛有浓硫酸和浓硝酸的混合液中,维持体系温度略低于20℃,搅拌,使其充分反应。反应过程中,亚硝酰硫酸的物质的量和硝酸的物质的量随时间的变化如图所示。
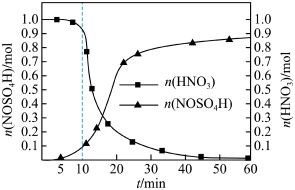
(1)①实验室制备NOSO4H的化学反应方程式为___ 。
②反应进行到10min后,反应速度明显加快,其可能的原因是___ 。
③反应过程中,硝酸减少的物质的量大于NOSO4H生成的物质的量的可能原因是___
(2)为了测定亚硝酰硫酸的纯度,进行如下实验:。
准确称取1.200g产品放入锥形瓶中,加入50.00mL0.1000mol·L-1的KMnO4标准溶液和足量稀H2SO4,摇匀,使其充分反应。再将反应后溶液加热至60~70℃(使生成的HNO3挥发逸出),冷却至室温,用0.2500mol·L-1Na2C2O4标准溶液滴定至终点,消耗Na2C2O4溶液的体积为16.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4;KMnO4在酸性条件下被还原为Mn2+。
根据以上实验数据计算亚硝酰硫酸的纯度。(写出计算过程)___

(1)①实验室制备NOSO4H的化学反应方程式为
②反应进行到10min后,反应速度明显加快,其可能的原因是
③反应过程中,硝酸减少的物质的量大于NOSO4H生成的物质的量的可能原因是
(2)为了测定亚硝酰硫酸的纯度,进行如下实验:。
准确称取1.200g产品放入锥形瓶中,加入50.00mL0.1000mol·L-1的KMnO4标准溶液和足量稀H2SO4,摇匀,使其充分反应。再将反应后溶液加热至60~70℃(使生成的HNO3挥发逸出),冷却至室温,用0.2500mol·L-1Na2C2O4标准溶液滴定至终点,消耗Na2C2O4溶液的体积为16.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4;KMnO4在酸性条件下被还原为Mn2+。
根据以上实验数据计算亚硝酰硫酸的纯度。(写出计算过程)
您最近一年使用:0次



