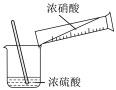
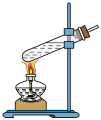
1 . 丁香酚氧基乙酸不仅有抗病毒、抗菌性能,而且还有抑制脂质增加的功能。纯净的丁香酚氧基乙酸( )为白色固体,可用丁香酚(
)为白色固体,可用丁香酚( ,沸点:254℃)为主要原料制得,其合成原理如图所示。
,沸点:254℃)为主要原料制得,其合成原理如图所示。
I.将 溶于
溶于 中,添加
中,添加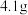 丁香酚,在80℃~90℃中搅拌,得到溶液甲。
丁香酚,在80℃~90℃中搅拌,得到溶液甲。
Ⅱ.小心将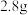 氯乙酸溶解在
氯乙酸溶解在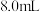 水中,缓慢添加
水中,缓慢添加 溶液使其呈碱性,得到溶液乙。
溶液使其呈碱性,得到溶液乙。
Ⅲ.将溶液乙缓慢滴加到溶液甲中,在90℃~95℃搅拌混合物1小时。反应完毕后,冷却至室温,加入盐酸至溶液呈酸性,得到溶液丙。
Ⅳ.向溶液丙中加入碎冰,搅拌至黄色油状物变成淡黄色固体,过滤、洗涤。
Ⅴ.向固体中加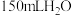 ,加热至沸腾,随后将溶液用冰水冷却。经过滤、洗涤、干燥称量,得到
,加热至沸腾,随后将溶液用冰水冷却。经过滤、洗涤、干燥称量,得到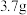 固体。
固体。
回答下列问题:
(1)步骤I中最适宜的加热方式为___________ 。
(2)若第Ⅱ步用NaOH代替 ,则产生的后果是
,则产生的后果是___________ 。(用化学方程式表示)
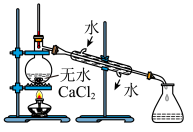
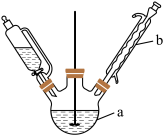
(3)某兴趣小组设计了第Ⅲ步反应装置(如图所示,加热装置略去),仪器a的名称是___________ ;有同学认为仪器b是多余的,他给出的理由是___________ 。___________ 。
(5)第Ⅴ步分离提纯方法的名称是___________ ;在分离过程中可加入一些活性炭脱色,但加入活性炭过多,会造成产率下降,可能原因为___________ 。
(6)本实验的产率为___________ 。(用丁香酚算,精确至 )
)
 )为白色固体,可用丁香酚(
)为白色固体,可用丁香酚( ,沸点:254℃)为主要原料制得,其合成原理如图所示。
,沸点:254℃)为主要原料制得,其合成原理如图所示。
I.将
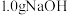 溶于
溶于 中,添加
中,添加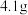 丁香酚,在80℃~90℃中搅拌,得到溶液甲。
丁香酚,在80℃~90℃中搅拌,得到溶液甲。Ⅱ.小心将
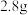 氯乙酸溶解在
氯乙酸溶解在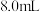 水中,缓慢添加
水中,缓慢添加 溶液使其呈碱性,得到溶液乙。
溶液使其呈碱性,得到溶液乙。Ⅲ.将溶液乙缓慢滴加到溶液甲中,在90℃~95℃搅拌混合物1小时。反应完毕后,冷却至室温,加入盐酸至溶液呈酸性,得到溶液丙。
Ⅳ.向溶液丙中加入碎冰,搅拌至黄色油状物变成淡黄色固体,过滤、洗涤。
Ⅴ.向固体中加
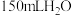 ,加热至沸腾,随后将溶液用冰水冷却。经过滤、洗涤、干燥称量,得到
,加热至沸腾,随后将溶液用冰水冷却。经过滤、洗涤、干燥称量,得到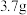 固体。
固体。回答下列问题:
(1)步骤I中最适宜的加热方式为
(2)若第Ⅱ步用NaOH代替
 ,则产生的后果是
,则产生的后果是(3)某兴趣小组设计了第Ⅲ步反应装置(如图所示,加热装置略去),仪器a的名称是
(5)第Ⅴ步分离提纯方法的名称是
(6)本实验的产率为
 )
)
您最近半年使用:0次
2 . 实验室制备硝基苯(密度 ,不溶于水)时,经过配制混酸、硝化反应(
,不溶于水)时,经过配制混酸、硝化反应( )、洗涤分离、干燥蒸馏等步骤。下列图示装置和原理能达到目的的是
)、洗涤分离、干燥蒸馏等步骤。下列图示装置和原理能达到目的的是
 ,不溶于水)时,经过配制混酸、硝化反应(
,不溶于水)时,经过配制混酸、硝化反应( )、洗涤分离、干燥蒸馏等步骤。下列图示装置和原理能达到目的的是
)、洗涤分离、干燥蒸馏等步骤。下列图示装置和原理能达到目的的是
|
|
| A.配制混酸 | B.硝化反应 |
|
|
| C.分离硝基苯 | D.蒸馏硝基苯 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
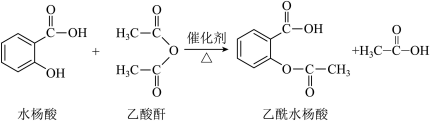
3 . 乙酰水杨酸(阿司匹林)是应用广泛的解热、镇痛和抗炎药,它对肠胃的刺激较小,在体内还具有抗血栓的作用,可用于预防心脑血管疾病,与青霉素、安定并称为“医药史上三大经典药物”。其合成原理如下:
(一)制备过程
①向100mL的三颈烧瓶中依次加入6.9g干燥的水杨酸、8.0mL新蒸的乙酸酐和0.5mL浓硫酸(作催化剂),磁力搅拌下,小心加热,控制温度在70℃左右反应30min。
②稍冷后,将反应液缓慢倒入100mL冰水中冷却15min,用图2装置减压抽滤,将所有产品收集到布氏漏斗中,滤饼用少量冷水多次洗涤,继续抽滤,得到乙酰水杨酸粗品。
(二)提纯过程
③将粗产品转移至100mL圆底烧瓶中,再加入20mL乙酸乙酯,加热溶解,如有不溶物出现,趁热过滤,热滤液置冰箱中冷却至-5℃~0℃,抽滤,洗涤,干燥,得无色晶体乙酰水杨酸,称重得4.50g。
回答下列问题:
(1)图2中“抽滤”操作相对于普通过滤的优点是_______ 。
(2)步骤①中加热操作宜采用_______ ,图1中仪器A的名称为_______ ,A的作用是防止外界的水蒸气进入三颈烧瓶导致发生副反应,降低水杨酸的转化率。写出该副反应的化学方程式_______ 。
(3)步骤②用冷水洗涤后,如何检验阿司匹林中是否还有杂质水杨酸剩余?_______ 。
(4)步骤③的提纯方法是_______ (写操作名称)。
(5)计算乙酰水杨酸(阿司匹林)的产率为_______ 。
| 物质 | 相对分子质量 | 密度/g/cm3 | 熔点/℃ | 其他性质 |
| 水杨酸 | 138 | 1.44 | 157~159 | 溶于乙醇、微溶于水 |
| 乙酸酐 | 102 | 1.08 | -72~-74 | 沸点140℃,无色透明液体,遇水形成乙酸 |
| 阿司匹林 | 180 | 1.35 | 135~138 | 分解温度为128~135℃,溶于乙醇、微溶于水 |
| 乙酸乙酯 | 88 | 0.90 | -87 | 沸点77℃,微溶于水,溶于乙醇等有机溶剂 |

(一)制备过程
①向100mL的三颈烧瓶中依次加入6.9g干燥的水杨酸、8.0mL新蒸的乙酸酐和0.5mL浓硫酸(作催化剂),磁力搅拌下,小心加热,控制温度在70℃左右反应30min。
②稍冷后,将反应液缓慢倒入100mL冰水中冷却15min,用图2装置减压抽滤,将所有产品收集到布氏漏斗中,滤饼用少量冷水多次洗涤,继续抽滤,得到乙酰水杨酸粗品。
(二)提纯过程
③将粗产品转移至100mL圆底烧瓶中,再加入20mL乙酸乙酯,加热溶解,如有不溶物出现,趁热过滤,热滤液置冰箱中冷却至-5℃~0℃,抽滤,洗涤,干燥,得无色晶体乙酰水杨酸,称重得4.50g。
回答下列问题:
(1)图2中“抽滤”操作相对于普通过滤的优点是
(2)步骤①中加热操作宜采用
(3)步骤②用冷水洗涤后,如何检验阿司匹林中是否还有杂质水杨酸剩余?
(4)步骤③的提纯方法是
(5)计算乙酰水杨酸(阿司匹林)的产率为
您最近半年使用:0次
4 . 间苯三酚可用于合成重要的有机合成中间体3,5-二甲氧基苯酚,反应如图:
下列说法不正确的是

| 物质 | 沸点/ | 熔点/ | 溶解性 |
| 甲醇 | 64.7 | 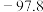 | 易溶于水 |
| 3,5-二甲氧基苯酚 | 172~175 | 33~36 | 易溶于甲醇、乙醚,微溶于水 |
| A.该反应属于取代反应 |
| B.分离出甲醇的操作是蒸馏 |
C.洗涤时,可用饱和 溶液除去有机层中的氯化氢 溶液除去有机层中的氯化氢 |
D.间苯三酚与3,5-二甲氧基苯酚均可与 溶液发生显色反应 溶液发生显色反应 |
您最近半年使用:0次
解题方法
5 . 富马酸亚铁(结构简式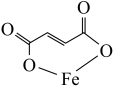 ,刚对分子质量170)是治疗贫血药物的一种。实验制备富马酸亚铁并测其产品中富马酸亚铁的质量分数。
,刚对分子质量170)是治疗贫血药物的一种。实验制备富马酸亚铁并测其产品中富马酸亚铁的质量分数。
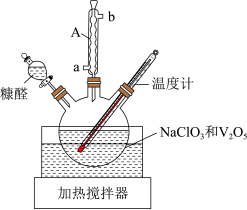
Ⅰ.富马酸( )的制备。制取装置如图所示(夹持仪器已略去),按如图装置打开分液漏斗活塞,滴加糠醛(
)的制备。制取装置如图所示(夹持仪器已略去),按如图装置打开分液漏斗活塞,滴加糠醛(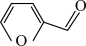 ),在90~100℃条件下层续加热2~3h。
),在90~100℃条件下层续加热2~3h。
Ⅱ.富马酸亚铁的制备
步骤1:将4.64 g富马酸置于100 mL烧杯中,加水20 mL,在热沸搅拌下加入
 溶液10 mL,使其pH为6.5~6.7;
溶液10 mL,使其pH为6.5~6.7;步骤2:将上述溶液转移至如图所示的装置中,缓慢加入40 mL 2 mol⋅L

 溶液,维持温度100℃,充分搅拌1.5 h;
溶液,维持温度100℃,充分搅拌1.5 h;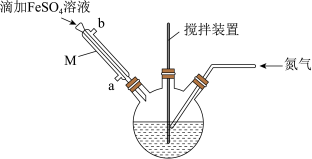
(2)在回流过程中一直通入氮气的目的是
(3)步骤1控制溶液pH为6.5~6.7;若反应后溶液的pH太小;则引起的后果是
Ⅲ.产品纯度测定
步骤①:准确称取粗产品0.1600 g,加煮沸过的3 mol⋅L

 溶液15 mL,待样品完全溶解后,加煮沸过的冷水50 mL和4滴邻二氮菲-亚铁指示剂,立即用0.0500 mol⋅L
溶液15 mL,待样品完全溶解后,加煮沸过的冷水50 mL和4滴邻二氮菲-亚铁指示剂,立即用0.0500 mol⋅L
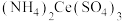 (硫酸高铈铵)标准溶液进行滴定。用去标准液的体积为16.82 mL(反应式为
(硫酸高铈铵)标准溶液进行滴定。用去标准液的体积为16.82 mL(反应式为 ),
),步骤②:不加产品,重复步骤①操作,滴定终点用去标准液0.02 mL。
(4)
(5)产品中富马酸亚铁的质量分数为
您最近半年使用:0次
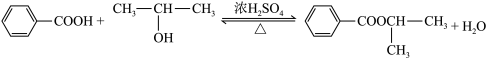
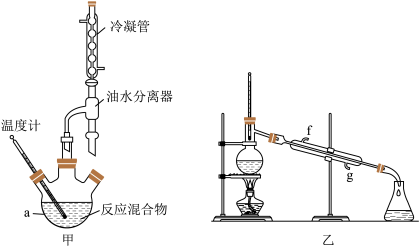
6 . 某化学兴趣小组设计图甲装置制备苯甲酸异丙酯,其反应原理如下:
实验步骤:
步骤i.在图甲干燥的仪器a中加入24.4g苯甲酸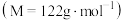 、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;
、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;
步骤ii.加热至70℃左右保持恒温半小时;
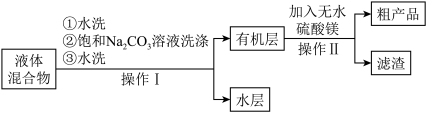
步骤iii.将图甲的仪器a中的液体混合物进行如下操作得到粗产品:
回答下列问题:
(1)图甲中仪器a的名称为___________ ,步骤i中选择的仪器a的容积大小为___________ (填标号)。
A. B.
B. C.
C. D.
D.
(2)实验中,加入的异丙醇需过量,其目的是___________ 。判断酯化反应接近反应限度的现象为___________ 。
(3)本实验一般可采用的加热方式为___________ 。
(4)操作Ⅰ中饱和碳酸钠溶液洗涤的目的是___________ ,操作Ⅱ中加入无水硫酸镁的作用为___________ 。
(5)步骤iv操作时应收集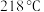 的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为
的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为___________ (填物质名称)。
(6)如果得到的苯甲酸异丙酯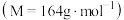 的质量为
的质量为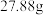 ,那么该实验的产率为
,那么该实验的产率为___________ %(保留3位有效数字)。
| 物质 | 相对分子质量 | 密度/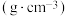 | 沸点/℃ | 水溶性 |
| 苯甲酸 | 122 | 1.27 | 249 | 微溶 |
| 异丙醇 | 60 | 0.79 | 82 | 易溶 |
| 苯甲酸异丙酯 | 164 | 1.08 | 218 | 不溶 |
步骤i.在图甲干燥的仪器a中加入24.4g苯甲酸
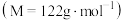 、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;
、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;步骤ii.加热至70℃左右保持恒温半小时;
步骤iii.将图甲的仪器a中的液体混合物进行如下操作得到粗产品:
回答下列问题:
(1)图甲中仪器a的名称为
A.
 B.
B. C.
C. D.
D.
(2)实验中,加入的异丙醇需过量,其目的是
(3)本实验一般可采用的加热方式为
(4)操作Ⅰ中饱和碳酸钠溶液洗涤的目的是
(5)步骤iv操作时应收集
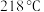 的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为
的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为(6)如果得到的苯甲酸异丙酯
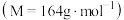 的质量为
的质量为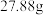 ,那么该实验的产率为
,那么该实验的产率为
您最近半年使用:0次
解题方法
7 . 过氧乙酸( )是无色透明液体,常用于速效漂白和消毒,氧化性比
)是无色透明液体,常用于速效漂白和消毒,氧化性比 强,与酸性
强,与酸性 相近。某课外实验小组同学用
相近。某课外实验小组同学用 溶液与乙酸酐制备高浓度过氧乙酸并对其含量测定,实验过程如下。
溶液与乙酸酐制备高浓度过氧乙酸并对其含量测定,实验过程如下。
 。
。Ⅰ.过氧化氢的浓缩:
 溶液浓缩至75%(
溶液浓缩至75%( 沸点150.2℃):浓缩装置如下图所示(连接用橡胶管和支持仪器以及抽气泵已省略):
沸点150.2℃):浓缩装置如下图所示(连接用橡胶管和支持仪器以及抽气泵已省略):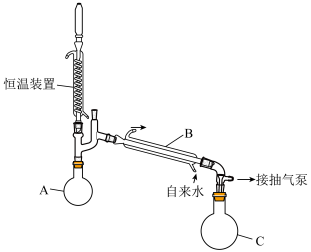
 溶液主要在
溶液主要在(2)该实验过程操作的正确顺序是
_______→_______→_______→_______→③→④
①水浴加热;②连接装置;③抽真空后向冷凝管中通水;
④自滴液漏斗往烧瓶中缓慢滴加
 溶液;
溶液;⑤在滴液漏斗中装入
 溶液;
溶液;⑥检查装置气密性。
Ⅱ.过氧乙酸的制备:如下图所示,搅拌器不断搅拌下,向三颈烧瓶中加入45mL乙酸酐,逐步滴加
 溶液25mL(过量),再加1mL浓硫酸,搅拌4小时,室温静置15小时即得47%的过氧乙酸溶液。
溶液25mL(过量),再加1mL浓硫酸,搅拌4小时,室温静置15小时即得47%的过氧乙酸溶液。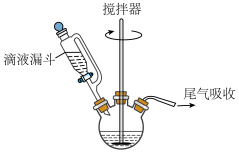
(4)实验中,利用搅拌器充分搅拌的作用是
(5)乙酸酐与
 反应的尾气可以用
反应的尾气可以用Ⅲ.过氧乙酸(含杂质)的含量测定:取适量样品按下图所示步骤依次进行实验,测定过氧乙酸的含量。

 溶液恰好除尽
溶液恰好除尽 的实验现象是
的实验现象是②第3步中过氧乙酸可被
 还原为乙酸,其离子方程式为
还原为乙酸,其离子方程式为③若实验中所取样品体积为
 ,第3步中加入
,第3步中加入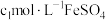 溶液
溶液 ,第4步滴定中消耗
,第4步滴定中消耗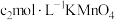 溶液
溶液 ,则过氧乙酸含量为
,则过氧乙酸含量为 。
。
您最近半年使用:0次
名校
解题方法
8 . 双氰胺( )为白色晶体,在冷水中溶解度较小,溶于热水、乙醇,其水溶液在80℃以上会发生分解等副反应,主要用于生产树脂、涂料、含氮复合肥等。实验室以石灰氮
)为白色晶体,在冷水中溶解度较小,溶于热水、乙醇,其水溶液在80℃以上会发生分解等副反应,主要用于生产树脂、涂料、含氮复合肥等。实验室以石灰氮 为原料制备双氰胺的流程如下:
为原料制备双氰胺的流程如下:
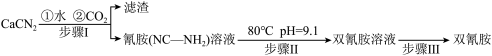
已知氰胺二聚反应机理为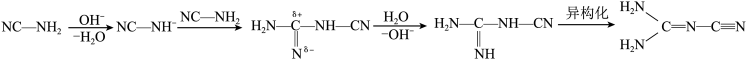
(1)已知:氰基是吸电子基团。氰氨
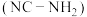 的碱性
的碱性(2)写出步骤Ⅰ的化学反应方程式:
(3)步骤Ⅱ中调节溶液pH为9.1,pH不能过低的原因:
(4)步骤Ⅲ中蒸发浓缩时,常采用真空蒸发浓缩,目的是
(5)凯氏定氮法是测定有机物中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐。
已知:
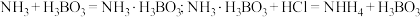

②仪器清洗后,g中加入硼酸
 和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭
和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭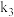 ,d中保留少量水。打开
,d中保留少量水。打开 ,加热b,使水蒸气进入e。
,加热b,使水蒸气进入e。d中保留少量水的目的是
③取双氰胺样品m克进行测定,滴定g中吸收液时消耗浓度为
 的盐酸VmL,则样品中氮的质量分数为
的盐酸VmL,则样品中氮的质量分数为
您最近半年使用:0次
解题方法
9 . 某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O;CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质如表所示:
(1)仪器A中发生反应的化学方程式为:______ 。
(2)装置B中的试剂是______ ,若撤去装置B,可能导致装置D中副产物______ (填化学式)的量增加;装置D可采用______ 加热的方法控制反应温度在70℃左右。
(3)装置D中球形冷凝管的作用为______ 。写出E中所有可能发生的无机反应的离子方程式:______ 。
(4)测定产品纯度:称取产品0.40g配成待测溶液,加入0.1000mol·L-1碘标准溶液22.00mL,再加入适量Na2CO3溶液,待反应完全后,加盐酸调节溶液的pH,立即用0.02000mol·L-1Na2S2O3溶液滴定至终点。进行三次平行实验,测得消耗Na2S2O3溶液20.00mL。则产品的纯度为______ 。(计算结果保留三位有效数字)
滴定的反应原理:CCl3CHO+OH-=CHCl3+HCOO-;HCOO-+I2=H++2I-+CO2↑;I2+2S2O =2I-+S4O
=2I-+S4O 。
。
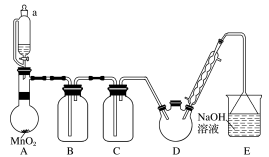
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O;CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质如表所示:
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
(2)装置B中的试剂是
(3)装置D中球形冷凝管的作用为
(4)测定产品纯度:称取产品0.40g配成待测溶液,加入0.1000mol·L-1碘标准溶液22.00mL,再加入适量Na2CO3溶液,待反应完全后,加盐酸调节溶液的pH,立即用0.02000mol·L-1Na2S2O3溶液滴定至终点。进行三次平行实验,测得消耗Na2S2O3溶液20.00mL。则产品的纯度为
滴定的反应原理:CCl3CHO+OH-=CHCl3+HCOO-;HCOO-+I2=H++2I-+CO2↑;I2+2S2O
 =2I-+S4O
=2I-+S4O 。
。
您最近半年使用:0次
名校
解题方法
10 . 苯甲酸乙酯可用于配制香水香精和人造精油,也可作为食用香精用于食品中。实验室可用苯甲酸与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略):
制备方法:
①在烧瓶C中加入一定量的下列物质(如表2)。按图甲所示安装好装置,加热烧瓶C.反应一段时间后,停止加热。
表2:试剂及用量
②将烧瓶C中的反应液倒入盛有30mL水的烧杯中,加入 ,至溶液呈中性。
,至溶液呈中性。
③用分液漏斗分出有机层,再用乙醚萃取水层中的残留产品,二者合并,加入图乙的烧瓶D中,加入沸石并加入无水硫酸镁,加热蒸馏,制得产品2.6mL。
回答下列问题:
(1)仪器A的名称是___________ ,仪器A和仪器B的自来水进水口分别为b口、d口,采用这种进水方式的原因是___________ 。
(2)环己烷、乙醇与水可形成共沸物,沸点为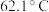 。烧瓶C的最佳加热方式是
。烧瓶C的最佳加热方式是___________ ,分水器的“分水”原理是___________ ,制备苯甲酸乙酯时,加入的环己烷的作用是___________ 。
(3) 的作用是
的作用是___________ 。
(4)采用图乙装置进行蒸馏操作,加入无水硫酸镁的目的是___________ 。
(5)该制备方法中苯甲酸乙酯的产率是___________ 。

| 物质 | 乙醇 | 苯甲酸 | 环己烷 | 乙醚 | 苯甲酸乙酯 |
密度 | 0.7893 | 1.2659 | 0.7785 | 0.7318 | 1.0500 |
熔点 | -114.0 | 122.1 | 6.5 | -116.3 | -34.6 |
沸点 | 78.5 | 249.0 | 80.0 | 34.5 | 211.0~213.0 |
①在烧瓶C中加入一定量的下列物质(如表2)。按图甲所示安装好装置,加热烧瓶C.反应一段时间后,停止加热。
表2:试剂及用量
| 物质 | 苯甲酸 | 乙醇 | 环己烷 | 浓硫酸 |
| 用量 | 2.44g | 15.0mL | 10.0mL | 3.0mL |
 ,至溶液呈中性。
,至溶液呈中性。③用分液漏斗分出有机层,再用乙醚萃取水层中的残留产品,二者合并,加入图乙的烧瓶D中,加入沸石并加入无水硫酸镁,加热蒸馏,制得产品2.6mL。
回答下列问题:
(1)仪器A的名称是
(2)环己烷、乙醇与水可形成共沸物,沸点为
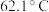 。烧瓶C的最佳加热方式是
。烧瓶C的最佳加热方式是(3)
 的作用是
的作用是(4)采用图乙装置进行蒸馏操作,加入无水硫酸镁的目的是
(5)该制备方法中苯甲酸乙酯的产率是
您最近半年使用:0次