1 . 下列物质的性质与用途对应关系错误的是
| A.聚合硫酸铁铝能水解形成胶体,可用作净水剂 |
| B.钠钾合金导热能力特别强,可用作原子反应堆的导热剂 |
| C.聚四氟乙烯具有抗酸碱、自润滑等性能,可用于制作滴定管活塞 |
| D.乙二醇水溶液凝固点很高,可作汽车发动机的抗冻剂 |
您最近半年使用:0次
2 . 某化学兴趣小组模拟侯氏制碱法制取Na2CO3产品并回收NH4Cl,设计如下实验方案。
Ⅰ.NaHCO3的制备,实验装置如图甲:
②向反应器中通入CO2气体,待溶液变为无色后,再加入10mL浓氨水,继续通入CO2.
③再加入10mL浓氨水,充分振荡,使NaCl完全溶解,继续通入过量CO2至生成大量NaHCO3晶体。
④将反应器冷却,然后抽滤,回收母液。用无水乙醇洗涤沉淀,收集NaHCO3晶体。
Ⅱ.Na2CO3的制备
将制得的NaHCO3晶体转移到已称量的蒸发皿中,加热至质量不再改变,停止加热,冷却到室温并称量。
Ⅲ.NH4Cl的回收
加热母液使NH4HCO3分解,滴加氨水至溶液呈碱性,操作b,抽滤,洗涤,置于干燥器中干燥,称重。
(1)仪器a的名称是_____ 。
(2)步骤③中通入过量CO2生成NaHCO3晶体的离子方程式为_____ 。
(3)已知0℃时NaHCO3的溶解度是0.8mol·L-1,不考虑溶液混合时体积的变化及对NaHCO3溶解度的影响,若10.0gNaCl全部转化成NaHCO3,则在0℃时从溶液中能析出NaHCO3固体_____ g(保留1位小数)。
(4)已知碳酸氢钠分解反应的ΔH=+135.6kJ·mol-1·K-1、ΔS=+333.3J·mol-1·K-1。在下列哪些温度下该反应能自发进行_____(填标号)。
(5)①回收NH4Cl时加入氨水的目的是_____ 。
②结合图乙,简单说明操作b的过程_____ 。
(6)若制得的NaHCO3中含有未反应的NaCl,则分解后所得固体的质量_____ (填“大于”、“小于”或“等于”)理论上生成Na2CO3的质量。
Ⅰ.NaHCO3的制备,实验装置如图甲:

②向反应器中通入CO2气体,待溶液变为无色后,再加入10mL浓氨水,继续通入CO2.
③再加入10mL浓氨水,充分振荡,使NaCl完全溶解,继续通入过量CO2至生成大量NaHCO3晶体。
④将反应器冷却,然后抽滤,回收母液。用无水乙醇洗涤沉淀,收集NaHCO3晶体。
Ⅱ.Na2CO3的制备
将制得的NaHCO3晶体转移到已称量的蒸发皿中,加热至质量不再改变,停止加热,冷却到室温并称量。
Ⅲ.NH4Cl的回收
加热母液使NH4HCO3分解,滴加氨水至溶液呈碱性,操作b,抽滤,洗涤,置于干燥器中干燥,称重。
(1)仪器a的名称是
(2)步骤③中通入过量CO2生成NaHCO3晶体的离子方程式为
(3)已知0℃时NaHCO3的溶解度是0.8mol·L-1,不考虑溶液混合时体积的变化及对NaHCO3溶解度的影响,若10.0gNaCl全部转化成NaHCO3,则在0℃时从溶液中能析出NaHCO3固体
(4)已知碳酸氢钠分解反应的ΔH=+135.6kJ·mol-1·K-1、ΔS=+333.3J·mol-1·K-1。在下列哪些温度下该反应能自发进行_____(填标号)。
| A.308K | B.373K | C.421K | D.573K |
(5)①回收NH4Cl时加入氨水的目的是
②结合图乙,简单说明操作b的过程
(6)若制得的NaHCO3中含有未反应的NaCl,则分解后所得固体的质量
您最近半年使用:0次
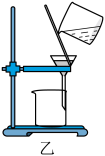
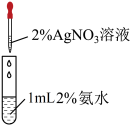
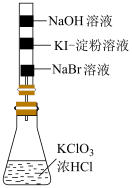
3 . 利用下列仪器或实验装置能够达到相关目的的是
|
|
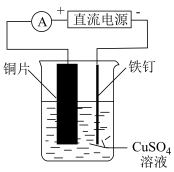
A.用装置甲测定溶液的 | B.用装置乙分离 胶体和 胶体和 溶液 溶液 |
|
|
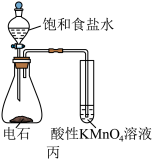
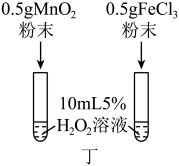
| C.用装置丙检验乙炔具有还原性 | D.用装置丁比较 和 和 对 对 分解的催化效果 分解的催化效果 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
4 . 下列有关实验室仪器和试剂的使用说法错误的是
| A.进行钾与水反应的实验,可用培养皿代替小烧杯 |
B.实验室使用试管和烧瓶加热液体时,所盛液体体积应介于其容积的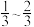 之间 之间 |
| C.制备硝基苯时用到的混酸,可通过将浓硫酸缓缓注入浓硝酸中获得 |
| D.用苯进行萃取溴水中的溴的实验时,振荡后打开分液漏斗的活塞及时放气 |
您最近半年使用:0次
5 . 下列由废易拉罐制取 的实验原理与装置不能达到实验目的的是
的实验原理与装置不能达到实验目的的是
 的实验原理与装置不能达到实验目的的是
的实验原理与装置不能达到实验目的的是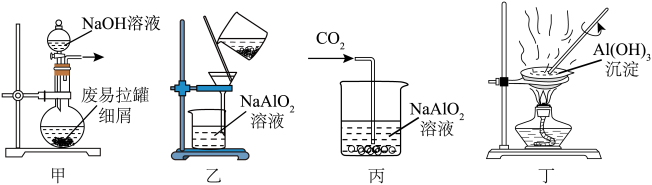
| A.用装置甲溶解废易拉罐细屑 | B.用装置乙过滤得到Na[Al(OH)4]溶液 |
C.用装置丙制取 沉淀 沉淀 | D.用装置丁灼烧 制取 制取 |
您最近半年使用:0次
昨日更新
|
192次组卷
|
2卷引用:江苏省南京市2024届高三下学期第二次模拟考试化学试题
解题方法
6 . 实验是进行科学探究的重要方式。下列叙述正确的是
| A.过滤适用于过滤胶状氢氧化物类沉淀 |
| B.用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸 |
| C.某些强氧化剂(如高锰酸钾)与葡萄糖的混合物不能研磨,否则可能引起爆炸 |
| D.除去碱式滴定管胶管内的气泡时,将尖嘴垂直向下,挤压胶管内玻璃球将气泡排出 |
您最近半年使用:0次
7 . 氮化镁是一种重要的化工原料,易水解。某兴趣小组拟选用如下装置,利用氮气和镁反应制备氮化镁(部分夹持装置已略去)。
(1)盛放亚硝酸钠饱和溶液的仪器为_____ (填仪器名称),该仪器使用前需要进行的实验操作为_____ 。
(2)利用上述装置完成实验(部分装置可重复使用,缓冲瓶只需连接装置B后),按气流方向从左到右正确的连接顺序为_____ (填仪器接口的小写字母);缓冲瓶的作用是防止倒吸,造成倒吸的可能原因为_____ 。
(3)装置A中发生反应的离子方程式为_____ 。
(4)请你设计一个实验,证明镁粉已经完全反应,写出实验简要步骤及观察到的现象:_____ 。
(5)所得氮化镁纯度的测定:
步骤一、取 所得产品浸泡在足量浓
所得产品浸泡在足量浓 溶液中,加热,将生成的
溶液中,加热,将生成的 全部蒸出并用
全部蒸出并用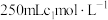 的盐酸(过量)吸收。
的盐酸(过量)吸收。
步骤二、准确量取 吸收液于锥形瓶中,滴入几滴指示剂,用
吸收液于锥形瓶中,滴入几滴指示剂,用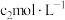 标准
标准 溶液滴定至终点。
溶液滴定至终点。
步骤三、重复步骤二实验两次,平均消耗标准 溶液的体积为
溶液的体积为 。
。
①蒸氨时,若温度过高,可能造成盐酸中 的挥发,会造成最终测定结果
的挥发,会造成最终测定结果_____ (填“偏大”“偏小”或“无影响”)。
②步骤二中指示剂最好选用_____ (填“酚酞”或“甲基橙”)。
③通过上述实验测得的产品纯度为_____ (用含 的代数式表示)。
的代数式表示)。

(1)盛放亚硝酸钠饱和溶液的仪器为
(2)利用上述装置完成实验(部分装置可重复使用,缓冲瓶只需连接装置B后),按气流方向从左到右正确的连接顺序为
(3)装置A中发生反应的离子方程式为
(4)请你设计一个实验,证明镁粉已经完全反应,写出实验简要步骤及观察到的现象:
(5)所得氮化镁纯度的测定:
步骤一、取
 所得产品浸泡在足量浓
所得产品浸泡在足量浓 溶液中,加热,将生成的
溶液中,加热,将生成的 全部蒸出并用
全部蒸出并用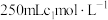 的盐酸(过量)吸收。
的盐酸(过量)吸收。步骤二、准确量取
 吸收液于锥形瓶中,滴入几滴指示剂,用
吸收液于锥形瓶中,滴入几滴指示剂,用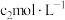 标准
标准 溶液滴定至终点。
溶液滴定至终点。步骤三、重复步骤二实验两次,平均消耗标准
 溶液的体积为
溶液的体积为 。
。①蒸氨时,若温度过高,可能造成盐酸中
 的挥发,会造成最终测定结果
的挥发,会造成最终测定结果②步骤二中指示剂最好选用
③通过上述实验测得的产品纯度为
 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
解题方法
8 . 水热法制备 的流程如图,下列叙述正确的是
的流程如图,下列叙述正确的是
 的流程如图,下列叙述正确的是
的流程如图,下列叙述正确的是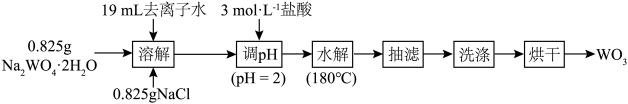
| A.本实验使用托盘天平称量 | B. 作反应的氧化剂 作反应的氧化剂 |
C.调 为2的目的是促进反应完全 为2的目的是促进反应完全 | D.用 溶液检验产品是否洗净 溶液检验产品是否洗净 |
您最近半年使用:0次
9 . 下述装置或操作能实现相应实验目的的是
| 装置或操作 |
|
|
| 实验目的 | 铁钉表面镀铜 | 配制银氨溶液 |
| 选项 | A | B |
| 装置或操作 |
|
|
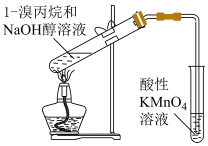
| 实验目的 | 验证氧化性:Cl2>Br2>I2 | 检验1-溴丙烷的消去反应产物丙烯 |
| 选项 | C | D |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
10 . 二茂铁(化学式为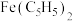 )常温下是一种橙黄色针状晶体,熔点为173℃,易升华,能进行一系列的取代反应,可用作紫外吸收剂、火箭燃料添加剂。实验室合成二茂铁的步骤如下:
)常温下是一种橙黄色针状晶体,熔点为173℃,易升华,能进行一系列的取代反应,可用作紫外吸收剂、火箭燃料添加剂。实验室合成二茂铁的步骤如下: ,开始搅拌;
,开始搅拌;
②向仪器A中分批次加入8.125g无水 ,然后加入2.000g还原铁粉,水浴加热回流。反应结束除去多余的反应物后将回流装置改为减压蒸馏装置,蒸去溶剂;
,然后加入2.000g还原铁粉,水浴加热回流。反应结束除去多余的反应物后将回流装置改为减压蒸馏装置,蒸去溶剂;
③反应器冷却后,再改成回流装置并继续通入 ,逐滴加入事先混合好的足量
,逐滴加入事先混合好的足量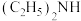 (二乙胺)
(二乙胺) (环戊二烯)的混合液,搅拌加热反应;
(环戊二烯)的混合液,搅拌加热反应;
④反应结束后蒸去溶剂,析出粗品,然后以升华法提纯。
回答下列问题:
(1)仪器A的名称为___________ ,仪器B的作用是___________ 。
(2)步骤①中通入 的作用是
的作用是___________ 。
(3)写出在步骤②中仪器A内发生反应的化学方程式___________ 。
(4)已知步骤③中二乙胺反应后生成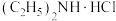 ,写出制备二茂铁的化学反应方程式
,写出制备二茂铁的化学反应方程式___________ 。
(5)采用图2所示装置进行升华法提纯时,粗品二茂铁放在___________ (填“蒸发皿”或“带孔滤纸”)上,装置中漏斗颈处棉花的作用是___________ 。___________ 。(保留4位有效数字)
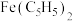 )常温下是一种橙黄色针状晶体,熔点为173℃,易升华,能进行一系列的取代反应,可用作紫外吸收剂、火箭燃料添加剂。实验室合成二茂铁的步骤如下:
)常温下是一种橙黄色针状晶体,熔点为173℃,易升华,能进行一系列的取代反应,可用作紫外吸收剂、火箭燃料添加剂。实验室合成二茂铁的步骤如下: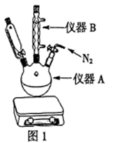
 ,开始搅拌;
,开始搅拌;②向仪器A中分批次加入8.125g无水
 ,然后加入2.000g还原铁粉,水浴加热回流。反应结束除去多余的反应物后将回流装置改为减压蒸馏装置,蒸去溶剂;
,然后加入2.000g还原铁粉,水浴加热回流。反应结束除去多余的反应物后将回流装置改为减压蒸馏装置,蒸去溶剂;③反应器冷却后,再改成回流装置并继续通入
 ,逐滴加入事先混合好的足量
,逐滴加入事先混合好的足量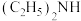 (二乙胺)
(二乙胺) (环戊二烯)的混合液,搅拌加热反应;
(环戊二烯)的混合液,搅拌加热反应;④反应结束后蒸去溶剂,析出粗品,然后以升华法提纯。
回答下列问题:
(1)仪器A的名称为
(2)步骤①中通入
 的作用是
的作用是(3)写出在步骤②中仪器A内发生反应的化学方程式
(4)已知步骤③中二乙胺反应后生成
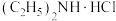 ,写出制备二茂铁的化学反应方程式
,写出制备二茂铁的化学反应方程式(5)采用图2所示装置进行升华法提纯时,粗品二茂铁放在

您最近半年使用:0次