1 . 已知反应:
①
②
③
请根据上述反应判断氧化性由强到弱的顺序是
①

②

③

请根据上述反应判断氧化性由强到弱的顺序是
A.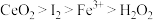 | B. |
C.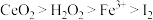 | D.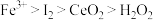 |
您最近半年使用:0次
名校
解题方法
2 . 下列实验操作和现象能得出相应结论或达到相应目的的是
| 选项 | 实验操作、现象 | 结论或目的 |
| A | 向某样品溶液中加入NaOH溶液并微热,产生能使湿润的蓝色石蕊试纸变红的气体 | 该样品中一定含 |
| B | 向某样品溶液中加入 溶液,生成白色沉淀,再加入硝酸,沉淀不溶解 溶液,生成白色沉淀,再加入硝酸,沉淀不溶解 | 该样品中一定含 |
| C | 向硫酸酸化的 溶液中滴入 溶液中滴入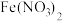 ,溶液变黄 ,溶液变黄 | 比较氧化性: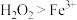 |
| D | 向 溶液中通入少量的氯气,出现淡黄色浑浊 溶液中通入少量的氯气,出现淡黄色浑浊 | 氯气的氧化性大于硫 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
3 . Ⅰ.氯水具有多种性质,该小组同学用足量氯水分别与 溶液,
溶液, 溶液和
溶液和 溶液反应。完成下列问题:
溶液反应。完成下列问题:
已知:常温下发生反应:i. ;ii:
;ii:
(1)证明氯水中含有盐酸,可选择的试剂是________ 溶液(选填“石蕊溶液”或“ ”)。
”)。
(2)氯水与 溶液反应能证明氯水具有氧化性。请补充完整足量氯水与
溶液反应能证明氯水具有氧化性。请补充完整足量氯水与 溶液反应的离子方程式:
溶液反应的离子方程式:________ 。
________ ________
________ ________
________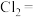 ________
________ ________
________ ________
________
Ⅱ.该小组同学在实验室中利用下图装置(部分装置省略)制备 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
(3)写出装置①中制取氯气的离子方程式________ 。
(4)装置②盛装的试剂是________ ,其作用是________ 。
(5)装置③中反应化学方程式为________ ,反应结束后,取出③中试管,经冷却结晶,过滤,少量(冷)水洗涤,干燥,得到 晶体。
晶体。
(6)装置④中采用冰水浴冷却的目的是________ 。
(7)取少量 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫色。根据上述实验,以下结论正确的是________
层显紫色。根据上述实验,以下结论正确的是________
 溶液,
溶液, 溶液和
溶液和 溶液反应。完成下列问题:
溶液反应。完成下列问题:已知:常温下发生反应:i.
 ;ii:
;ii:
(1)证明氯水中含有盐酸,可选择的试剂是
 ”)。
”)。(2)氯水与
 溶液反应能证明氯水具有氧化性。请补充完整足量氯水与
溶液反应能证明氯水具有氧化性。请补充完整足量氯水与 溶液反应的离子方程式:
溶液反应的离子方程式:________
 ________
________ ________
________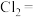 ________
________ ________
________ ________
________
Ⅱ.该小组同学在实验室中利用下图装置(部分装置省略)制备
 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。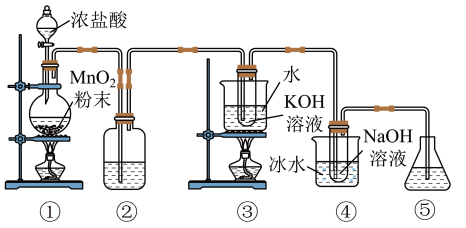
(3)写出装置①中制取氯气的离子方程式
(4)装置②盛装的试剂是
(5)装置③中反应化学方程式为
 晶体。
晶体。(6)装置④中采用冰水浴冷却的目的是
(7)取少量
 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫色。根据上述实验,以下结论正确的是________
层显紫色。根据上述实验,以下结论正确的是________A.氧化性: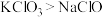 | B.氧化性: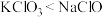 |
C.还原性: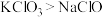 | D.还原性: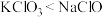 |
您最近半年使用:0次
解题方法
4 . 对于下列实验,能正确描述其反应的离子方程式是
| A.FeSO4溶液与溴水反应:2Fe2++Br2=2Fe3++2Br- |
| B.向CaCl2溶液中通入CO2:Ca2++H2O+CO2=CaCO3↓+2H+ |
| C.向H2O2溶液中滴加少量FeCl3:2Fe3++H2O2=O2↑+2H++2Fe2+ |
D.同浓度同体积NH4HSO4溶液与NaOH溶液混合: +OH-=NH3·H2O +OH-=NH3·H2O |
您最近半年使用:0次
名校
解题方法
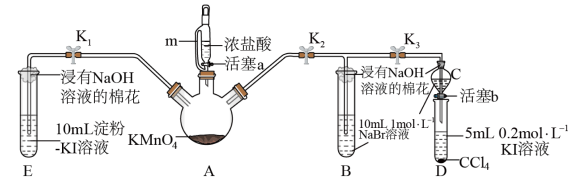
5 . 为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
I.打开 关闭
关闭 ,
, ,打开活塞a,滴加浓盐酸。
,打开活塞a,滴加浓盐酸。
Ⅱ.关闭 ,打开
,打开 ,
, ,当B和C中的溶液都变为黄色时,关闭
,当B和C中的溶液都变为黄色时,关闭 。
。
Ⅲ.B中继续通气体,当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)装置A中m的作用为__________________ 。
(2)能说明氯气的氧化性强于碘的实验现象是___________________ 。
(3)用离子方程式解释过程Ⅱ中溶液变为黄色的原因:_________________ 。
(4)过程V的目的是验证溴的氧化性强于碘,简述其操作过程___________________ 。
(5)过程Ⅲ实验的目的是____________________ 。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下________________ ,得电子能力逐渐减弱。
I.打开
 关闭
关闭 ,
, ,打开活塞a,滴加浓盐酸。
,打开活塞a,滴加浓盐酸。Ⅱ.关闭
 ,打开
,打开 ,
, ,当B和C中的溶液都变为黄色时,关闭
,当B和C中的溶液都变为黄色时,关闭 。
。Ⅲ.B中继续通气体,当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)装置A中m的作用为
(2)能说明氯气的氧化性强于碘的实验现象是
(3)用离子方程式解释过程Ⅱ中溶液变为黄色的原因:
(4)过程V的目的是验证溴的氧化性强于碘,简述其操作过程
(5)过程Ⅲ实验的目的是
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下
您最近半年使用:0次
6 . 已知氯酸钠与浓盐酸反应的化学方程式为NaClO3+6HCl(浓)=NaCl+3Cl2↑+3H2O。下列说法正确的是
| A.该反应每生成3molCl2,转移6NA个电子 |
| B.NaClO3是氧化剂,发生还原反应 |
| C.还原性:Cl2>HCl |
| D.氧化剂与还原剂的物质的量之比为1∶6 |
您最近半年使用:0次
名校
解题方法
7 . 某校化学实验兴趣小组同学设计了如图所示的实验装置(支撑用的铁架台省略),探究实验室制备 并验证氯气的某些性质。
并验证氯气的某些性质。 (标准状况下),则被氧化的
(标准状况下),则被氧化的
___________  ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为___________ 。
(2)A中产生白色沉淀,甲同学认为是 与水反应产生
与水反应产生 的结果,写出其中发生反应的离子方程式
的结果,写出其中发生反应的离子方程式___________ ,___________ 。
(3)乙同学则认为A中的现象不足以说明白色沉淀是 与水反应产生
与水反应产生 的结果,因为生成的
的结果,因为生成的 中混有杂质
中混有杂质 ,所以应在A之前增加一个洗气瓶除去
,所以应在A之前增加一个洗气瓶除去 ,洗气瓶中所盛试剂是
,洗气瓶中所盛试剂是___________ 。
(4)装置C和D中出现的不同现象说明的问题是___________ 。
(5)装置E上面蘸有下列浓溶液的棉花可用于吸收氯气的是___________ (填字母)。
a. 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.浓硫酸 e.
溶液 d.浓硫酸 e. 溶液
溶液
(6)设计装置E、F的目的是比较 、
、 、
、 的氧化性,反应一段时间后,观察到装置E中的现象是
的氧化性,反应一段时间后,观察到装置E中的现象是___________ ,然后打开装置E的活塞,将E中的少量溶液加到装置F中,振荡,观察到的现象是___________ ,甲同学认为据上述现象可以说明氧化性 ,乙同学却认为不可以说明,理由是
,乙同学却认为不可以说明,理由是___________ 。
 并验证氯气的某些性质。
并验证氯气的某些性质。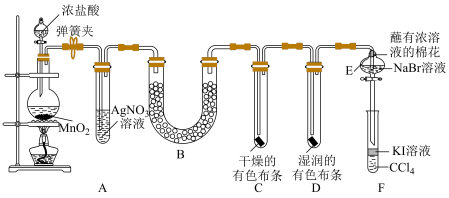
 (标准状况下),则被氧化的
(标准状况下),则被氧化的
 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为(2)A中产生白色沉淀,甲同学认为是
 与水反应产生
与水反应产生 的结果,写出其中发生反应的离子方程式
的结果,写出其中发生反应的离子方程式(3)乙同学则认为A中的现象不足以说明白色沉淀是
 与水反应产生
与水反应产生 的结果,因为生成的
的结果,因为生成的 中混有杂质
中混有杂质 ,所以应在A之前增加一个洗气瓶除去
,所以应在A之前增加一个洗气瓶除去 ,洗气瓶中所盛试剂是
,洗气瓶中所盛试剂是(4)装置C和D中出现的不同现象说明的问题是
(5)装置E上面蘸有下列浓溶液的棉花可用于吸收氯气的是
a.
 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.浓硫酸 e.
溶液 d.浓硫酸 e. 溶液
溶液(6)设计装置E、F的目的是比较
 、
、 、
、 的氧化性,反应一段时间后,观察到装置E中的现象是
的氧化性,反应一段时间后,观察到装置E中的现象是 ,乙同学却认为不可以说明,理由是
,乙同学却认为不可以说明,理由是
您最近半年使用:0次
名校
8 . 高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
)是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
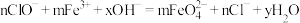 ,回答下列问题:
,回答下列问题:
(1)上述反应中的
___________ ,
___________ 。
(2)上述反应中还原产物为___________ ,氧化性强弱:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(3)请用双线桥法表示以下反应中电子的转移情况:___________ 。
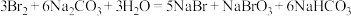
 )是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
)是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为: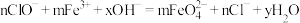 ,回答下列问题:
,回答下列问题:(1)上述反应中的


(2)上述反应中还原产物为

 (填“>”或“<”)。
(填“>”或“<”)。(3)请用双线桥法表示以下反应中电子的转移情况:
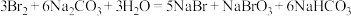
您最近半年使用:0次
名校
解题方法
9 . 已知还原性: ,则将
,则将 通入到
通入到 、
、 、
、 的混合溶液中,
的混合溶液中, 、
、 、
、 生成的先后顺序为
生成的先后顺序为
 ,则将
,则将 通入到
通入到 、
、 、
、 的混合溶液中,
的混合溶液中, 、
、 、
、 生成的先后顺序为
生成的先后顺序为A. , , , , | B. , , , , | C. , , , , | D. , , , , |
您最近半年使用:0次
名校
解题方法
10 . 下列实验操作、现象及结论正确的是
| 选项 | 实验设计 | 现象 | 实验结论 |
| A | 在医用酒精中加一块绿豆大的钠 | 产生气泡 | 乙醇中断裂氢氧键 |
| B | 分别测定等物质的量浓度的HCOONH4和NH4HS溶液的pH | 后者pH大 | 酸性:HCOOH>H2S |
| C | 向含0.1mol溶质的FeI2溶液中通入0.1molCl2,再滴加淀粉溶液 | 溶液变蓝色 | 还原性:I->Fe2+ |
| D | 向2mL氯乙烷样品中,加入5mL20%KOH的溶液并加热,冷却到室温后,再滴加AgNO3溶液 | 溶液变浑浊 | 氯乙烷含有氯元素 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



