1 . 下列对化学实验及现象的解释不合理的是
| 选项 | 化学实验及现象 | 解释 |
| A | 分别向浓度均为0.1 的 的 和 和 溶液中通入 溶液中通入 至饱和,前者无明显现象,后者生成沉淀 至饱和,前者无明显现象,后者生成沉淀 | 溶度积常数: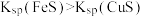 |
| B | 将 分别通入品红的乙醇溶液和品红的水溶液中,品红的乙醇溶液不褪色,品红的水溶液逐渐褪色 分别通入品红的乙醇溶液和品红的水溶液中,品红的乙醇溶液不褪色,品红的水溶液逐渐褪色 | 使品红褪色的不是 而是 而是 与水反应后的产物 与水反应后的产物 |
| C | 向KI溶液中加入少量氯水和 ,振荡、静置,下层溶液为紫红色 ,振荡、静置,下层溶液为紫红色 | 还原性: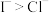 |
| D | 向0.01  溶液中,加入少量 溶液中,加入少量 固体,溶液颜色加深 固体,溶液颜色加深 |  水解程度增大 水解程度增大 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
2 . 向含 、
、 、
、 的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
 、
、 、
、 的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
A.原溶液中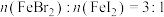 | B.线段II表示 的变化情况 的变化情况 |
C.线段IV表示 的变化情况 的变化情况 | D.根据图像可计算出a=5 |
您最近半年使用:0次
2024高三·全国·专题练习
3 . 根据下列实验现象所得出的结论正确的是
A.向某溶液中加入足量氯化钡溶液,生成白色沉淀,证明该溶液中含SO |
| B.向Na2S溶液中通入足量SO2,生成淡黄色沉淀,证明SO2具有酸性和氧化性 |
| C.向FeI2溶液中滴加少量氯水,溶液变为黄色,证明氧化性:Cl2>Fe3+ |
D.向某溶液中加入NaOH稀溶液,用湿润的蓝色石蕊试纸检验生成的气体时无颜色变化,证明该溶液中无NH |
您最近半年使用:0次
2024高三·全国·专题练习
4 . 自来水中的余氯可用大苏打(Na2S2O3)除去,其反应的离子方程式为S2O +4Cl2+5H2O=2SO
+4Cl2+5H2O=2SO +8Cl-+10H+。下列关于该反应的说法正确的是
+8Cl-+10H+。下列关于该反应的说法正确的是
 +4Cl2+5H2O=2SO
+4Cl2+5H2O=2SO +8Cl-+10H+。下列关于该反应的说法正确的是
+8Cl-+10H+。下列关于该反应的说法正确的是| A.Na2S2O3被还原 | B.氧化性:SO >Cl2 >Cl2 |
C.H2O的电子式为 | D.可用AgNO3溶液检验还原产物 |
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
5 . 根据实验方案和现象,判断下列结论正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 将过量Cl2通入淀粉—碘化钾溶液中 | 溶液颜色最终未变蓝 | 说明Cl2不能氧化I- |
| B | 向0.1 mol·L-1 Na2S溶液中加入H2O2 | 产生淡黄色沉淀 | H2O2将S2-氧化为S |
| C | 在Ca(ClO)2溶液中通入SO2 | 产生白色沉淀 | 酸性:H2SO3>HClO |
| D | 用pH试纸分别测定1 mol·L-1的Na2S和1 mol·L-1的NaCl溶液的pH | 前者的试纸颜色比后者深 | 非金属性:S<Cl |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
6 . 已知Ⅰ: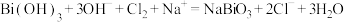 ;
;
Ⅱ.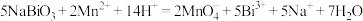 。下列推断不正确的是
。下列推断不正确的是
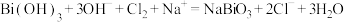 ;
;Ⅱ.
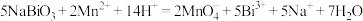 。下列推断不正确的是
。下列推断不正确的是A. 可与盐酸发生反应: 可与盐酸发生反应: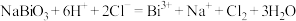 |
B.任何条件下,都存在氧化性: |
C.反应Ⅱ中,当有10.45g 生成时转移电子数为 生成时转移电子数为 |
D.已知 可由 可由 与王水(浓硝酸和浓盐酸的混合物)反应制取,说明 与王水(浓硝酸和浓盐酸的混合物)反应制取,说明 不能被硝酸氧化 不能被硝酸氧化 |
您最近半年使用:0次
7 . 氮和氧是构建化合物的常见元素。
(1)下列说法正确的是___________。
(2)①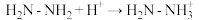 ,其中
,其中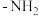 的
的 原子杂化方式为
原子杂化方式为___________ ;比较键角 中的-NH2
中的-NH2_____ H2N-NH 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由___________ 。
②将 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是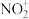 。比较氧化性强弱:NO
。比较氧化性强弱:NO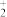
_____ HNO3(填“>”、“<”或“=”);写出A中阴离子的结构式___________ 。
已知: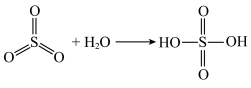
(1)下列说法正确的是___________。
A.电负性: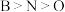 | B.离子半径: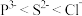 |
C.第一电离能: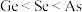 | D.基态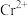 的简化电子排布式: 的简化电子排布式: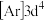 |
(2)①
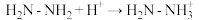 ,其中
,其中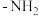 的
的 原子杂化方式为
原子杂化方式为 中的-NH2
中的-NH2 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由②将
 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是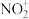 。比较氧化性强弱:NO
。比较氧化性强弱:NO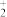
您最近半年使用:0次
2024高三·全国·专题练习
8 . 室温下,下列实验探究方案、现象得出的结论错误的是
| 选项 | 探究方案 | 现象 | 结论 |
| A | 向5mL0.1mol·L-1KI溶液中加入1mL0.1mol·L-1FeCl3溶液,充分反应后用苯萃取2~3次,取水层滴加KSCN溶液 | 溶液变红色 | 反应:2Fe3++2I-=2Fe2++I2有一定限度 |
| B | 将Na[Al(OH)4]溶液与NaHCO3溶液混合,观察现象 | 产生白色沉淀 | 结合质子能力:[Al(OH)4]-> |
| C | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,观察溶液颜色变化 | 溶液变黄色 | 氧化性:H2O2>Fe3+ |
| D | 用pH计测量等温等浓度的CH3COONa和HCOONa溶液的pH | pH:前者更大 | Kh(CH3COO-)>Kh(HCOO-) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 实验是学习化学的基础。已知:[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-呈无色。根据实验操作及现象,下列结论中正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向FeCl3溶液中滴K3[Fe(CN)6]溶液,再加入少量铜粉 | 开始时无明显变化,加入铜粉后产生蓝色沉淀 | 氧化性:Fe3+>Cu2+ |
| B | 将C2H5Br与NaOH溶液共热。冷却后,加入AgNO3溶液 | 没有产生淡黄色沉淀 | C2H5Br没有发生水解反应 |
| C | 将CoCl2固体溶于水,加入适量浓盐酸后,再加入少量ZnCl2固体 | 溶液先由粉红色变为蓝色,再由蓝色变成无色 | 稳定性:[CoCl4]2->[ZnCl4]2- |
| D | 常温下,分别测定1mol/LCH3COONH4溶液和0.1mol/LCH3COONH4溶液的pH | pH都等于7 | 同温下,不同浓度CH3COONH4溶液中水的电离程度相同 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
10 . 通过下列实验操作和实验现象,得到的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用pH试纸测溶液pH | NaHCO3显蓝色,NaHSO3显红色 | H2CO3、H2SO3均是弱酸 |
| B | 向钾盐溶液中滴加浓盐酸 | 产生的无色气体使品红溶液褪色 | 该钾盐一定是K2SO3或KHSO3 |
| C | 向含有等量KBr、KI混合溶液中依次加入少量新制氯水和CCl4,振荡、静置 | 溶液分层,下层呈紫红色 | 氧化性:Cl2>Br2>I2 |
| D | 在火焰上灼烧搅拌过某无色溶液的玻璃棒 | 火焰出现黄色 | 不能确定溶液中含有Na元素 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



