1 . 化学学习小组欲探究铁及其化合物的氧化性和还原性。请你协助他们完成实验报告。
实验目的:探究铁及其化合物的氧化性和还原性。
实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、 溶液、铁粉、锌片、铜片、稀硫酸。
溶液、铁粉、锌片、铜片、稀硫酸。
仪器:胶头滴管、试管、烧杯等。
(1)实验记录(仿照①实验作答,填写空白部分)。
(2)在实验②中,有部分同学在氯化亚铁溶液中滴入  溶液后,出现了红色,你认为是什么原因:
溶液后,出现了红色,你认为是什么原因:___________ ;你对实验员在配制氯化亚铁溶液时,提出的建议是___________ 。
实验目的:探究铁及其化合物的氧化性和还原性。
实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、
 溶液、铁粉、锌片、铜片、稀硫酸。
溶液、铁粉、锌片、铜片、稀硫酸。仪器:胶头滴管、试管、烧杯等。
(1)实验记录(仿照①实验作答,填写空白部分)。
| 序号 | 实验设计 | 实验现象 | 离子方程式 | 解释与结论 |
| ① | 在铁粉中滴入稀硫酸 | 铁粉溶解,溶液由无色变成浅绿色,生成无色无味气体 | 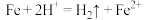 |  具有还原性 具有还原性 |
| ② |  溶液中滴入 溶液中滴入  溶液,再加氯水 溶液,再加氯水 | 滴入 溶液无明显变化,加入氯水立即变成红色 溶液无明显变化,加入氯水立即变成红色 | ||
| ③ |  溶液中加入锌片 溶液中加入锌片 |  | ||
| ④ |  |  具有氧化性 具有氧化性 |
 溶液后,出现了红色,你认为是什么原因:
溶液后,出现了红色,你认为是什么原因:
您最近一年使用:0次
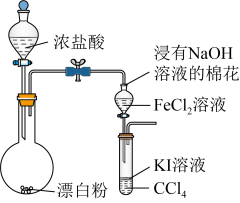
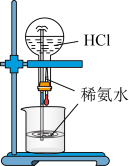
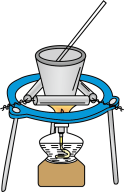
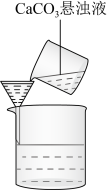
2 . 下列实验所选择的装置和试剂对应且正确的是
|
|
A.比较 、 、 、 、 的氧化性 的氧化性 | B.喷泉实验 |
|
|
C.从 溶液中得到 溶液中得到 固体 固体 | D.固液分离 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 根据以下几个反应:①I2+H2S═2HI+S↓,②2FeCl2+Cl2═2FeCl3,③2FeCl3+2KI═2FeCl2+2KCl+I2,判断下列微粒氧化性由强到弱的顺序是
| A. Cl2>I2>FeCl3>S |
| B. Cl2>FeCl3>I2>S |
| C. FeCl3>Cl2>I2>S |
| D. S>I2>FeCl3>Cl2 |
您最近一年使用:0次
4 . 已知下述三个实验均能发生化学反应:
下列判断正确的是
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴氯水 | 将铜丝放入氯化铁溶液中 |
| A.实验①中铁钉只作还原剂 | B.实验②中 既显氧化性又显还原性 既显氧化性又显还原性 |
| C.实验③中发生的是置换反应 | D.上述实验证明氧化性: |
您最近一年使用:0次
5 . 铅与碳是同族元素,有 两种价态,铅的氧化物均难溶于水,已知有下列两个反应:①
两种价态,铅的氧化物均难溶于水,已知有下列两个反应:① ;②
;② 。下列有关叙述不正确的是
。下列有关叙述不正确的是
 两种价态,铅的氧化物均难溶于水,已知有下列两个反应:①
两种价态,铅的氧化物均难溶于水,已知有下列两个反应:① ;②
;② 。下列有关叙述不正确的是
。下列有关叙述不正确的是A. 可写成 可写成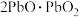 的形式 的形式 |
B.反应②中 是氧化产物 是氧化产物 |
C.生成相同质量的 ,反应①②转移电子数之比为 ,反应①②转移电子数之比为 |
D.根据反应可推测在题给条件下氧化性: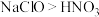 |
您最近一年使用:0次
6 . 已知有如下反应:①ClO +5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是
+5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是
 +5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是
+5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是| A.I->Cl->Fe2+>Cl2 | B.Fe2+>I->Cl->Cl2 |
| C.I->Fe2+>Cl->Cl2 | D.I->Cl->Fe2+>Cl2 |
您最近一年使用:0次
7 . 已知反应:
①
②
③
请根据上述反应判断氧化性由强到弱的顺序是
①

②

③

请根据上述反应判断氧化性由强到弱的顺序是
A.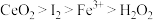 | B. |
C.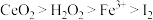 | D.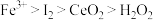 |
您最近一年使用:0次
8 . 已知氯酸钠与浓盐酸反应的化学方程式为NaClO3+6HCl(浓)=NaCl+3Cl2↑+3H2O。下列说法正确的是
| A.该反应每生成3molCl2,转移6NA个电子 |
| B.NaClO3是氧化剂,发生还原反应 |
| C.还原性:Cl2>HCl |
| D.氧化剂与还原剂的物质的量之比为1∶6 |
您最近一年使用:0次
解题方法
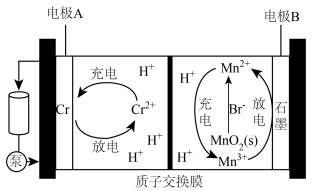
9 . 中科院大连化物所储能技术研究部提出了一种基于 辅助
辅助 放电的混合型液流电池,装置如图所示,下列说法错误的是
放电的混合型液流电池,装置如图所示,下列说法错误的是
 辅助
辅助 放电的混合型液流电池,装置如图所示,下列说法错误的是
放电的混合型液流电池,装置如图所示,下列说法错误的是
A.充电时, 向电极A迁移 向电极A迁移 |
B.在放电过程中,可利用 及时清除电极B上的“死锰” 及时清除电极B上的“死锰”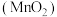 ,提高充放电过程的可逆性 ,提高充放电过程的可逆性 |
C.放电时,电极B上还可能发生: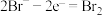 |
D.放电时,在该环境下的氧化性: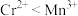 |
您最近一年使用:0次
10 . 依据下列实验和现象,得出结论正确的是
选项 | 实验 | 现象 | 结论 |
A | 向 | 有白色沉淀生成 | 酸性: |
B | 激光灯照射蛋白质溶液 | 观察到“光亮的通路” | 蛋白质溶液属于胶体 |
C | 向 | 溶液变蓝 | 氧化性: |
D | 向葡萄糖溶液中滴加酸性 | 酸性 | 葡萄糖中含有醛基 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 溶液中通入
溶液中通入 气体
气体
 的
的 溶液中滴加KI-淀粉溶液
溶液中滴加KI-淀粉溶液
 溶液
溶液

