1 . 依据下列实验和现象,得出结论正确的是
选项 | 实验 | 现象 | 结论 |
A | 向 | 有白色沉淀生成 | 酸性: |
B | 激光灯照射蛋白质溶液 | 观察到“光亮的通路” | 蛋白质溶液属于胶体 |
C | 向 | 溶液变蓝 | 氧化性: |
D | 向葡萄糖溶液中滴加酸性 | 酸性 | 葡萄糖中含有醛基 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 高铁酸钠(Na2FeO4)是一种新型、高效、多功能的水处理剂。高铁酸钠(Na2FeO4)制备方法有:
湿法制备:
干法制备: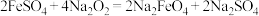 。
。
有关分析错误的是
湿法制备:

干法制备:
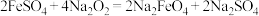 。
。有关分析错误的是
A.干法制备中每生成 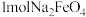 转移 转移  电子 电子 |
| B.湿法制备中,次氯酸钠的氧化性大于高铁酸钠 |
| C.在净水能力上,Na2FeO4氧化能力不如NaClO |
| D.高铁酸钠做水处理剂的优点之一是比较环保 |
您最近一年使用:0次
名校
3 . 已知:2Fe+3Br2=2FeBr3,2Fe3++2I-=2Fe2++I2,3Fe2++NO +4H+=3Fe3++NO↑+2H2O,现将Fe(NO3)2溶液分别滴入到以下溶液中:①H2SO4;②HNO3;③溴水;④碘水。其中能使Fe2+转变成Fe3+的是
+4H+=3Fe3++NO↑+2H2O,现将Fe(NO3)2溶液分别滴入到以下溶液中:①H2SO4;②HNO3;③溴水;④碘水。其中能使Fe2+转变成Fe3+的是
 +4H+=3Fe3++NO↑+2H2O,现将Fe(NO3)2溶液分别滴入到以下溶液中:①H2SO4;②HNO3;③溴水;④碘水。其中能使Fe2+转变成Fe3+的是
+4H+=3Fe3++NO↑+2H2O,现将Fe(NO3)2溶液分别滴入到以下溶液中:①H2SO4;②HNO3;③溴水;④碘水。其中能使Fe2+转变成Fe3+的是| A.只有②③ | B.①②③ | C.②③④ | D.全部 |
您最近一年使用:0次
名校
解题方法
4 . 已知有如下反应:
①2Fe3++2I-=2Fe2++I2
②2Fe2++Cl2=2Fe3++2Cl-
③
(1)判断上述三个反应中,氧化性最强的分子或离子是___________ ;
(2)若某溶液中有Cl-和I-共存时,为氧化I-而使Cl-不被氧化,应选用上述反应中的___________ 离子作为氧化剂。
①2Fe3++2I-=2Fe2++I2
②2Fe2++Cl2=2Fe3++2Cl-
③

(1)判断上述三个反应中,氧化性最强的分子或离子是
(2)若某溶液中有Cl-和I-共存时,为氧化I-而使Cl-不被氧化,应选用上述反应中的
您最近一年使用:0次
名校
解题方法
5 . a g铁粉与含有H2SO4的CuSO4溶液完全反应后,得到a g铜,则参与反应的CuSO4与H2SO4的物质的量之比为
| A.1∶7 | B.8∶1 | C.7∶8 | D.7∶1 |
您最近一年使用:0次
名校
6 . 下列实验操作对应的现象及结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 把炽热的炭投入到盛有浓硝酸的试管中 | 有红棕色气体产生 | 炭与浓硝酸发生了反应 |
| B | 浓硫酸滴入蔗糖中,产生的气体通入澄清石灰水 | 蔗糖变黑、体积膨胀,澄清石灰水变浑浊 | 浓硫酸具有脱水性和强氧化性 |
| C | 过量铁粉加入稀硝酸中,充分反应后,滴加KSCN溶液 | 有无色气泡产生,溶液呈血红色 | 稀硝酸能将 氧化成 氧化成 |
| D | 向含有淀粉的 溶液中滴入 溶液中滴入 溶液 溶液 | 溶液变成蓝色 | 氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-20更新
|
177次组卷
|
2卷引用:海南省琼海市嘉积中学2023-2024学年高一下学期4月月考化学试题
7 . 已知KBrO3可发生反应:2KBrO3 + I2 = 2KIO3 + Br2,下列有关溴酸钾的说法不正确的是
| A.氧化剂与还原剂的物质的量之比为1:2 |
| B.该反应说明I2的还原性强于Br2 |
| C.当有1molKBrO3参与反应时转移5 mol电子 |
| D.该反应中物质氧化性强弱顺序为:KBrO3 < KIO3 |
您最近一年使用:0次
8 . 常温下,实验室可用 和浓盐酸反应制取
和浓盐酸反应制取 ,反应原理为
,反应原理为
 ,下列说法正确的是
,下列说法正确的是
 和浓盐酸反应制取
和浓盐酸反应制取 ,反应原理为
,反应原理为
 ,下列说法正确的是
,下列说法正确的是A.该反应中 是氧化剂,发生还原反应 是氧化剂,发生还原反应 |
B.该反应中氧化剂与还原剂的物质的量之比为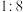 |
C.该反应说明氧化性: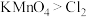 |
D.该反应中每消耗 ,生成 ,生成 |
您最近一年使用:0次
名校
9 . 高温下,钠可以把 中的钛置换出来,反应的化学方程式为
中的钛置换出来,反应的化学方程式为 。下列说法错误的是
。下列说法错误的是
 中的钛置换出来,反应的化学方程式为
中的钛置换出来,反应的化学方程式为 。下列说法错误的是
。下列说法错误的是A.该反应中 表现了还原性 表现了还原性 |
B.该反应中还原性: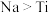 |
C.该反应中有 参与反应时,转移 参与反应时,转移 电子 电子 |
D.依该反应类推,将 投入 投入 稀溶液中,有红色物质生成 稀溶液中,有红色物质生成 |
您最近一年使用:0次
名校
10 . 化学实验中的颜色变化,可将化学抽象之美具体为形象之美。下列叙述正确的是
A.将 通入水中所得溶液为黄绿色,说明 通入水中所得溶液为黄绿色,说明 与水不发生反应 与水不发生反应 |
B.向淀粉 溶液中通入 溶液中通入 ,溶液变成蓝色,说明 ,溶液变成蓝色,说明 的氧化性强于 的氧化性强于 |
C.向待测液中滴加 溶液,产生白色沉淀,说明待测液中含有 溶液,产生白色沉淀,说明待测液中含有 |
| D.用洁净的铂丝蘸取某溶液进行焰色试验,火焰呈黄色,说明该溶液一定为钠盐溶液 |
您最近一年使用:0次

 溶液中通入
溶液中通入 气体
气体
 的
的

