1 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。

已知:①饱和食盐水可以除去氯气中混有的氯化氢气体。
②碘的 溶液显紫红色。
溶液显紫红色。
回答下列问题:
(1)写出圆底烧瓶中发生反应的离子方程式:___________ ,e装置的作用为___________ 。
(2)b中盛放的试剂为___________ 。
(3)取少量 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变;2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变;2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫红色。可知该条件下
层显紫红色。可知该条件下 的氧化能力
的氧化能力___________ (填“大于”或“小于”)NaClO。
(4)一定条件下,在一定量的NaOH溶液中通入一定量的氯气,二者恰好完全反应。生成物中除了含有氯离子外,还含有ClO、 两种离子,
两种离子, 、
、 两种离子的物质的量(n)与反应时间(t)的关系如图1所示。则该反应的离子方程式为
两种离子的物质的量(n)与反应时间(t)的关系如图1所示。则该反应的离子方程式为___________ 。

(5)某同学设计实验探究“84”消毒液的漂白性(已知该消毒液中存在反应: )。
)。
I.在2mL“84”消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL“84”消毒液中加入2mL盐酸后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得“84”消毒液ORP值随时间的变化关系如图2所示。
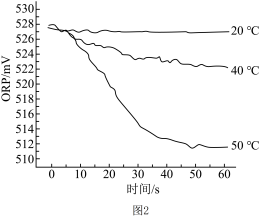
已知:ORP可以表示水溶液中物质的氧化性或还原性强弱。本实验中,ORP值越大,氧化性越强。
①实验I、Ⅱ现象不同的原因是___________ 。
②实验Ⅲ中,随温度的变化ORP值不同的原因可能是___________ 。
③针对不同物品的消毒,需将“84”消毒液稀释到不同的浓度。已知某品牌“84”消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释成8%的溶液,则需加水的质量为___________ g。
 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
已知:①饱和食盐水可以除去氯气中混有的氯化氢气体。
②碘的
 溶液显紫红色。
溶液显紫红色。回答下列问题:
(1)写出圆底烧瓶中发生反应的离子方程式:
(2)b中盛放的试剂为
(3)取少量
 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变;2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变;2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫红色。可知该条件下
层显紫红色。可知该条件下 的氧化能力
的氧化能力(4)一定条件下,在一定量的NaOH溶液中通入一定量的氯气,二者恰好完全反应。生成物中除了含有氯离子外,还含有ClO、
 两种离子,
两种离子, 、
、 两种离子的物质的量(n)与反应时间(t)的关系如图1所示。则该反应的离子方程式为
两种离子的物质的量(n)与反应时间(t)的关系如图1所示。则该反应的离子方程式为
(5)某同学设计实验探究“84”消毒液的漂白性(已知该消毒液中存在反应:
 )。
)。I.在2mL“84”消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL“84”消毒液中加入2mL盐酸后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得“84”消毒液ORP值随时间的变化关系如图2所示。

已知:ORP可以表示水溶液中物质的氧化性或还原性强弱。本实验中,ORP值越大,氧化性越强。
①实验I、Ⅱ现象不同的原因是
②实验Ⅲ中,随温度的变化ORP值不同的原因可能是
③针对不同物品的消毒,需将“84”消毒液稀释到不同的浓度。已知某品牌“84”消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释成8%的溶液,则需加水的质量为
您最近一年使用:0次
解题方法
2 . 某校化学学习小组分别设计了一组实验来探究元素周期律。第一小组根据元素非金属性与其对应最高价含氧酸之间的关系,设计了如图所示装置来完成元素非金属性强弱比较的实验探究。
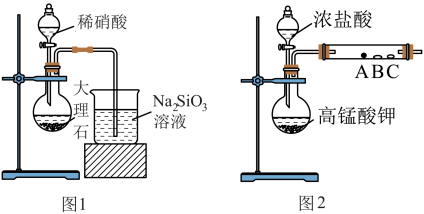
已知:I.稀硝酸具有挥发性。
Ⅱ. 是难溶于水的胶状沉淀。
是难溶于水的胶状沉淀。
Ⅲ.常温下浓盐酸能与高锰酸钾反应生成氯气。
回答下列问题:
(1)第一小组为比较C、N、Si的非金属性强弱,用图1装置进行实验。
①烧杯中的现象为___________ ,其中 与
与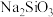 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为___________ 。
②根据实验现象,第一小组得出的结论是:元素的非金属性由强到弱的顺序为___________ 。但其中存在的问题是___________ 。
(2)第二小组设计了图2装置来验证卤素单质的氧化性强弱和潮湿的氯气具有漂白性, A、B、C三处分别是蘸有溴化钠溶液的棉花、湿润的淀粉-碘化钾试纸、湿润的红色纸条。
①写出A处发生反应的离子方程式:___________ 。
②第二小组通过实验___________ (“能”或“不能”)得出实验结论:氧化性: ;原因是
;原因是___________ 。

已知:I.稀硝酸具有挥发性。
Ⅱ.
 是难溶于水的胶状沉淀。
是难溶于水的胶状沉淀。Ⅲ.常温下浓盐酸能与高锰酸钾反应生成氯气。
回答下列问题:
(1)第一小组为比较C、N、Si的非金属性强弱,用图1装置进行实验。
①烧杯中的现象为
 与
与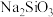 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为②根据实验现象,第一小组得出的结论是:元素的非金属性由强到弱的顺序为
(2)第二小组设计了图2装置来验证卤素单质的氧化性强弱和潮湿的氯气具有漂白性, A、B、C三处分别是蘸有溴化钠溶液的棉花、湿润的淀粉-碘化钾试纸、湿润的红色纸条。
①写出A处发生反应的离子方程式:
②第二小组通过实验
 ;原因是
;原因是
您最近一年使用:0次
3 . 根据下列实验目的进行的实验操作和观察到的现象及得出的结论均正确的是
| 选项 | 实验目的 | 实验操作 | 现象 | 结论 |
| A | 检验溶液中是否含有 | 向溶液中滴加氯水后,再滴入KSCN溶液 | 溶液变红色 | 原溶液中含有 |
| B | 比较 和 和 氧化性强弱 氧化性强弱 | 向溶液中滴加淀粉碘化钾溶液 | 溶液变蓝色 | 氧化性: |
| C | 比较金属镁和铝的活泼性强弱 | 分别向两只盛有等体积等浓度的NaOH溶液的烧杯中加入打磨过的同样大小的镁片和铝片 | 镁片上产生的气泡比铝片快 | 活泼性:Mg>Al |
| D | 检验未知溶液中是否含有 | 用洁净的铂丝蘸取溶液进行焰色试验 | 观察到火焰呈黄色 | 原溶液中无 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 为了防止钢铁零件生锈,常采用化学处理使钢铁零件表面生成 ,致密保护层—“发蓝”。化学处理过程中涉及到的反应为
,致密保护层—“发蓝”。化学处理过程中涉及到的反应为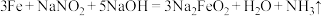 ,下列叙述错误的是
,下列叙述错误的是
 ,致密保护层—“发蓝”。化学处理过程中涉及到的反应为
,致密保护层—“发蓝”。化学处理过程中涉及到的反应为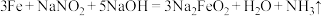 ,下列叙述错误的是
,下列叙述错误的是| A.铁做还原剂,被氧化 | B. 中N元素的化合价为+3价 中N元素的化合价为+3价 |
C.氧化性: | D.反应中每转移3mol电子,生成11.2L |
您最近一年使用:0次
2024-02-22更新
|
130次组卷
|
2卷引用:山西省长治市上党好教育联盟2023-2024学年高一上学期1月期末化学试题
5 . 在一定条件下,氯酸钾和碘按下式发生反应:2KClO3+I2=2KIO3+Cl2,由此推断下列相应的结论不正确的是
| A.氧化性I2>Cl2 | B.该反应中Cl2是还原产物 |
| C.KClO3中Cl元素的化合价为+5 | D.KClO3是氧化剂 |
您最近一年使用:0次
6 . 废水脱氮工艺中有一种方法是在废水中加入NaClO使 完全氧化为
完全氧化为 ,该反应可表示为
,该反应可表示为
 。下列说法正确的是
。下列说法正确的是
 完全氧化为
完全氧化为 ,该反应可表示为
,该反应可表示为
 。下列说法正确的是
。下列说法正确的是A.还原性: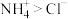 | B. 发生氧化反应 发生氧化反应 |
C. 的摩尔质量是28 的摩尔质量是28 | D.反应中每生成28g  ,转移3mol电子 ,转移3mol电子 |
您最近一年使用:0次
7 . 已知:①
②
③
下列说法正确的是

②

③

下列说法正确的是
A.氧化性: |
B.常温下, 溶液与 溶液与 溶液混合能发生反应生成 溶液混合能发生反应生成 |
C.反应①中, 体现了氧化性和酸性 体现了氧化性和酸性 |
D.反应③中电子的转移可表示为 (少量) (少量) |
您最近一年使用:0次
8 . 过氧化氢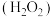 水溶液俗称双氧水,常用于医用伤口消毒、环境消毒和食品消毒。
水溶液俗称双氧水,常用于医用伤口消毒、环境消毒和食品消毒。 的高锰酸钾溶液常用于伤口的杀菌和鱼缸的消毒。二者混合使用时效果会大打折扣,因为混合时会发生反应:
的高锰酸钾溶液常用于伤口的杀菌和鱼缸的消毒。二者混合使用时效果会大打折扣,因为混合时会发生反应: 。下列说法正确的是
。下列说法正确的是
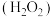 水溶液俗称双氧水,常用于医用伤口消毒、环境消毒和食品消毒。
水溶液俗称双氧水,常用于医用伤口消毒、环境消毒和食品消毒。 的高锰酸钾溶液常用于伤口的杀菌和鱼缸的消毒。二者混合使用时效果会大打折扣,因为混合时会发生反应:
的高锰酸钾溶液常用于伤口的杀菌和鱼缸的消毒。二者混合使用时效果会大打折扣,因为混合时会发生反应: 。下列说法正确的是
。下列说法正确的是A.氧化性: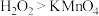 | B.还原剂和还原产物分别为 和 和 |
C. 的高锰酸钾溶液属于电解质 的高锰酸钾溶液属于电解质 | D. |
您最近一年使用:0次
名校
9 . 工业上SO2尾气和Cr2O 可通过Fe3+循环处理吸收,发生如下两个化学反应:SO2+2Fe3++2H2O=SO
可通过Fe3+循环处理吸收,发生如下两个化学反应:SO2+2Fe3++2H2O=SO +2Fe2++4H+,Cr2O
+2Fe2++4H+,Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O,有关说法正确的是
+6Fe2++14H+=2Cr3++6Fe3++7H2O,有关说法正确的是
 可通过Fe3+循环处理吸收,发生如下两个化学反应:SO2+2Fe3++2H2O=SO
可通过Fe3+循环处理吸收,发生如下两个化学反应:SO2+2Fe3++2H2O=SO +2Fe2++4H+,Cr2O
+2Fe2++4H+,Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O,有关说法正确的是
+6Fe2++14H+=2Cr3++6Fe3++7H2O,有关说法正确的是| A.两个反应中Fe2(SO4)3均作还原剂 |
B.氧化性Cr2O >SO2>Fe3+ >SO2>Fe3+ |
C.Cr2O 能将SO2氧化成SO 能将SO2氧化成SO |
D.第二个反应中1个Cr2O 参与反应,转移3个电子 参与反应,转移3个电子 |
您最近一年使用:0次
解题方法
10 . 高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为3ClO-+2Fe3++xOH-=2FeO +3Cl-+yH2O。
+3Cl-+yH2O。
(1)上述反应中的x =___________ ,y=___________ 。
(2)上述反应中氧化剂为___________ ;还原产物为___________ 。
(3)由上述反应可知,氧化性强弱:ClO-___________ (填“>”或“<”,下同)FeO ;还原性强弱:Cl-
;还原性强弱:Cl-___________ Fe3+。
(4)请用单线桥法表示该反应中电子的转移情况:___________ 。
(5)已知:Na2FeO4在处理饮用水的过程中铁元素会被转化为Fe3+,进而Fe3+在水中产生Fe(OH)3胶体,Fe(OH)3胶体具有吸附性。
①Na2FeO4在处理饮用水的过程中___________ (填“发生了”或“未发生”)氧化还原反应。
②Fe(OH)3胶体呈___________ 色,写出区分胶体与溶液的操作及现象:___________ 。
③已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的方法是___________ ,装置是下列中的___________ (填序号)。
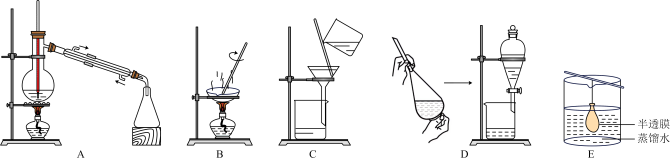
④现有10 mL明胶的水溶液与5mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜
能够透过半透膜___________ 。
 +3Cl-+yH2O。
+3Cl-+yH2O。(1)上述反应中的x =
(2)上述反应中氧化剂为
(3)由上述反应可知,氧化性强弱:ClO-
 ;还原性强弱:Cl-
;还原性强弱:Cl-(4)请用单线桥法表示该反应中电子的转移情况:
(5)已知:Na2FeO4在处理饮用水的过程中铁元素会被转化为Fe3+,进而Fe3+在水中产生Fe(OH)3胶体,Fe(OH)3胶体具有吸附性。
①Na2FeO4在处理饮用水的过程中
②Fe(OH)3胶体呈
③已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的方法是

④现有10 mL明胶的水溶液与5mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
 能够透过半透膜
能够透过半透膜
您最近一年使用:0次



