名校
解题方法
1 . 下列离子方程式书写正确的是
| A.澄清的石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O |
| B.钠与水反应:Na+H2O=Na++OH-+H2↑ |
C.铜粉与浓硝酸反应:Cu+2H++NO =Cu2++NO2↑+H2O =Cu2++NO2↑+H2O |
D.氢氧化铝中加入氢氧化钠溶液:Al(OH)3+OH-=AlO +2H2O +2H2O |
您最近半年使用:0次
解题方法
2 . 下列有关钠、铁、铝性质的说法中错误的是
| A.均能与氧气反应 |
B.均能与氯气反应,生成物中金属元素化合价数值: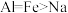 |
| C.均能从溶液中置换出铜 |
| D.均能与盐酸反应置换出氢气 |
您最近半年使用:0次
3 . 下列说法正确的是
| A.钠在空气中燃烧时,生成氧化钠 | B.铝是地壳里含量最多的金属元素 |
| C.钢是我国使用最早的合金, | D.在自然界中只有游离态的铁 |
您最近半年使用:0次
解题方法
4 . 钠与水反应的现象不能说明其性质的有
| A.钠融化成小球,说明钠的的熔点小 |
| B.发出“哧哧”的响声说明反应生成气体 |
| C.加酚酞的溶液变成红色,说明反应生成碱 |
| D.钠浮在水面上,说明反应放热 |
您最近半年使用:0次
解题方法
5 . 在一定条件下,不能由两种单质直接化合而生成的化合物是
| A.SO3 | B.Na2O2 | C.FeCl3 | D.Na2O |
您最近半年使用:0次
解题方法
6 . 如图所示, 是固体金属单质,燃烧时火焰呈黄色,且生成物
是固体金属单质,燃烧时火焰呈黄色,且生成物 为淡黄色固体.回答下列问题:
为淡黄色固体.回答下列问题:
B____________ ,C____________ ,D____________ .
(2)写出下列转化反应的化学方程式或离子方程式:
①B→D:____________ (写化学方程式);
②A→C:____________ (写离子方程式):
③B→C:____________ (写离子方程式).
 是固体金属单质,燃烧时火焰呈黄色,且生成物
是固体金属单质,燃烧时火焰呈黄色,且生成物 为淡黄色固体.回答下列问题:
为淡黄色固体.回答下列问题: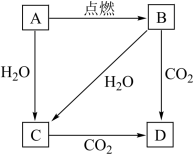
B
(2)写出下列转化反应的化学方程式或离子方程式:
①B→D:
②A→C:
③B→C:
您最近半年使用:0次
7 . 下列有关物质性质与用途的说法不正确 的是
| A.金属钠具有强还原性,可与TiCl4溶液反应制取金属Ti |
| B.硬铝密度小、强度高,具有较强的抗腐蚀能力,常用于制造飞机外壳 |
| C.常温下铁能被浓硝酸钝化,可用铁制容器贮运浓硝酸 |
| D.“84”消毒液具有强氧化性,能用于杀菌消毒 |
您最近半年使用:0次
名校
8 . X、Y、Z、M、R、Q是短周期主族元素,部分信息如表所示:
(1)Z的单质与水反应的化学方程式为___________ 。
(2)Y与R相比,非金属性较强的是___________ (用元素符号表示),下列事实能证明这一结论的是___________ (填标号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:
c.最高价氧化物对应的水化物的酸性: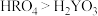
(3)根据表中数据推测Y的原子半径的范围:___________ 
___________  。
。
(4)甲、乙是上述部分元素的最高价氧化物对应的水化物,且甲+乙 丙+水,则丙的化学式为
丙+水,则丙的化学式为___________ (写出一种即可)。
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色试验呈黄色 |
(2)Y与R相比,非金属性较强的是
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:

c.最高价氧化物对应的水化物的酸性:
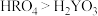
(3)根据表中数据推测Y的原子半径的范围:

 。
。(4)甲、乙是上述部分元素的最高价氧化物对应的水化物,且甲+乙
 丙+水,则丙的化学式为
丙+水,则丙的化学式为
您最近半年使用:0次
9 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.将0.2 mol  水解制成胶体,所得胶体粒子数为 水解制成胶体,所得胶体粒子数为 |
B.2.3 g Na与氧气完全反应,反应中转移的电子数介于 到 到 之间 之间 |
C.标准状况下, 完全燃烧后生成的 完全燃烧后生成的 分子个数约为 分子个数约为 |
D.8.0 g  和CuO的混合物中含有铜原子数为 和CuO的混合物中含有铜原子数为 |
您最近半年使用:0次
10 . 下列化学方程式与所给事实不相符的是
A.足量的铁在少量氯气中燃烧: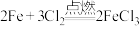 |
B.次氯酸见光分解: |
C.钠放置在空气中表面变暗: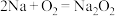 |
D.钠投入 溶液中: 溶液中: |
您最近半年使用:0次



