1 . 溴蒸气与氨气相遇产生“白烟”,化学方程式为 。用
。用 表示阿伏加德罗常数的值。下列说法错误的是
表示阿伏加德罗常数的值。下列说法错误的是
 。用
。用 表示阿伏加德罗常数的值。下列说法错误的是
表示阿伏加德罗常数的值。下列说法错误的是A.生成14gN2时,反应中还原剂的分子数目为 |
B.标准状况下,11.2LBr2参与反应时转移的电子数为 |
C.1L 的NH4Br溶液中含有 的NH4Br溶液中含有 的数目小于 的数目小于 |
D.当生成29.4gNH4Br时,消耗NH3分子的数目为 |
您最近半年使用:0次
名校
2 .  是一种半导体材料,一种制备方法是
是一种半导体材料,一种制备方法是 。设
。设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 是一种半导体材料,一种制备方法是
是一种半导体材料,一种制备方法是 。设
。设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.标准状况下,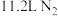 含 含 键数目为 键数目为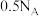 |
B.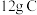 (金刚石)含非极性键数目为 (金刚石)含非极性键数目为 |
C.每生成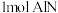 时转移电子数目为 时转移电子数目为 |
D.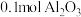 溶于足量盐酸,溶液中含 溶于足量盐酸,溶液中含 数目为 数目为 |
您最近半年使用:0次
今日更新
|
149次组卷
|
2卷引用:吉林省白山市2023-2024学年高三第二次模拟考试化学试题
3 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温常压下,18g  中含有的电子数为9 中含有的电子数为9 |
B.将2.24L  通入足量水中,得到的 通入足量水中,得到的 分子数为0.1 分子数为0.1 |
C.1mol  与足量 与足量 在一定条件下反应,生成的 在一定条件下反应,生成的 分子数为NA 分子数为NA |
D.以稀硫酸为电解液的锌铜原电池中,每转移0.2 个电子,负极质量减少6.4g 个电子,负极质量减少6.4g |
您最近半年使用:0次
名校
4 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.50mL、18.4mol/L浓硫酸与足量铜加热反应生成 分子的数目为 分子的数目为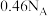 |
B.12.8gCu和0.2molS充分反应转移电子数为 |
C.常温下,将2.7g铝片投入足量的浓硝酸中,铝失去的电子数为 |
D.在标准状况下,22.4L氮气与足量的氢气反应,能生成 分子数为 分子数为 |
您最近半年使用:0次
5 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.将0.2 mol  水解制成胶体,所得胶体粒子数为 水解制成胶体,所得胶体粒子数为 |
B.2.3 g Na与氧气完全反应,反应中转移的电子数介于 到 到 之间 之间 |
C.标准状况下, 完全燃烧后生成的 完全燃烧后生成的 分子个数约为 分子个数约为 |
D.8.0 g  和CuO的混合物中含有铜原子数为 和CuO的混合物中含有铜原子数为 |
您最近半年使用:0次
6 . 工业上用S8(分子结构: )CH4为原料制备CS2,发生反应:
)CH4为原料制备CS2,发生反应: ,
, 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
A.1molH2S中含有的孤电子对数为 |
B.生成17gH2S,转移的电子数为 |
C.消耗1molS8,断裂的S-S键数目为 |
D.22.4LCH4中含有的电子数为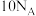 |
您最近半年使用:0次
名校
7 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1mol 与足量氧气反应可以产生 与足量氧气反应可以产生 个 个 分子 分子 |
B.常温下,将2.7g铝片投入足量的浓硫酸中,铝失去的电子数为 |
C.120g 和 和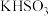 的固体混合物中含有的阳离子数为 的固体混合物中含有的阳离子数为 |
D.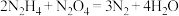 ,当生成标况下6.72L ,当生成标况下6.72L 时转移电子数为 时转移电子数为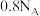 |
您最近半年使用:0次
8 . NA为阿伏加德罗常数的值,下列说法不正确的是
| A.1molHCN中含π键的数目为NA |
| B.6.5gZn与一定量浓硫酸反应完全溶解,转移的电子数为0.2NA |
C.将1molNH4CI溶于稀氨水中使溶液呈中性,溶液中 数目为NA 数目为NA |
| D.23gNa与O2充分反应生成Na2O和Na2O2的混合物,消耗O2的分子数在0.25NA和0.5NA之间 |
您最近半年使用:0次
9 . 硫化钠广泛应用于冶金、染料、皮革、电镀等工业。硫化钠的一种制备方法是
 。设
。设 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是

 。设
。设 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是A.常温常压下,11.2L  中含有的分子数目为0.5 中含有的分子数目为0.5 |
B.0.2 的 的 溶液中含有 溶液中含有 的数目为0.4 的数目为0.4 |
C.常温常压下,1.2g C中含有的质子数目为1.2 |
D.该反应每生成1mol  ,转移电子数目为8 ,转移电子数目为8 |
您最近半年使用:0次
解题方法
10 . 设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.常温下,18gD2O中含有中子的数目为9NA |
| B.32g O2和O3混合物中,含有的氧原子数目为NA |
| C.7.8gNa2O2与足量水反应转移电子数为0.2NA |
| D.1mol/L的MgCl2溶液中,含有Cl-的数目为2NA |
您最近半年使用:0次



