1 . NA为阿伏加德罗常数的值,下列说法正确的是
| A.0.2 mol/LAlCl3溶液中Cl-物质的量为0.6 mol |
| B.25℃ 101KPa,22.4L NH3中电子的数目为10NA |
| C.标准状况下,44.8LNO和22.4LO2反应后的分子数小于2NA |
| D.常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
您最近半年使用:0次
2 . 工业上,接触法制备硫酸的原理如下:
① ;②
;②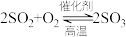 ;③
;③ 的浓硫酸吸收。
的浓硫酸吸收。
设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
①
 ;②
;②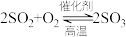 ;③
;③ 的浓硫酸吸收。
的浓硫酸吸收。设
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.①中每生成 时转移电子数为 时转移电子数为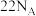 |
B.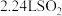 含原子数为 含原子数为 |
C.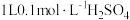 溶液含氧原子总数为 溶液含氧原子总数为 |
D.②中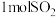 和 和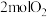 反应生成的 反应生成的 分子数为 分子数为 |
您最近半年使用:0次
3 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温常压下,18g  中含有的电子数为9 中含有的电子数为9 |
B.将2.24L  通入足量水中,得到的 通入足量水中,得到的 分子数为0.1 分子数为0.1 |
C.1mol  与足量 与足量 在一定条件下反应,生成的 在一定条件下反应,生成的 分子数为NA 分子数为NA |
D.以稀硫酸为电解液的锌铜原电池中,每转移0.2 个电子,负极质量减少6.4g 个电子,负极质量减少6.4g |
您最近半年使用:0次
4 . 下列物质中,所含分子数最多的是
| A.0.8mol氦气 | B.标况下,4.48 L二氧化硫 |
| C.3.01×1023个甲烷分子 | D.16 g臭氧 |
您最近半年使用:0次
5 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.28g单晶硅中所含的Si-Si键的数目为4NA |
B.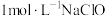 溶液中含有的 溶液中含有的 数目为NA 数目为NA |
| C.标准状况下,过氧化钠与水反应生成2.24L氧气,转移的电子数为0.2NA |
| D.标准状况下,22.4LHF中含有的氟原子数目为NA |
您最近半年使用:0次
6 . 利用“化学计量在实验中的应用”的相关知识进行填空(设NA表示阿伏加德罗常数的值)。
(1)标准状况下,0.2mol氨气的体积是___________ ,其中含有的NH3分子数是___________ (用NA来表示),含氢原子数是___________ (用NA来表示)。
(2)H2SO4的摩尔质量是___________ ,49g的H2SO4中含有___________ mol氧原子。
(3)将0.5mol Na2CO3溶解在水中,配成500mL溶液,所得溶液中溶质的物质的量浓度是___________ 。
(1)标准状况下,0.2mol氨气的体积是
(2)H2SO4的摩尔质量是
(3)将0.5mol Na2CO3溶解在水中,配成500mL溶液,所得溶液中溶质的物质的量浓度是
您最近半年使用:0次
7 . 已知NA为阿伏加德罗常数的数值,下列有关说法中正确的是
| A.标准状况下,11.2LCHCl3中含有的C-Cl的数目为1.5NA |
| B.向FeI2溶液中通入适量Cl2,当有1molFe2+被氧化时,共转移电子的数目为NA |
| C.常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA |
| D.室温下,pH为13的NaOH和Ba(OH)2混合溶液中含OH-个数为0.1NA |
您最近半年使用:0次
8 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 中含有的中子数为 中含有的中子数为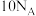 |
B.常温下, 甲烷中含有的极性键数目为 甲烷中含有的极性键数目为 |
C.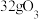 含有的原子总数为 含有的原子总数为 |
D. 和 和 分别与足量的 分别与足量的 反应,转移的电子数均为 反应,转移的电子数均为 |
您最近半年使用:0次
9 . 用 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A. 氮气中所含的氮原子数是 氮气中所含的氮原子数是 |
B.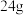 镁和足量的盐酸反应,电子转移的数目是 镁和足量的盐酸反应,电子转移的数目是 |
C. 氨水溶液中含 氨水溶液中含 的数目是 的数目是 |
D.标准状况下, 正己烷中所含的分子数是 正己烷中所含的分子数是 |
您最近半年使用:0次
10 . 硫化钠广泛应用于冶金、染料、皮革、电镀等工业。硫化钠的一种制备方法是
 。设
。设 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是

 。设
。设 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是A.常温常压下,11.2L  中含有的分子数目为0.5 中含有的分子数目为0.5 |
B.0.2 的 的 溶液中含有 溶液中含有 的数目为0.4 的数目为0.4 |
C.常温常压下,1.2g C中含有的质子数目为1.2 |
D.该反应每生成1mol  ,转移电子数目为8 ,转移电子数目为8 |
您最近半年使用:0次



