1 . 下列关于晶体冰、干冰、金刚石的说法正确的是
| A.熔点:金刚石>干冰>冰 |
| B.上述三种晶体的晶体类型相同 |
| C.金刚石熔化时,化学键一定会断裂 |
| D.冰的沸点高于干冰,是因为水分子的键能大于干冰分子的键能 |
您最近半年使用:0次
2 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.28g单晶硅中所含的Si-Si键的数目为4NA |
B.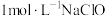 溶液中含有的 溶液中含有的 数目为NA 数目为NA |
| C.标准状况下,过氧化钠与水反应生成2.24L氧气,转移的电子数为0.2NA |
| D.标准状况下,22.4LHF中含有的氟原子数目为NA |
您最近半年使用:0次
3 . 下列叙述正确的是
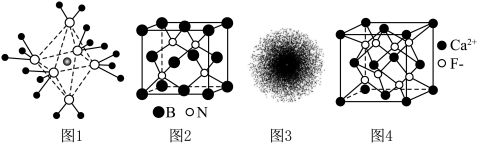
| A.图1为[Cu(NH3)4(H2O)2]2+结构示意图,该离子内存在极性键、配位键、离子键 |
| B.图2为BN晶体的晶胞示意图,由N和B原子围成的最小六元环为平面结构 |
| C.图3为H原子的电子云图,一个黑点表示一个电子 |
| D.图4为CaF2晶体的晶胞示意图,与Ca2+周围紧邻且距离相等的F-共有8个 |
您最近半年使用:0次
4 . MgO、BeO、CsCl、金刚石四种晶体的结构模型如图所示,下列说法正确的是

| A.MgO晶体中,每个晶胞含有4个MgO分子,CsCl晶胞含有1个CsCl分子 |
| B.BeO晶体中,每个Be2+周围与其最近且等距的O2-有4个 |
C.金刚石晶体中,碳原子之间的最短距离为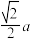 |
| D.MgO晶体熔点比BeO晶体的高 |
您最近半年使用:0次
5 . 火星岩的主要成分有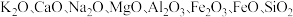 和
和 。
。
(1)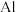 在周期表中的位置
在周期表中的位置_______ ;基态铁原子的价层电子排布式为_______ 。
(2)基态 原子的核外有
原子的核外有_______ 种能量不同的电子;  晶体中含有
晶体中含有_______ 个  键。
键。
(3)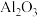 溶于
溶于  溶液的离子方程为
溶液的离子方程为_______ 。
(4)实验室用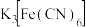 检验
检验  中
中 键、
键、 键数目之比为
键数目之比为_______ 。
(5)晶体熔点:
_______ (填“ ”或“
”或“ ”)
”)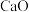 。
。
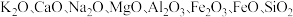 和
和 。
。(1)
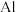 在周期表中的位置
在周期表中的位置(2)基态
 原子的核外有
原子的核外有 晶体中含有
晶体中含有 键。
键。(3)
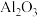 溶于
溶于  溶液的离子方程为
溶液的离子方程为(4)实验室用
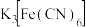 检验
检验  中
中 键、
键、 键数目之比为
键数目之比为(5)晶体熔点:

 ”或“
”或“ ”)
”)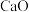 。
。
您最近半年使用:0次
6 .  代表阿伏加德罗常数的数值。下列说法中正确的是
代表阿伏加德罗常数的数值。下列说法中正确的是
 代表阿伏加德罗常数的数值。下列说法中正确的是
代表阿伏加德罗常数的数值。下列说法中正确的是A.0.1mol碳酸钠和碳酸氢钠的混合物含有的氧原子数为 |
B.标准状况下,22.4L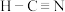 中 中 键数为 键数为 、 、 键数为 键数为 |
C.100mL1mol⋅L-1醋酸溶液中含有的氢离子数为 |
D.60g二氧化硅晶体中含有Si—O键数为 |
您最近半年使用:0次
7 . NA为阿伏加德罗常数的值。下列叙述正确的是
| A.0.5mol异丁烷分子中共价键的数目为6.5NA |
B.1.7g 中含有氧原子数为0.2NA 中含有氧原子数为0.2NA |
C.1mol晶体Si含Si-Si键的数目约为 |
D.标准状况下,0.5NA 分子所占的体积约为11.2L 分子所占的体积约为11.2L |
您最近半年使用:0次
8 . 以 表示阿伏加德罗常数的值,下列说法不正确的是
表示阿伏加德罗常数的值,下列说法不正确的是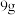 冰(图1)中含氢键数目为
冰(图1)中含氢键数目为
② 晶体硅(图2)中含有
晶体硅(图2)中含有 键数目为
键数目为
③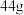 干冰(图3)中含共用电子对
干冰(图3)中含共用电子对
④石墨烯(图4)是碳原子单层片状新材料, 石墨烯中含
石墨烯中含 键数目为
键数目为
 表示阿伏加德罗常数的值,下列说法不正确的是
表示阿伏加德罗常数的值,下列说法不正确的是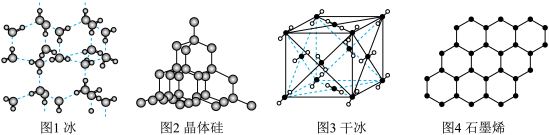
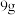 冰(图1)中含氢键数目为
冰(图1)中含氢键数目为
②
 晶体硅(图2)中含有
晶体硅(图2)中含有 键数目为
键数目为
③
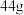 干冰(图3)中含共用电子对
干冰(图3)中含共用电子对
④石墨烯(图4)是碳原子单层片状新材料,
 石墨烯中含
石墨烯中含 键数目为
键数目为
| A.①② | B.①③ | C.②③ | D.③④ |
您最近半年使用:0次
9 . 我国某有机所研究团队合成一种盐,其阴离子结构如图所示。短周期主族元素X、Y、Z、R的原子序数依次增大,X、Y、Z的原子序数之和为23,下列有关叙述不正确的是
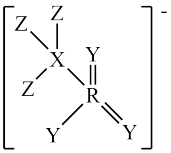
| A.电负性:Z>Y>R | B.简单氢化物的稳定性:Z>Y>X |
C.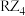 的键角和 的键角和 的键角相等 的键角相等 | D.X的单质可能是共价晶体 |
您最近半年使用:0次
解题方法
10 . 工业上用焦炭还原石英砂制得粗硅,下列说法不正确的是( 为阿伏伽德罗常数)
为阿伏伽德罗常数)
 为阿伏伽德罗常数)
为阿伏伽德罗常数)A.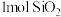 中含有 中含有 键数目为 键数目为 | B.消耗 焦炭转移 焦炭转移 电子 电子 |
C. (氧化产物): (氧化产物): 还原产物)=2:1 还原产物)=2:1 | D.可用氯化氢气体将硅与杂质分离 |
您最近半年使用:0次
2024-04-17更新
|
127次组卷
|
2卷引用:浙江省金华市十校2023-2024学年高三下学期4月模拟考试化学试题



