名校
1 . 请回答下列问题:
(1)由磷原子核形成的三种微粒:① 、②
、② 、③
、③ ,半径由大到小的顺序为
,半径由大到小的顺序为_______ (填标号,下同);再失去一个电子所需最低能量由大到小的顺序为_______ 。
(2)比较H-O-H键角大小;H3O+_______ H2O(填“>”、“<”或“=”)。
(3)胍(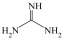 )分子中所有原子共平面,胍中N杂化方式为
)分子中所有原子共平面,胍中N杂化方式为_______ 。
(4)干冰晶体中,每个CO2周围等距离且紧邻的CO2有_______ 个;在冰晶体结构中,每个水分子最多与相邻的_______ 个水分子相连接。同为分子晶体,但干冰中CO2的配位数大于冰中水分子的配位数,其原因是_______ 。
(1)由磷原子核形成的三种微粒:①
 、②
、② 、③
、③ ,半径由大到小的顺序为
,半径由大到小的顺序为(2)比较H-O-H键角大小;H3O+
(3)胍(
 )分子中所有原子共平面,胍中N杂化方式为
)分子中所有原子共平面,胍中N杂化方式为(4)干冰晶体中,每个CO2周围等距离且紧邻的CO2有
您最近半年使用:0次
名校
2 . “燕山雪花大如席,纷纷吹落轩辕台”(李白《北风行》),描写了雪景的壮观。下列说法错误的是
| A.水转化为雪的过程是熵减的过程 |
| B.雪花和竹席的主要成分都属于高分子化合物 |
| C.往积雪上撒盐是为了降低水的凝固点,使雪融化 |
| D.雪花的形状受水分子结构和分子间作用力的影响 |
您最近半年使用:0次
3 . 以 表示阿伏加德罗常数的值,下列说法不正确的是
表示阿伏加德罗常数的值,下列说法不正确的是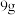 冰(图1)中含氢键数目为
冰(图1)中含氢键数目为
② 晶体硅(图2)中含有
晶体硅(图2)中含有 键数目为
键数目为
③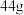 干冰(图3)中含共用电子对
干冰(图3)中含共用电子对
④石墨烯(图4)是碳原子单层片状新材料, 石墨烯中含
石墨烯中含 键数目为
键数目为
 表示阿伏加德罗常数的值,下列说法不正确的是
表示阿伏加德罗常数的值,下列说法不正确的是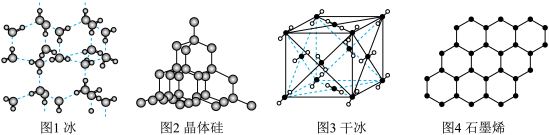
 冰(图1)中含氢键数目为
冰(图1)中含氢键数目为
②
 晶体硅(图2)中含有
晶体硅(图2)中含有 键数目为
键数目为
③
 干冰(图3)中含共用电子对
干冰(图3)中含共用电子对
④石墨烯(图4)是碳原子单层片状新材料,
 石墨烯中含
石墨烯中含 键数目为
键数目为
| A.①② | B.①③ | C.②③ | D.③④ |
您最近半年使用:0次
4 . SiH4的分子结构与CH4类似,对SiH4作出如下推测,其中不正确的是
| A. SiH4晶体是分子晶体 | B. SiH4的热稳定性比CH4弱 |
| C. SiH4是由极性键形成的非极性分子 | D. SiH4的沸点低于CH4 |
您最近半年使用:0次
5 . 将钴酞菁和三氯化铝复合嵌接在碳纳米管上,制得一种高效催化还原二氧化碳的催化剂。回答下列问题:
(1)碳的几种单质如图1所示。___________ 。
②金刚石晶体中C原子数与C-C键数的比为___________ 。
③石墨可以导电的原因是___________ 。
(2)C60的晶胞如图2所示。___________ 。
②1个C60晶胞中含有___________ 个原子。
③世界上第一辆单分子“纳米小车”的四个轮子是C60,小车运行情况如图所示,从a处化学键的特点说明其运动原因:___________ 。___________ 。
②钴酞菁分子中能形成配位键的原因是___________ 。
(4)气态AlCl3通常以二聚体Al2Cl6的形式存在,其空间结构如图4所示。AlF3结构属立方晶系,晶胞如图5所示。___________ 。
②AlF3的熔点为1090℃,远高于AlCl3的熔点192℃,原因是___________ 。
③AlF3晶体距离F-最近的阳离子有___________ 个。
④AlF3的晶胞形状为正方体,边长为anm,该晶体密度为___________ g·cm-3。(列出计算式,阿伏加德罗常数用NA表示,1nm=10-7cm)
(1)碳的几种单质如图1所示。
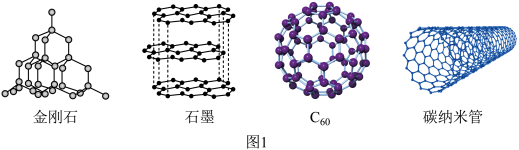
②金刚石晶体中C原子数与C-C键数的比为
③石墨可以导电的原因是
(2)C60的晶胞如图2所示。
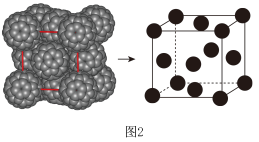
②1个C60晶胞中含有
③世界上第一辆单分子“纳米小车”的四个轮子是C60,小车运行情况如图所示,从a处化学键的特点说明其运动原因:
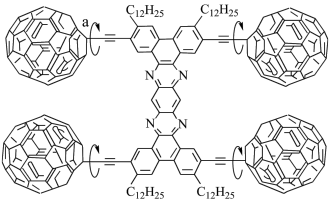

②钴酞菁分子中能形成配位键的原因是
(4)气态AlCl3通常以二聚体Al2Cl6的形式存在,其空间结构如图4所示。AlF3结构属立方晶系,晶胞如图5所示。
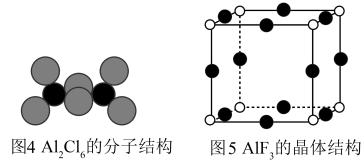
②AlF3的熔点为1090℃,远高于AlCl3的熔点192℃,原因是
③AlF3晶体距离F-最近的阳离子有
④AlF3的晶胞形状为正方体,边长为anm,该晶体密度为
您最近半年使用:0次
6 . 几种晶体的晶胞(或晶体结构)如图所示,下列说法正确的是
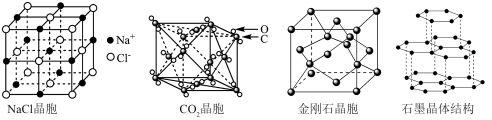
| A.NaCl晶胞中,距离每个Na+最近的Na+为6个 |
| B.CO2晶胞中,CO2分子的排列方式只有1种方向 |
| C.石墨晶体层内是共价键,层间是范德华力,所以石墨是一种混合型晶体 |
D.若金刚石的晶胞边长为a cm,其中两个最近的碳原子之间的距离为 cm cm |
您最近半年使用:0次
7 . 有关晶体的结构如图所示,下列说法中不正确的是
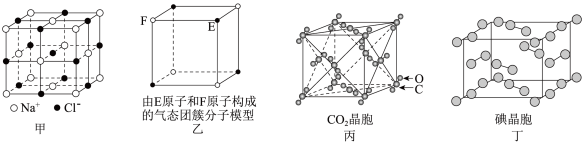
| A.在NaCl晶体(图甲)中,距Na+最近的Cl-有6个 |
B.该气态团簇分子(图乙)E、F两个原子个数比为 |
| C.在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻 |
| D.在碘晶体(图丁)中,只存在范德华力,不存在化学键 |
您最近半年使用:0次
名校
解题方法
8 . 如图为冰晶体的结构模型,大球代表O原子,小球代表H原子,下列有关说法正确的是
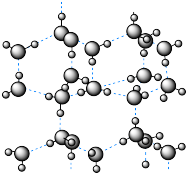
| A.冰晶体中每个水分子与另外四个水分子形成四面体 |
| B.冰晶体具有共价键三维骨架结构,是共价晶体 |
C.水分子间通过 形成冰晶体 形成冰晶体 |
| D.冰晶体融化时,水分子间的空隙增大 |
您最近半年使用:0次
9 . 短周期元素R、X、T、Z在元素周期表中的相对位置如图所示,其中X、T、Z原子核外电子数之和是R原子的7倍。则下列判断正确的是
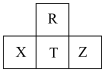

| A.第一电离能:Z<R<T |
| B.X原子核外未成对电子数为1 |
| C.四种元素对应最高价氧化物的晶体类型均不相同 |
D.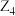 和R的简单氢化物均为正四面体结构且键角都为109°28′ 和R的简单氢化物均为正四面体结构且键角都为109°28′ |
您最近半年使用:0次
10 . 下列对分子结构与性质的描述中,不正确的是


| A.碘易溶于四氯化碳,甲烷难溶于水都可用“相似相溶”规律解释 |
B.某元素气态基态原子的逐级电离能( )分别为578、1817、2745、11575、14830、18376,当它与氯气反应时可能生成的阳离子是 )分别为578、1817、2745、11575、14830、18376,当它与氯气反应时可能生成的阳离子是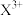 |
C.一个 晶胞中含有8个 晶胞中含有8个 分子 分子 |
D.青蒿素的分子式为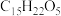 ,结构如图所示,该分子中包含7个手性碳原子 ,结构如图所示,该分子中包含7个手性碳原子 |
您最近半年使用:0次



