1 . 下列陈述I与陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述I | 陈述Ⅱ |
| A |  的氧化性强于 的氧化性强于 |  与 与 在暗处会发生爆炸; 在暗处会发生爆炸; 与 与 加热时会缓慢反应 加热时会缓慢反应 |
| B | 过氧化钠是碱性氧化物 | 过氧化钠能与酸反应 |
| C | 苏打受热易分解 | 苏打常用作食品膨松剂 |
| D | D与T的质子数和核外电子数均相同 | D与T的性质完全相同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 利用 、
、 溶液回收
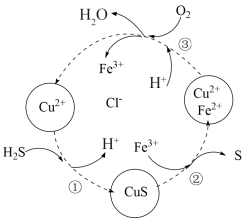
溶液回收 中的S,其转化关系如图所示.下列说法错误的是
中的S,其转化关系如图所示.下列说法错误的是
 、
、 溶液回收
溶液回收 中的S,其转化关系如图所示.下列说法错误的是
中的S,其转化关系如图所示.下列说法错误的是
| A.反应①②③均为氧化还原反应 |
B.氧化性: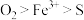 |
C.能循环利用的物质是 和 和 |
D.反应③的离子方程式为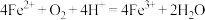 |
您最近一年使用:0次
3 . 钠及其化合物在生活生产中应用广泛,下面是一些它们的具体应用及反应原理。
①碳酸氢钠作食品膨松剂: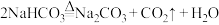
②氢化钠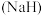 可用作野外生氢剂:
可用作野外生氢剂: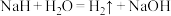
③钠单质组成“可呼吸”的 充电电池:
充电电池: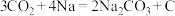
④饱和食盐水作侯氏制碱原料: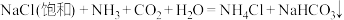
⑤电解饱和食盐水制备氯气和氢氧化钠(氯碱工业):
⑥高铁酸钠 可同时消毒和净水:
可同时消毒和净水: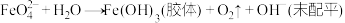
回答下列问题:
(1)以上反应中不属于氧化还原反应的是___________ (填标号)。
(2)钠是一种很活泼的金属,可用石蜡封存,实验室少量 保存于
保存于___________ 中(填字母)。
A.细沙 B.水 C.煤油
(3)野外生氢剂 中氢元素的化合价为
中氢元素的化合价为___________ 价,常用作___________ (填“氧化剂”或“还原剂”)。
(4)“可呼吸” 充电电池消耗
充电电池消耗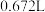 (标准状况)
(标准状况) 气体时,转移电子数为
气体时,转移电子数为_____  。
。
(5)氯碱工业生产中会使用阳离子交换膜,目的之一是将 溶液和
溶液和 分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为
分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为___________ 。
(6)请配平高铁酸钠 (
( 为
为 价)在水中发生反应的离子反应方程式:
价)在水中发生反应的离子反应方程式:___________ 。
并比较氧化性强弱:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
①碳酸氢钠作食品膨松剂:
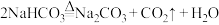
②氢化钠
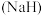 可用作野外生氢剂:
可用作野外生氢剂: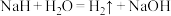
③钠单质组成“可呼吸”的
 充电电池:
充电电池: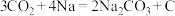
④饱和食盐水作侯氏制碱原料:
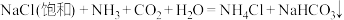
⑤电解饱和食盐水制备氯气和氢氧化钠(氯碱工业):

⑥高铁酸钠
 可同时消毒和净水:
可同时消毒和净水: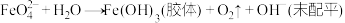
回答下列问题:
(1)以上反应中不属于氧化还原反应的是
(2)钠是一种很活泼的金属,可用石蜡封存,实验室少量
 保存于
保存于A.细沙 B.水 C.煤油
(3)野外生氢剂
 中氢元素的化合价为
中氢元素的化合价为(4)“可呼吸”
 充电电池消耗
充电电池消耗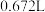 (标准状况)
(标准状况) 气体时,转移电子数为
气体时,转移电子数为 。
。(5)氯碱工业生产中会使用阳离子交换膜,目的之一是将
 溶液和
溶液和 分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为
分隔开,若未分隔开,两者会发生反应,该反应的化学反应方程式为(6)请配平高铁酸钠
 (
( 为
为 价)在水中发生反应的离子反应方程式:
价)在水中发生反应的离子反应方程式:
并比较氧化性强弱:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
名校
解题方法
4 . 某粗铜精炼得到的阳极泥主要成分为 、
、 、
、 ,从中提取
,从中提取 的工艺流程如图:
的工艺流程如图: ;
; 为弱酸。
为弱酸。
下列说法正确的是
 、
、 、
、 ,从中提取
,从中提取 的工艺流程如图:
的工艺流程如图:
 ;
; 为弱酸。
为弱酸。下列说法正确的是
A. 、 、 、 、 氧化性由强到弱的顺序为 氧化性由强到弱的顺序为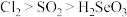 |
B.“氯化”过程中 转化为 转化为 ,反应的离子方程式为 ,反应的离子方程式为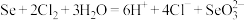 |
C. 转化为 转化为 的原因是 的原因是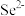 被 被 氧化为 氧化为 ,导致 ,导致 增大 增大 |
D.粗铜精炼时,若以恒定电流强度I安培持续电解t秒,电解效率为 ,当阴极增重m克时,则 ,当阴极增重m克时,则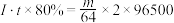 |
您最近一年使用:0次
2024-02-04更新
|
179次组卷
|
3卷引用:山东省日照市校际联合2023-2024学年高三上学期1月期末考试化学试题
解题方法
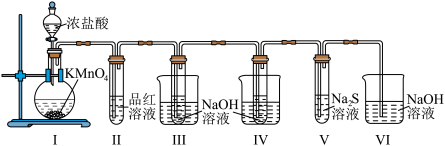
5 . 按如图装置进行实验,将浓盐酸滴入Ⅰ中的圆底烧瓶中(已知: 和
和 溶液在加热条件下会生成
溶液在加热条件下会生成 ),下列说法不正确的是
),下列说法不正确的是
 和
和 溶液在加热条件下会生成
溶液在加热条件下会生成 ),下列说法不正确的是
),下列说法不正确的是
| A.Ⅰ中圆底烧瓶内的反应,体现了盐酸的酸性和还原性 |
| B.Ⅱ试管内的红色褪去后,再加热又恢复原来的红色 |
| C.Ⅲ和Ⅳ试管分别进行冷水浴和热水浴,反应的还原产物相同 |
D.Ⅴ试管内出现浑浊,氧化性: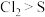 |
您最近一年使用:0次
6 . 下列实验操作及现象与结论之间对应关系正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向 溶液中加入铁粉,有红色固体析出 溶液中加入铁粉,有红色固体析出 | 氧化性: |
| B | 向紫色石蕊试液中不断通入干燥的 ,溶液最终呈无色 ,溶液最终呈无色 | 干燥的 有漂白性 有漂白性 |
| C | 向某白色粉末中滴加稀盐酸,产生能使澄清石灰水变浑浊的气体 | 该粉末中一定含 |
| D | 向某含 的溶液中滴加 的溶液中滴加 溶液,无明显现象,再滴加 溶液,无明显现象,再滴加 溶液后,溶液变成红色 溶液后,溶液变成红色 |  溶液可能是氯水 溶液可能是氯水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-04更新
|
64次组卷
|
2卷引用:河南省商丘市2023-2024学年高一上学期期末考试化学(B)试题
解题方法
7 . 下列实验操作或现象与实验目的均正确且匹配的是
| 选项 | 实验操作或现象 | 实验目的 |
| A |  固体受热熔化后可以导电 固体受热熔化后可以导电 | 证明 是电解质 是电解质 |
| B | 将饱和 溶液滴入稀 溶液滴入稀 溶液 溶液 | 制备 胶体 胶体 |
| C | 用洁净的玻璃棒蘸取溶液进行焰色试验 | 检验溶液中含有 |
| D | 将铝片插入 溶液中,短时间内无明显现象 溶液中,短时间内无明显现象 | 氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-03更新
|
104次组卷
|
2卷引用:广东省深圳市罗湖区2023-2024学年高一上学期期末考试化学试题
解题方法
8 . 某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。已知:铜与稀硝酸反应,金和稀硝酸不反应。回答下列问题:
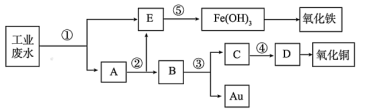
(1)图中标号处需加入的相应物质分别是①___________ 、②___________ (均写物质名称)。
(2)③处加入的物质为稀硝酸,化学反应为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,请用单线桥标明电子转移方向及数目___________ 。
(3)在浓度相等的条件下,Fe3+、Cu2+、Au3+氧化性由强到弱的顺序为___________ 。
(4)⑤处的总离子方程式为: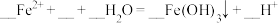 ,请补全缺项并配平
,请补全缺项并配平___________ ;该反应的现象为___________ 。

(1)图中标号处需加入的相应物质分别是①
(2)③处加入的物质为稀硝酸,化学反应为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,请用单线桥标明电子转移方向及数目
(3)在浓度相等的条件下,Fe3+、Cu2+、Au3+氧化性由强到弱的顺序为
(4)⑤处的总离子方程式为:
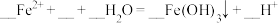 ,请补全缺项并配平
,请补全缺项并配平
您最近一年使用:0次
名校
9 .  气体与足量
气体与足量 溶液完全反应后,再加入
溶液完全反应后,再加入 溶液,发生如下反应:①
溶液,发生如下反应:①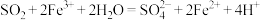 ;②
;② 。下列说法正确的是
。下列说法正确的是
 气体与足量
气体与足量 溶液完全反应后,再加入
溶液完全反应后,再加入 溶液,发生如下反应:①
溶液,发生如下反应:①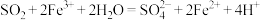 ;②
;② 。下列说法正确的是
。下列说法正确的是A.氧化性: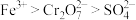 |
B.若有6.72L 完全反应,最终消耗0.2mol 完全反应,最终消耗0.2mol |
C.反应①中被还原的物质是 |
D.反应②中,1mol 参加反应,转移电子的数目为 参加反应,转移电子的数目为 |
您最近一年使用:0次
2024-02-03更新
|
164次组卷
|
3卷引用:湖北省武汉市部分重点中学2023-2024学年高一上学期期末联考化学试题
名校
10 . 室温下,下列实验探究方案不能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向盛有 溶液的试管中滴加几滴 溶液的试管中滴加几滴 溶液,振荡,再滴加几滴新制氯水,观察溶液颜色变化 溶液,振荡,再滴加几滴新制氯水,观察溶液颜色变化 | 证明 具有还原性 具有还原性 |
| B | 用玻璃棒蘸取某无色溶液后在酒精灯火焰上灼烧,观察火焰颜色 | 检验溶液中有 |
| C | 向盛有淀粉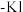 溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 | 比较 和 和 的氧化性强弱 的氧化性强弱 |
| D | 向包有足量过氧化钠粉末的脱脂棉上滴加几滴水,观察脱脂棉燃烧 | 证明过氧化钠与水反应放热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-03更新
|
187次组卷
|
3卷引用:吉林省长春吉大附中实验学校2023-2024学年高一上学期1月期末化学试题



