1 . 下列实验所选择的装置和试剂对应且正确的是
|
|
A.比较 、 、 、 、 的氧化性 的氧化性 | B.喷泉实验 |
|
|
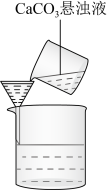
C.从 溶液中得到 溶液中得到 固体 固体 | D.固液分离 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 铅与碳是同族元素,有 两种价态,铅的氧化物均难溶于水,已知有下列两个反应:①
两种价态,铅的氧化物均难溶于水,已知有下列两个反应:① ;②
;② 。下列有关叙述不正确的是
。下列有关叙述不正确的是
 两种价态,铅的氧化物均难溶于水,已知有下列两个反应:①
两种价态,铅的氧化物均难溶于水,已知有下列两个反应:① ;②
;② 。下列有关叙述不正确的是
。下列有关叙述不正确的是A. 可写成 可写成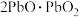 的形式 的形式 |
B.反应②中 是氧化产物 是氧化产物 |
C.生成相同质量的 ,反应①②转移电子数之比为 ,反应①②转移电子数之比为 |
D.根据反应可推测在题给条件下氧化性: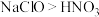 |
您最近一年使用:0次
3 . 已知氯酸钠与浓盐酸反应的化学方程式为NaClO3+6HCl(浓)=NaCl+3Cl2↑+3H2O。下列说法正确的是
| A.该反应每生成3molCl2,转移6NA个电子 |
| B.NaClO3是氧化剂,发生还原反应 |
| C.还原性:Cl2>HCl |
| D.氧化剂与还原剂的物质的量之比为1∶6 |
您最近一年使用:0次
解题方法
4 . 中科院大连化物所储能技术研究部提出了一种基于 辅助
辅助 放电的混合型液流电池,装置如图所示,下列说法错误的是
放电的混合型液流电池,装置如图所示,下列说法错误的是
 辅助
辅助 放电的混合型液流电池,装置如图所示,下列说法错误的是
放电的混合型液流电池,装置如图所示,下列说法错误的是
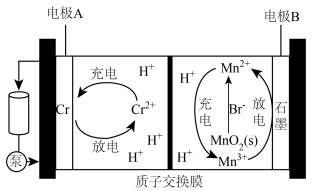
A.充电时, 向电极A迁移 向电极A迁移 |
B.在放电过程中,可利用 及时清除电极B上的“死锰” 及时清除电极B上的“死锰”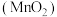 ,提高充放电过程的可逆性 ,提高充放电过程的可逆性 |
C.放电时,电极B上还可能发生: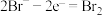 |
D.放电时,在该环境下的氧化性: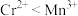 |
您最近一年使用:0次
5 . 依据下列实验和现象,得出结论正确的是
选项 | 实验 | 现象 | 结论 |
A | 向 | 有白色沉淀生成 | 酸性: |
B | 激光灯照射蛋白质溶液 | 观察到“光亮的通路” | 蛋白质溶液属于胶体 |
C | 向 | 溶液变蓝 | 氧化性: |
D | 向葡萄糖溶液中滴加酸性 | 酸性 | 葡萄糖中含有醛基 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
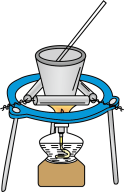
6 . 下列实验操作装置图中至少有三处错误的是
| A | B |
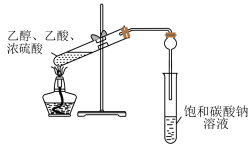 | 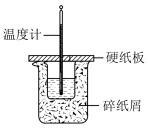 |
| 乙酸乙酯的制备 | 中和热的测定 |
| C | D |
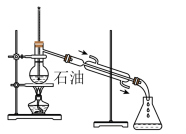 |  |
| 石油分馏 | 比较KMnO4、Cl2、S的氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 高铁酸钠(Na2FeO4)是一种新型、高效、多功能的水处理剂。高铁酸钠(Na2FeO4)制备方法有:
湿法制备:
干法制备: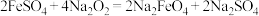 。
。
有关分析错误的是
湿法制备:

干法制备:
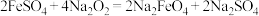 。
。有关分析错误的是
A.干法制备中每生成 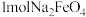 转移 转移  电子 电子 |
| B.湿法制备中,次氯酸钠的氧化性大于高铁酸钠 |
| C.在净水能力上,Na2FeO4氧化能力不如NaClO |
| D.高铁酸钠做水处理剂的优点之一是比较环保 |
您最近一年使用:0次
名校
8 . 下列实验目的、操作、现象及结论合理的是
| 实验目的 | 实验操作 | 现象及结论 | |
| A | 比较 与 与 氧化性强弱 氧化性强弱 | 取少量 溶液于试管中,滴入硫酸酸化的 溶液于试管中,滴入硫酸酸化的 溶液 溶液 | 溶液由浅绿色变为黄色氧化性: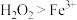 |
| B | 比较Mg与Al金属性强弱 | 向同浓度等体积的 、 、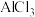 溶液中分别滴加同浓度的过量的NaOH溶液 溶液中分别滴加同浓度的过量的NaOH溶液 |  溶液中有白色沉淀生成且不溶解, 溶液中有白色沉淀生成且不溶解,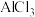 溶液中有白色沉淀生成后溶解,则金属性:Mg>Al 溶液中有白色沉淀生成后溶解,则金属性:Mg>Al |
| C | 检验 溶液中是否含有 溶液中是否含有 | 向溶液中滴加酸性 溶液 溶液 | 若紫红色退去,则溶液中含有 |
| D | 检验溶液中是否含有 | 取少量溶液于试管中,滴加稀盐酸 | 若产生的气体能使澄清石灰水变浑浊,则溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-08更新
|
269次组卷
|
2卷引用:浙江省杭州市长河高级中学2023-2024学年高一上学期期末考试化学试题
解题方法
9 . 某校化学学习小组分别设计了一组实验来探究元素周期律。第一小组根据元素非金属性与其对应最高价含氧酸之间的关系,设计了如图所示装置来完成元素非金属性强弱比较的实验探究。
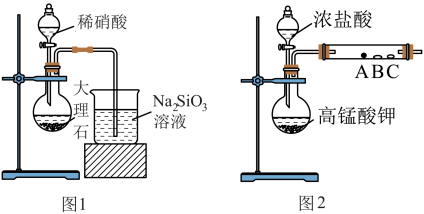
已知:I.稀硝酸具有挥发性。
Ⅱ. 是难溶于水的胶状沉淀。
是难溶于水的胶状沉淀。
Ⅲ.常温下浓盐酸能与高锰酸钾反应生成氯气。
回答下列问题:
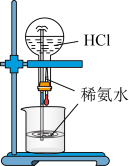
(1)第一小组为比较C、N、Si的非金属性强弱,用图1装置进行实验。
①烧杯中的现象为___________ ,其中 与
与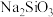 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为___________ 。
②根据实验现象,第一小组得出的结论是:元素的非金属性由强到弱的顺序为___________ 。但其中存在的问题是___________ 。
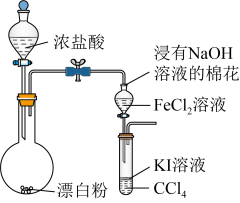
(2)第二小组设计了图2装置来验证卤素单质的氧化性强弱和潮湿的氯气具有漂白性, A、B、C三处分别是蘸有溴化钠溶液的棉花、湿润的淀粉-碘化钾试纸、湿润的红色纸条。
①写出A处发生反应的离子方程式:___________ 。
②第二小组通过实验___________ (“能”或“不能”)得出实验结论:氧化性: ;原因是
;原因是___________ 。

已知:I.稀硝酸具有挥发性。
Ⅱ.
 是难溶于水的胶状沉淀。
是难溶于水的胶状沉淀。Ⅲ.常温下浓盐酸能与高锰酸钾反应生成氯气。
回答下列问题:
(1)第一小组为比较C、N、Si的非金属性强弱,用图1装置进行实验。
①烧杯中的现象为
 与
与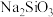 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为②根据实验现象,第一小组得出的结论是:元素的非金属性由强到弱的顺序为
(2)第二小组设计了图2装置来验证卤素单质的氧化性强弱和潮湿的氯气具有漂白性, A、B、C三处分别是蘸有溴化钠溶液的棉花、湿润的淀粉-碘化钾试纸、湿润的红色纸条。
①写出A处发生反应的离子方程式:
②第二小组通过实验
 ;原因是
;原因是
您最近一年使用:0次
名校
解题方法
10 . 下列实验操作、现象和解释与结论有错误的是
| 选项 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向硅酸钠溶液中通入适量 | 溶液变浑浊 | 酸性: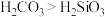 |
| B | 用 计测同温同浓度的 计测同温同浓度的 和 和 溶液的 溶液的 | 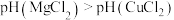 | 金属性: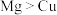 |
| C | 向足量含有 的 的 溶液中滴加2滴氯水 溶液中滴加2滴氯水 | 溶液变血红色 | 还原性: |
| D | 向NaCl和KI混合溶液中滴加 溶液 溶液 | 先产生黄色沉淀,后产生白色沉淀 | 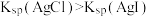 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 溶液中通入
溶液中通入 气体
气体
 的
的


