名校
解题方法
1 . 下列由实验现象所得结论正确的是
A.向 溶液中滴入稀硫酸酸化的 溶液中滴入稀硫酸酸化的 溶液,溶液由浅绿色变为黄色,证明 溶液,溶液由浅绿色变为黄色,证明 氧化性大于 氧化性大于 |
B.向某无色溶液中滴加1—2滴酚酞试液,一段时间后溶液仍呈无色,证明该溶液的 |
C.常温下将带火星的木条放入浓 加热分解生成的气体中,木条复燃,证明 加热分解生成的气体中,木条复燃,证明 支持燃烧 支持燃烧 |
D.将某气体通入淀粉和 的混合溶液,蓝色褪去,证明该气体具有漂白性 的混合溶液,蓝色褪去,证明该气体具有漂白性 |
您最近一年使用:0次
2024-02-11更新
|
365次组卷
|
2卷引用:上海市宜川中学2023-2024学年高三上学期11月考化学试卷
名校
2 .  将逐渐取代
将逐渐取代 成为生产自来水的消毒剂。工业上常通过如下反应制取:
成为生产自来水的消毒剂。工业上常通过如下反应制取: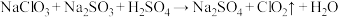 (未配平)。下列说法正确的是
(未配平)。下列说法正确的是
 将逐渐取代
将逐渐取代 成为生产自来水的消毒剂。工业上常通过如下反应制取:
成为生产自来水的消毒剂。工业上常通过如下反应制取: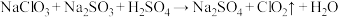 (未配平)。下列说法正确的是
(未配平)。下列说法正确的是| A.反应中氯元素被氧化,硫元素被还原 |
B.还原性: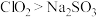 |
| C.氧化剂和还原剂的物质的量之比为2:1 |
D.每生成 转移2mol电子 转移2mol电子 |
您最近一年使用:0次
2024-02-11更新
|
164次组卷
|
4卷引用:陕西省宝鸡市金台区2023-2024学年高一上学期期末检测化学试题
3 .  是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过如下反应制得
是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过如下反应制得 :
: (未配平)。
(未配平)。 为阿伏加德罗常数的值,下列与该反应有关的说法中错误的是
为阿伏加德罗常数的值,下列与该反应有关的说法中错误的是
 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过如下反应制得
是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过如下反应制得 :
: (未配平)。
(未配平)。 为阿伏加德罗常数的值,下列与该反应有关的说法中错误的是
为阿伏加德罗常数的值,下列与该反应有关的说法中错误的是A.氧化剂与还原剂的物质的量之比为 |
B.还原性: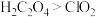 |
C. 作氧化剂发生还原反应 作氧化剂发生还原反应 |
D.若生成标准状况下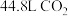 ,则转移电子数目为 ,则转移电子数目为 |
您最近一年使用:0次
2024-01-30更新
|
128次组卷
|
2卷引用:安徽省阜阳市2023-2024学年高一上学期期末联考化学试卷
名校
解题方法
4 . 有下列三个反应:
①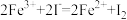
②
③
下列说法正确的是
①
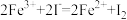
②

③

下列说法正确的是
A.①②③中的还原产物分别是 、 、 、 、 |
| B.在反应③中HCl做还原剂,每产生67.2LCl2,转移电子数目为6NA |
C.氧化性: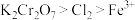 |
| D.反应①中铁元素被氧化,反应②铁元素被还原 |
您最近一年使用:0次
2024-01-24更新
|
110次组卷
|
2卷引用:四川省凉山州宁南中学2023-2024学年高一上学期期末考试化学模拟试题(一)
解题方法
5 . 铁—铬液流电池是近年新投产、较好利用储(放)能技术的新型电池。该电池总反应为 。下列有关说法错误的是
。下列有关说法错误的是
 。下列有关说法错误的是
。下列有关说法错误的是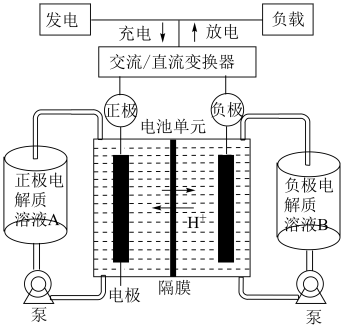
| A.放电时正极电解质溶液酸性增强 |
B.储能时原正极上的电极反应为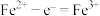 |
C.负极区电解质溶液中存在 与 与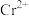 的相互转化 的相互转化 |
D.在相同条件下,离子的氧化性: |
您最近一年使用:0次
解题方法
6 . 探究是创新的源泉,某化学兴趣小组进行了制备氯气并探究卤素性质的实验。
(1)用二氧化锰与浓盐酸制备氯气,应选择的发生装置是_______ (填字母代号),该反应体现了浓盐酸的酸性和_______ (填“氧化性”或“还原性”)。
①甲中反应的离子方程式为_______ ,向反应后的橙黄色溶液中滴加 KI-淀粉溶液,溶液变为蓝色,通过上述实验_______ (填“能”或“不能”)得出氧化性:Cl2>Br2>I2。
②乙装置中 NaOH 溶液的作用为_______ ,其主要反应的化学方程式为_______ 。
(1)用二氧化锰与浓盐酸制备氯气,应选择的发生装置是
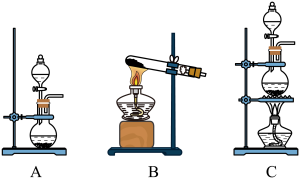
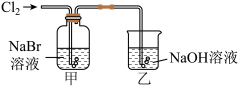
①甲中反应的离子方程式为
②乙装置中 NaOH 溶液的作用为
您最近一年使用:0次
名校
7 . 利用下列装置(夹持装置略)进行实验,能达到实验目的的是
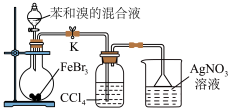 | 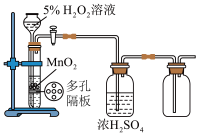 |
甲 | 乙 |
 |  |
丙 | 丁 |
| A.用甲装置制备溴苯并验证有HBr产生 | B.用乙装置制备氧气并收集纯净干燥的氧气 |
| C.用丙装置制备NO、收集和尾气处理 | D.用丁装置验证氧化性强弱顺序Cl2>Br2>I2 |
您最近一年使用:0次
2023-12-31更新
|
775次组卷
|
3卷引用:河北省石家庄市部分重点高中2023-2024学年高三上学期12月期末化学试题
8 . Ⅰ.下面两个方法都可以用来制氯气:①MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。③4HCl+O2
MnCl2+Cl2↑+2H2O;②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。③4HCl+O2 2Cl2+2H2O(g),根据以上两个反应,回答下列问题:
2Cl2+2H2O(g),根据以上两个反应,回答下列问题:
(1)反应①的离子方程式为___________ 。
(2)浓盐酸在反应①中表现出来的性质是___________。
(3)若要制得相同质量的氯气,反应①②所消耗的HCl的质量之比为___________ 。
(4)由上述3个反应发生的条件可推知MnO2、KMnO4、O2三种物质氧化性由强到弱的顺序为___________ 。
Ⅱ.某同学欲利用浓盐酸、MnO2、Fe等试剂制取无水氯化铁、收集一定量的氯气并验证其某些性质,实验装置如图所示(制气装置省略)。___________ (填名称)。
(6)装置③中现象是___________ ,装置④中有一处错误,更正为___________ 。
(7)装置⑦是用于氯气的尾气处理,防止污染空气,发生反应的化学方程式为___________ 。
 MnCl2+Cl2↑+2H2O;②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。③4HCl+O2
MnCl2+Cl2↑+2H2O;②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。③4HCl+O2 2Cl2+2H2O(g),根据以上两个反应,回答下列问题:
2Cl2+2H2O(g),根据以上两个反应,回答下列问题:(1)反应①的离子方程式为
(2)浓盐酸在反应①中表现出来的性质是___________。
| A.只有还原性 | B.只有氧化性 | C.只有酸性 | D.既表还原性和又表酸性 |
(3)若要制得相同质量的氯气,反应①②所消耗的HCl的质量之比为
(4)由上述3个反应发生的条件可推知MnO2、KMnO4、O2三种物质氧化性由强到弱的顺序为
Ⅱ.某同学欲利用浓盐酸、MnO2、Fe等试剂制取无水氯化铁、收集一定量的氯气并验证其某些性质,实验装置如图所示(制气装置省略)。
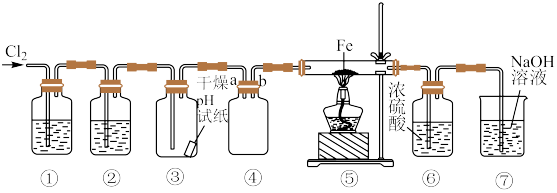
(6)装置③中现象是
(7)装置⑦是用于氯气的尾气处理,防止污染空气,发生反应的化学方程式为
您最近一年使用:0次
9 . A和B两支试管所盛的溶液中共含有K+、Ag+、Mg2+、Cl−、OH−、 六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
(1)若向某试管中滴入稀盐酸产生沉淀,则该试管为___________ (填“A”或“B”)。
(2)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是___________ (填化学式)。
(3)若将试管A和试管B中的溶液按一定体积比混合后过滤,蒸干所得滤液可得到一种纯净物,该物质为___________ ( 写化学式),则混合过程中发生反应的离子方程式为Ag++Cl-=AgCl↓与___________ (不考虑Ag+与OH−的反应)。
(4)按如图所示操作,充分反应后:___________ 。
②结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为___________ 。
(5)已知 可发生反应:
可发生反应:
①该反应中氧化剂是___________ (填化学式)。
②用双线桥法标出电子转移的数目和方向:___________ 。
 六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:(1)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(2)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(3)若将试管A和试管B中的溶液按一定体积比混合后过滤,蒸干所得滤液可得到一种纯净物,该物质为
(4)按如图所示操作,充分反应后:
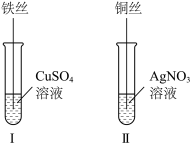
②结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(5)已知
 可发生反应:
可发生反应:
①该反应中氧化剂是
②用双线桥法标出电子转移的数目和方向:
您最近一年使用:0次
名校
解题方法
10 . 探究铁及其化合物的性质,下列方案设计、现象和结论不完全正确的是
实验方案 | 现象 | 结论 | |
A | 往 溶液中加入Zn片 溶液中加入Zn片 | 溶液浅绿色逐渐褪去 |  的氧化能力比 的氧化能力比 强 强 |
B | 往 溶液中滴加KSCN溶液,再加入少量 溶液中滴加KSCN溶液,再加入少量 固体 固体 | 溶液先变成血红色后无明显变化 |  对反应无影响 对反应无影响 |
C | 将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加KSCN溶液 | 溶液呈浅绿色 | 食品脱氧剂样品中没有+3价铁 |
D | 向沸水中逐滴加5~6滴饱和 溶液,持续煮沸 溶液,持续煮沸 | 溶液先变成红褐色再析出沉淀 |  先水解得 先水解得 再聚集成 再聚集成 沉淀 沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



