1 . 铬酸铅俗称铬黄,主要用于油漆、油墨、塑料以及橡胶等行业。一种以含铬废水(含 、
、 、
、 )和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下:
)和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下:
(1)草酸泥渣“粉碎”的目的是___________ ,“焙烧”时加入碳酸钠是为了将硫酸铅转化为氧化铅PbO,同时放出 ,该转化过程的化学方程式为
,该转化过程的化学方程式为___________ 。
(2)滤渣的主要成分为___________ 、___________ 。(填化学式)
(3)“沉淀除杂”所得滤液中含铬化合物主要为___________ 。(填化学式)
(4)“氧化”步骤加入过氧化氢溶液发生反应的离子方程式为___________ 。
(5)为了提高沉铬率,用平衡移动原理解释“酸溶”过程中所加硝酸不能过量的原因___________ 。
(6)处理含 的废水时,Cr(VI)被还原成Cr(Ⅲ)。若投入
的废水时,Cr(VI)被还原成Cr(Ⅲ)。若投入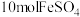 ,使金属阳离子恰好完全形成铁铬氧体(
,使金属阳离子恰好完全形成铁铬氧体( )沉淀,理论上还需要
)沉淀,理论上还需要 的物质的量为
的物质的量为___________ mol。
 、
、 、
、 )和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下:
)和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下: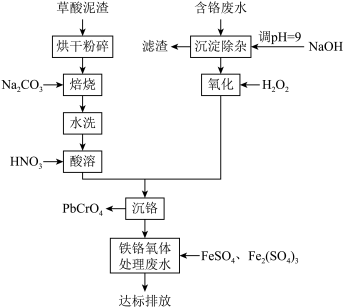

(1)草酸泥渣“粉碎”的目的是
 ,该转化过程的化学方程式为
,该转化过程的化学方程式为(2)滤渣的主要成分为
(3)“沉淀除杂”所得滤液中含铬化合物主要为
(4)“氧化”步骤加入过氧化氢溶液发生反应的离子方程式为
(5)为了提高沉铬率,用平衡移动原理解释“酸溶”过程中所加硝酸不能过量的原因
(6)处理含
 的废水时,Cr(VI)被还原成Cr(Ⅲ)。若投入
的废水时,Cr(VI)被还原成Cr(Ⅲ)。若投入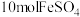 ,使金属阳离子恰好完全形成铁铬氧体(
,使金属阳离子恰好完全形成铁铬氧体( )沉淀,理论上还需要
)沉淀,理论上还需要 的物质的量为
的物质的量为
您最近半年使用:0次
2 . 向10.95g铜铝混合物(除铜、铝外无其他物质)中加入2 稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是
稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是
 稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是
稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是| A.V约为3.36 |
| B.混合物中铜与铝的物质的量之比为2∶1 |
| C.至少需要400mL稀硝酸 |
| D.滴加NaOH溶液的过程中,固体质量最大为18.2g |
您最近半年使用:0次
解题方法
3 . 已知某物质的XO(OH) 与Na2SO3反应时, XO(OH)
与Na2SO3反应时, XO(OH) 作氧化剂,Na2SO3被氧化为Na2SO4。经测得4分子XO(OH)
作氧化剂,Na2SO3被氧化为Na2SO4。经测得4分子XO(OH) 与2分子的Na2SO3恰好完全作用。试问XO(OH)
与2分子的Na2SO3恰好完全作用。试问XO(OH) 还原后X的最终价态是
还原后X的最终价态是
 与Na2SO3反应时, XO(OH)
与Na2SO3反应时, XO(OH) 作氧化剂,Na2SO3被氧化为Na2SO4。经测得4分子XO(OH)
作氧化剂,Na2SO3被氧化为Na2SO4。经测得4分子XO(OH) 与2分子的Na2SO3恰好完全作用。试问XO(OH)
与2分子的Na2SO3恰好完全作用。试问XO(OH) 还原后X的最终价态是
还原后X的最终价态是| A.+3 | B.+4 | C.+5 | D.0 |
您最近半年使用:0次
名校
4 . 二氧化碳、甲烷的捕集、转化与利用对环境和能源具有重要意义。
Ⅰ. 的捕集
的捕集
(1)地球上最高效的碳捕捉过程是绿色植物的______ ,该过程中能量的转化形式为______ 。
(2)用碱液吸收 。
。
①用足量NaOH溶液吸收 ,该过程中溶液的温度
,该过程中溶液的温度______ (填“上升”或“下降”)。
②若用100 mL 5 mol⋅L 的NaOH溶液吸收
的NaOH溶液吸收 后,测得吸收液中的
后,测得吸收液中的 ,则吸收的
,则吸收的 在标准状况下的体积为
在标准状况下的体积为______ L。
Ⅱ. 、
、 的转化
的转化
(3)在一定条件下,在催化剂表面将 转化为
转化为 ,其原理如图所示:
,其原理如图所示: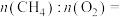
______ 。
Ⅲ. 、
、 的利用
的利用
(4)一种将 转化为合成气(
转化为合成气( 和CO)的原理如图所示:
和CO)的原理如图所示:____________ 。
②理论上,2.24 L (标准状况)通过以上两步反应最多可制得
(标准状况)通过以上两步反应最多可制得 的物质的量为
的物质的量为______ 。
(5)通过人工光合作用可实现对 的再利用,以
的再利用,以 和
和 为原料制备甲酸(HCOOH),工作原理如图所示:
为原料制备甲酸(HCOOH),工作原理如图所示: 的移动方向是左
的移动方向是左______ 右(填“→”或“←”)。
②电极b上的电极反应式为____________ 。
Ⅰ.
 的捕集
的捕集(1)地球上最高效的碳捕捉过程是绿色植物的
(2)用碱液吸收
 。
。①用足量NaOH溶液吸收
 ,该过程中溶液的温度
,该过程中溶液的温度②若用100 mL 5 mol⋅L
 的NaOH溶液吸收
的NaOH溶液吸收 后,测得吸收液中的
后,测得吸收液中的 ,则吸收的
,则吸收的 在标准状况下的体积为
在标准状况下的体积为Ⅱ.
 、
、 的转化
的转化(3)在一定条件下,在催化剂表面将
 转化为
转化为 ,其原理如图所示:
,其原理如图所示: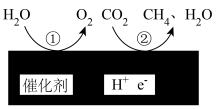
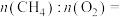
Ⅲ.
 、
、 的利用
的利用(4)一种将
 转化为合成气(
转化为合成气( 和CO)的原理如图所示:
和CO)的原理如图所示: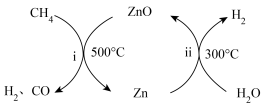
②理论上,2.24 L
 (标准状况)通过以上两步反应最多可制得
(标准状况)通过以上两步反应最多可制得 的物质的量为
的物质的量为(5)通过人工光合作用可实现对
 的再利用,以
的再利用,以 和
和 为原料制备甲酸(HCOOH),工作原理如图所示:
为原料制备甲酸(HCOOH),工作原理如图所示: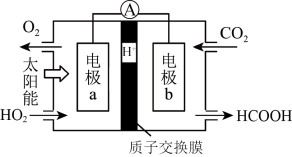
 的移动方向是左
的移动方向是左②电极b上的电极反应式为
您最近半年使用:0次
5 .  铜锌合金完全溶解于
铜锌合金完全溶解于 的浓硝酸(密度为
的浓硝酸(密度为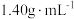 )中,得到
)中,得到 和
和 混合气体
混合气体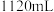 (换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入
(换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入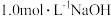 溶液,当金属离子刚好全部沉淀,得到
溶液,当金属离子刚好全部沉淀,得到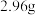 沉淀。下列说法正确的是
沉淀。下列说法正确的是
 铜锌合金完全溶解于
铜锌合金完全溶解于 的浓硝酸(密度为
的浓硝酸(密度为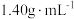 )中,得到
)中,得到 和
和 混合气体
混合气体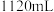 (换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入
(换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入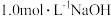 溶液,当金属离子刚好全部沉淀,得到
溶液,当金属离子刚好全部沉淀,得到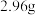 沉淀。下列说法正确的是
沉淀。下列说法正确的是A.该合金中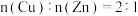 |
B.合金完全溶解时,溶液中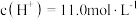 |
C. 和 和 的混合气体中, 的混合气体中, 的体积分数是 的体积分数是 |
D.刚好得到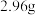 沉淀时,加入 沉淀时,加入 溶液的体积是 溶液的体积是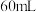 |
您最近半年使用:0次
名校
6 . 将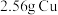 投入
投入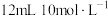 硝酸中,恰好完全反应,向反应后的溶液中加入
硝酸中,恰好完全反应,向反应后的溶液中加入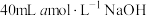 溶液,
溶液, 恰好完全沉淀,将生成的气体与
恰好完全沉淀,将生成的气体与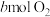 一起通入足量
一起通入足量 溶液中,气体恰好被完全吸收生成
溶液中,气体恰好被完全吸收生成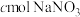 。下列判断正确的是
。下列判断正确的是
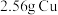 投入
投入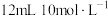 硝酸中,恰好完全反应,向反应后的溶液中加入
硝酸中,恰好完全反应,向反应后的溶液中加入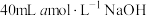 溶液,
溶液, 恰好完全沉淀,将生成的气体与
恰好完全沉淀,将生成的气体与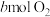 一起通入足量
一起通入足量 溶液中,气体恰好被完全吸收生成
溶液中,气体恰好被完全吸收生成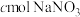 。下列判断正确的是
。下列判断正确的是| A.生成的气体中只有NO | B. |
C. | D.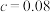 |
您最近半年使用:0次
名校
解题方法
7 . 为了测定镁铜合金的组成,将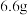 镁、铜合金加入
镁、铜合金加入 某浓度的稀硝酸中,将合金完全溶解后,共收集到
某浓度的稀硝酸中,将合金完全溶解后,共收集到 气体
气体 (标准状况下),并测得溶液中
(标准状况下),并测得溶液中 的浓度为
的浓度为 ,若反应前后溶液的体积变化忽略不计,则下列判断不正确的是
,若反应前后溶液的体积变化忽略不计,则下列判断不正确的是
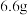 镁、铜合金加入
镁、铜合金加入 某浓度的稀硝酸中,将合金完全溶解后,共收集到
某浓度的稀硝酸中,将合金完全溶解后,共收集到 气体
气体 (标准状况下),并测得溶液中
(标准状况下),并测得溶液中 的浓度为
的浓度为 ,若反应前后溶液的体积变化忽略不计,则下列判断不正确的是
,若反应前后溶液的体积变化忽略不计,则下列判断不正确的是A.上述反应中金属共失去电子 |
B.合金中,铜的质量为 |
C.原硝酸的浓度: |
D.要使溶液中的金属离子完全沉淀,需加 的 的 溶液 溶液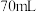 |
您最近半年使用:0次
8 . 草酸是一种二元弱酸,可用作还原剂、沉淀剂等。某校课外小组的同学设计利用C2H2气体制取H2C2O4·2H2O。回答下列问题:
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。___________ (写一种即可)。
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为___________ 。该过程中,可能产生新的杂质气体Cl2,其原因是:___________ (用离子方程式回答)。
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是___________ 。
②装置D中生成H2C2O4的化学方程式为___________ 。
③从装置D中得到产品,还需经过___________ (填操作名称)、过滤、洗涤及干燥。
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是___________ 。
②产品中H2C2O4·2H2O的质量分数为___________ (列出含 m、c、V 的表达式)。
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。
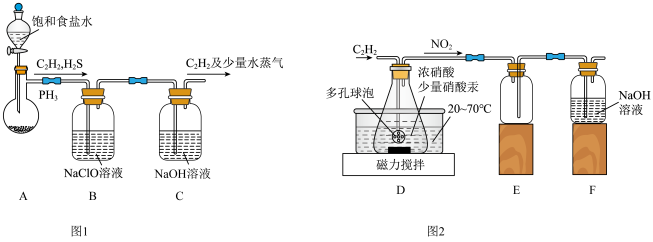
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是
②装置D中生成H2C2O4的化学方程式为
③从装置D中得到产品,还需经过
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是
②产品中H2C2O4·2H2O的质量分数为
您最近半年使用:0次
名校
9 . 将13.6g Cu和Cu2O组成的混合物加入250 mL一定浓度的稀硝酸中,固体完全溶解生成Cu(NO3)2和NO,向所得溶液中加入1.0 L 0.5 mol/LNaOH溶液时,金属离子恰好沉淀完全,生成沉淀的质量为19.6 g,下列说法错误的是
| A.原稀硝酸的浓度为2 mol/L |
| B.Cu和Cu2O的物质的量之比为2:1 |
| C.反应后剩余硝酸的物质的量为0.1 mol |
| D.产生的NO在标准状况下的体积为2.24L |
您最近半年使用:0次
名校
解题方法
10 . 将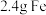 、Mg合金投入一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体
、Mg合金投入一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体 (硝酸被还原成NO),若向反应后的溶液中加入足量的
(硝酸被还原成NO),若向反应后的溶液中加入足量的 溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为
溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为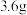 。则收集到的气体体积V的值不可能是
。则收集到的气体体积V的值不可能是
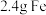 、Mg合金投入一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体
、Mg合金投入一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体 (硝酸被还原成NO),若向反应后的溶液中加入足量的
(硝酸被还原成NO),若向反应后的溶液中加入足量的 溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为
溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为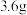 。则收集到的气体体积V的值不可能是
。则收集到的气体体积V的值不可能是| A.1.10 | B.1.00 | C.0.90 | D.0.784 |
您最近半年使用:0次



