1 . 下列对化学实验及现象的解释不合理的是
| 选项 | 化学实验及现象 | 解释 |
| A | 分别向浓度均为0.1 的 的 和 和 溶液中通入 溶液中通入 至饱和,前者无明显现象,后者生成沉淀 至饱和,前者无明显现象,后者生成沉淀 | 溶度积常数: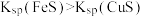 |
| B | 将 分别通入品红的乙醇溶液和品红的水溶液中,品红的乙醇溶液不褪色,品红的水溶液逐渐褪色 分别通入品红的乙醇溶液和品红的水溶液中,品红的乙醇溶液不褪色,品红的水溶液逐渐褪色 | 使品红褪色的不是 而是 而是 与水反应后的产物 与水反应后的产物 |
| C | 向KI溶液中加入少量氯水和 ,振荡、静置,下层溶液为紫红色 ,振荡、静置,下层溶液为紫红色 | 还原性: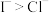 |
| D | 向0.01  溶液中,加入少量 溶液中,加入少量 固体,溶液颜色加深 固体,溶液颜色加深 |  水解程度增大 水解程度增大 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
2 . 向含 、
、 、
、 的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
 、
、 、
、 的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
A.原溶液中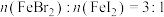 | B.线段II表示 的变化情况 的变化情况 |
C.线段IV表示 的变化情况 的变化情况 | D.根据图像可计算出a=5 |
您最近半年使用:0次
3 . 已知Ⅰ: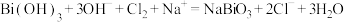 ;
;
Ⅱ.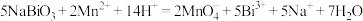 。下列推断不正确的是
。下列推断不正确的是
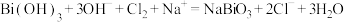 ;
;Ⅱ.
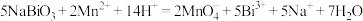 。下列推断不正确的是
。下列推断不正确的是A. 可与盐酸发生反应: 可与盐酸发生反应: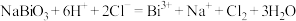 |
B.任何条件下,都存在氧化性: |
C.反应Ⅱ中,当有10.45g 生成时转移电子数为 生成时转移电子数为 |
D.已知 可由 可由 与王水(浓硝酸和浓盐酸的混合物)反应制取,说明 与王水(浓硝酸和浓盐酸的混合物)反应制取,说明 不能被硝酸氧化 不能被硝酸氧化 |
您最近半年使用:0次
4 . 氮和氧是构建化合物的常见元素。
(1)下列说法正确的是___________。
(2)①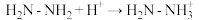 ,其中
,其中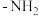 的
的 原子杂化方式为
原子杂化方式为___________ ;比较键角 中的-NH2
中的-NH2_____ H2N-NH 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由___________ 。
②将 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是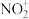 。比较氧化性强弱:NO
。比较氧化性强弱:NO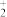
_____ HNO3(填“>”、“<”或“=”);写出A中阴离子的结构式___________ 。
已知: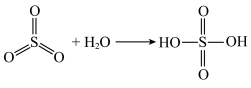
(1)下列说法正确的是___________。
A.电负性: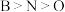 | B.离子半径: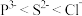 |
C.第一电离能: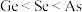 | D.基态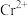 的简化电子排布式: 的简化电子排布式: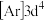 |
(2)①
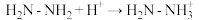 ,其中
,其中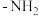 的
的 原子杂化方式为
原子杂化方式为 中的-NH2
中的-NH2 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由②将
 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是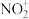 。比较氧化性强弱:NO
。比较氧化性强弱:NO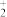
您最近半年使用:0次
5 . 实验是学习化学的基础。已知:[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-呈无色。根据实验操作及现象,下列结论中正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向FeCl3溶液中滴K3[Fe(CN)6]溶液,再加入少量铜粉 | 开始时无明显变化,加入铜粉后产生蓝色沉淀 | 氧化性:Fe3+>Cu2+ |
| B | 将C2H5Br与NaOH溶液共热。冷却后,加入AgNO3溶液 | 没有产生淡黄色沉淀 | C2H5Br没有发生水解反应 |
| C | 将CoCl2固体溶于水,加入适量浓盐酸后,再加入少量ZnCl2固体 | 溶液先由粉红色变为蓝色,再由蓝色变成无色 | 稳定性:[CoCl4]2->[ZnCl4]2- |
| D | 常温下,分别测定1mol/LCH3COONH4溶液和0.1mol/LCH3COONH4溶液的pH | pH都等于7 | 同温下,不同浓度CH3COONH4溶液中水的电离程度相同 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024·黑龙江·模拟预测
解题方法
6 . 下列探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 将浓硫酸滴入乙醇中,加热至 ,生成的气体通入酸性高锰酸钾溶液 ,生成的气体通入酸性高锰酸钾溶液 | 验证乙烯具有还原性 |
| B | 向0.1 H2O2溶液中滴加0.1 H2O2溶液中滴加0.1 KMnO4溶液,观察溶液颜色变化 KMnO4溶液,观察溶液颜色变化 | 探究H2O2具有氧化性 |
| C | 向某溶液中加入氢氧化钠溶液并加热,观察产生的气体能否使蓝色石蕊试纸变色 | 溶液中是否存在NH |
| D | 向 溶液中同时通入 溶液中同时通入 和 和 | 比较 和 和 的氧化能力 的氧化能力 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
7 . 请回答下列问题:
(1)已知实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为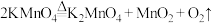 ,氧化产物是
,氧化产物是___________ (填化学式)。
(2)已知反应:
① ;
;
②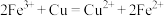 ;
;
③ ;
;
④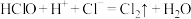 。
。
微粒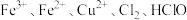 氧化性由强到弱的顺序为
氧化性由强到弱的顺序为___________ 。
(1)已知实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为
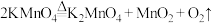 ,氧化产物是
,氧化产物是(2)已知反应:
①
 ;
;②
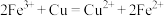 ;
;③
 ;
;④
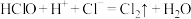 。
。微粒
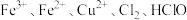 氧化性由强到弱的顺序为
氧化性由强到弱的顺序为
您最近半年使用:0次
8 . 下列实验设计能够成功的是
A.除去粗盐中含有的硫酸钙杂质:粗盐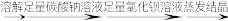 精盐 精盐 |
B.检验亚硫酸钠试样是否变质:试样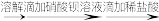 白色沉淀不溶解→试样已变质 白色沉淀不溶解→试样已变质 |
C.证明酸性条件H2O2的氧化性比I2强:NaI溶液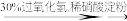 溶液变蓝色→氧化性:H2O2>I2 溶液变蓝色→氧化性:H2O2>I2 |
D.检验某溶液中是否含有Fe2+:试样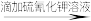 溶液颜色无变化 溶液颜色无变化 溶液变红色→溶液中含有Fe2+ 溶液变红色→溶液中含有Fe2+ |
您最近半年使用:0次
9 . 基态饿原子( )的价电子排布式为
)的价电子排布式为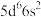 。氧化物
。氧化物 常作烯烃醇化的氧化剂,其重要的氮基饿酸盐有
常作烯烃醇化的氧化剂,其重要的氮基饿酸盐有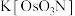 。有关反应如下:
。有关反应如下:
反应I:
反应Ⅱ:
 )的价电子排布式为
)的价电子排布式为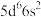 。氧化物
。氧化物 常作烯烃醇化的氧化剂,其重要的氮基饿酸盐有
常作烯烃醇化的氧化剂,其重要的氮基饿酸盐有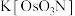 。有关反应如下:
。有关反应如下:反应I:

反应Ⅱ:

反应IⅢ:
A. 的立体异构分子中不存在手性分子 的立体异构分子中不存在手性分子 |
B.反应I中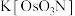 的 的 的化合价为+8 的化合价为+8 |
| C.反应Ⅱ中氧化产物与还原产物的物质的量之比为1∶1 |
D.由反应Ⅲ可推测氧化性: 强于酸性 强于酸性 溶液 溶液 |
您最近半年使用:0次
名校
10 . 大苏打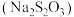 常用于防毒面具中吸收氯气,
常用于防毒面具中吸收氯气,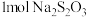 完全反应,失去
完全反应,失去 电子,下列说法正确的是
电子,下列说法正确的是
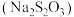 常用于防毒面具中吸收氯气,
常用于防毒面具中吸收氯气,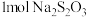 完全反应,失去
完全反应,失去 电子,下列说法正确的是
电子,下列说法正确的是A.氧化性: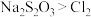 |
B.反应中 转化为 转化为 |
C.氧化产物与还原产物的物质的量之比为 |
D.标准状况下,每吸收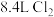 ,反应中转移电子数为 ,反应中转移电子数为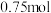 |
您最近半年使用:0次



