1 . 下述装置或操作能实现相应实验目的的是
| 装置或操作 |
|
|
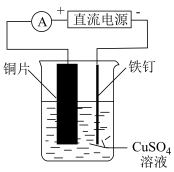
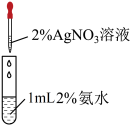
| 实验目的 | 铁钉表面镀铜 | 配制银氨溶液 |
| 选项 | A | B |
| 装置或操作 |
|
|
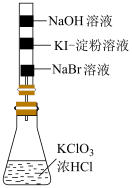
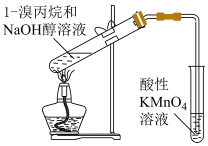
| 实验目的 | 验证氧化性:Cl2>Br2>I2 | 检验1-溴丙烷的消去反应产物丙烯 |
| 选项 | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 标准电极电位指离子有效浓度为1mol/L时相对标准氢电极的电极电位差值,电对的标准电极电势 越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①
越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①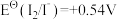 ;②
;②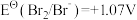 ;③
;③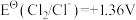 ;④
;④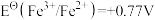 ;⑤
;⑤ ;⑥
;⑥ 。下列有关说法正确的是
。下列有关说法正确的是
 越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①
越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①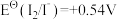 ;②
;②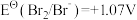 ;③
;③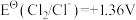 ;④
;④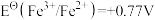 ;⑤
;⑤ ;⑥
;⑥ 。下列有关说法正确的是
。下列有关说法正确的是A.向1mol/L的HBr溶液中滴加 溶液,无明显现象发生 溶液,无明显现象发生 |
B.2mol/L的 与2mol/L的稀盐酸等体积混合有大量 与2mol/L的稀盐酸等体积混合有大量 产生 产生 |
C.在含 、 、 、 、 的混合溶液中若仅氧化 的混合溶液中若仅氧化 ,最佳的氧化剂是 ,最佳的氧化剂是 |
D.浓度相等时,还原性: |
您最近一年使用:0次
解题方法
3 . 下列实验操作不能达到相应实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 提纯 | 将含少量 的 的 固体溶于足量浓氨水中,过滤、洗涤、干燥 固体溶于足量浓氨水中,过滤、洗涤、干燥 |
| B | 向 溶液中滴加几滴KSCN溶液,振荡,再滴加几滴新制氯水,观察溶液颜色的变化 溶液中滴加几滴KSCN溶液,振荡,再滴加几滴新制氯水,观察溶液颜色的变化 |  的还原性比 的还原性比 的强 的强 |
| C | 室温下,向一定量饱和 溶液中通入足量 溶液中通入足量 气体,观察是否有晶体析出 气体,观察是否有晶体析出 | 室温下固体在水中的溶解性: |
| D | 用pH计测量相同温度、相同浓度NaClO溶液、 溶液的pH,比较pH大小 溶液的pH,比较pH大小 | HClO的酸性比 的强 的强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列实验操作不能达到实验目的的是
| 选项 | 操作及现象 | 目的 |
| A | 将含少量 的 的 溶于浓氨水中,过滤、洗涤、干燥 溶于浓氨水中,过滤、洗涤、干燥 | 提纯 |
| B | 加热溴乙烷和NaOH的乙醇溶液混合物,产生的气体通入溴水溶液中,溶液褪色 | 证明溴乙烷发生了消去反应 |
| C | 在饱和 溶液中加入少量KI粉末,产生黄色沉淀 溶液中加入少量KI粉末,产生黄色沉淀 | 证明溶液存在沉淀溶解平衡 |
| D | 在 溶液中滴加酸化的双氧水,溶液变棕色 溶液中滴加酸化的双氧水,溶液变棕色 | 探究 、 、 的还原性强弱 的还原性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 将 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法正确的是
A.基态Cu原子的电子排布式为 |
B.过程①的离子方程式为: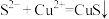 |
C.氧化性: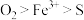 |
D.相同条件下, 和空气的比例不影响处理效果 和空气的比例不影响处理效果 |
您最近一年使用:0次
名校
6 .  .某实验小组为探究含硫化合物
.某实验小组为探究含硫化合物 的性质,设计如下实验探究
的性质,设计如下实验探究 的氧化性。
的氧化性。
实验操作:向小试管中加入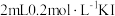 溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量
溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量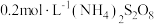 溶液,试管中溶液立即变蓝。取上层清液检验,证明溶液中存在
溶液,试管中溶液立即变蓝。取上层清液检验,证明溶液中存在 。
。
(1) 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(2)检验该溶液中存在 的具体操作及现象为
的具体操作及现象为___________ 。
(3)实验结论: 的氧化性
的氧化性___________ (填“强于”或“弱于”) 。
。
已知: 可与
可与 发生反应:
发生反应: 。为了进一步探究
。为了进一步探究 与
与 的反应速率,小组同学设计下表实验:
的反应速率,小组同学设计下表实验:
(4)上述实验 中的
中的
___________ ;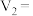
___________ 。
加入 溶液后溶液变蓝的时间明显增长,小组同学对此提出两种清想:
溶液后溶液变蓝的时间明显增长,小组同学对此提出两种清想:
猜想1: 与
与 反应的速率远低于
反应的速率远低于 与
与 反应的速率;
反应的速率;
猜想2: 先与
先与 反应,
反应, 消耗完后才与
消耗完后才与 反应。
反应。
为验证上述猜想,小组同学补充下表实验(已知 密度比水大,且
密度比水大,且 溶于
溶于 显紫色)
显紫色)
(5)验证猜想1的实验设计为___________ 。(填“实验 ”或“实验
”或“实验 ”)
”)
(6)实验 中下层溶液显浅紫色的原因为
中下层溶液显浅紫色的原因为___________ 。
(7)由上述实验可知___________ (填“猜想1”或“猜想2”)成立。
 .某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。
.某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。 空气时,酸性
空气时,酸性 溶液恰好褪色,停止实验。发生反应的离子方程式为:
溶液恰好褪色,停止实验。发生反应的离子方程式为:___________ 。该空气中二氧化硫的体积分数为___________ 。
 .某实验小组为探究含硫化合物
.某实验小组为探究含硫化合物 的性质,设计如下实验探究
的性质,设计如下实验探究 的氧化性。
的氧化性。实验操作:向小试管中加入
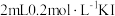 溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量
溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量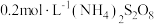 溶液,试管中溶液立即变蓝。取上层清液检验,证明溶液中存在
溶液,试管中溶液立即变蓝。取上层清液检验,证明溶液中存在 。
。(1)
 与
与 反应的离子方程式为
反应的离子方程式为(2)检验该溶液中存在
 的具体操作及现象为
的具体操作及现象为(3)实验结论:
 的氧化性
的氧化性 。
。已知:
 可与
可与 发生反应:
发生反应: 。为了进一步探究
。为了进一步探究 与
与 的反应速率,小组同学设计下表实验:
的反应速率,小组同学设计下表实验:| 试验编号 |  溶液/ 溶液/ | 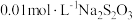 溶液/ 溶液/ | 蒸馏水/ | 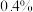 的淀粉溶液/滴 的淀粉溶液/滴 | 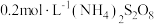 溶液/ 溶液/ | 变色 时间/s |
 | 4.0 | 0 | 4.0 | 2 | 2.0 | 立即 |
 | 4.0 | 1.0 |  | 2 |  | 30 |
(4)上述实验
 中的
中的
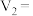
加入
 溶液后溶液变蓝的时间明显增长,小组同学对此提出两种清想:
溶液后溶液变蓝的时间明显增长,小组同学对此提出两种清想:猜想1:
 与
与 反应的速率远低于
反应的速率远低于 与
与 反应的速率;
反应的速率;猜想2:
 先与
先与 反应,
反应, 消耗完后才与
消耗完后才与 反应。
反应。为验证上述猜想,小组同学补充下表实验(已知
 密度比水大,且
密度比水大,且 溶于
溶于 显紫色)
显紫色)| 试验编号 |   溶液/ 溶液/ | 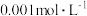 碘水/ 碘水/ |   溶液/ 溶液/ |  / / | 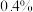 的淀粉溶液/滴 的淀粉溶液/滴 |   溶液/ 溶液/ | 实验现象 |
 | 2 | 0 | 20 | 10 | 0 | 0.2 | 下层溶液显浅紫色 |
 | 0 | 5 | 20 | 0 | 2 | 20 | 溶液先变蓝,后迅速褪色,一段时间后又变蓝 |
(5)验证猜想1的实验设计为
 ”或“实验
”或“实验 ”)
”)(6)实验
 中下层溶液显浅紫色的原因为
中下层溶液显浅紫色的原因为(7)由上述实验可知
 .某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。
.某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。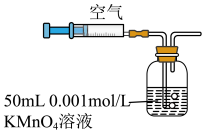
 空气时,酸性
空气时,酸性 溶液恰好褪色,停止实验。发生反应的离子方程式为:
溶液恰好褪色,停止实验。发生反应的离子方程式为:
您最近一年使用:0次
名校
解题方法
7 . 下列实验操作、现象和得出的结论正确的是
| 实验操作 | 现象 | 结论 | |
| A | 取少量Fe(NO3)2溶液于试管中,滴入硫酸酸化的H2O2溶液 | 溶液由浅绿色变为黄色 | 氧化性:H2O2>Fe3+ |
| B | 向溶液中加入盐酸酸化的氯化钡 | 产生白色沉淀 | 溶液中一定含有 |
| C | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 试管里出现凝胶 | 非金属性:Cl>Si |
| D | 取5mL0.1mol/LKI溶液于试管中,加入1mL0.1mol/LFeCl3溶液,充分反应后滴入5滴10%KSCN溶液 | 溶液变血红色 | KI与FeCl3的反应有一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 如图是部分短周期主族元素原子半径与原子序数的关系图。
(1)写出A在元素周期表中的位置___________ 。比较Z、Q两种元素的简单离子半径大小___________ ;M的原子结构示意图为___________ 。
(2)图中最活泼的金属是___________ ,将其单质在氧气中加热,生成的产物为___________ 。
该元素的最高价氧化物对应的水化物与L的最高价氧化物对应的水化物发生反应的离子方程式为___________ 。
(3)比较X、R两种元素的简单气态氢化物的沸点高低___________ ;B的氢化物在常温下跟该元素的最高价氧化物对应的水化物发生反应生成的物质的化学式___________ 。
(4)最高价氧化物的水化物中酸性最强的是___________ 。(填化学式)
(5)用一个化学方程式证明X单质氧化性比Q的强:___________ 。

(1)写出A在元素周期表中的位置
(2)图中最活泼的金属是
该元素的最高价氧化物对应的水化物与L的最高价氧化物对应的水化物发生反应的离子方程式为
(3)比较X、R两种元素的简单气态氢化物的沸点高低
(4)最高价氧化物的水化物中酸性最强的是
(5)用一个化学方程式证明X单质氧化性比Q的强:
您最近一年使用:0次
名校
9 . 下列有关推理中得到的结论与事实不相符合的是
A.Cu可以还原 得到 得到 ,所以Fe也可以还原 ,所以Fe也可以还原 生成 生成 |
B.常温条件下,Cu与浓硝酸剧烈反应放出 气体,所以Fe和浓硝酸反应将更加剧烈 气体,所以Fe和浓硝酸反应将更加剧烈 |
C. 与NaOH溶液反应生成碳酸盐, 与NaOH溶液反应生成碳酸盐, 也与NaOH溶液反应生成亚硫酸盐 也与NaOH溶液反应生成亚硫酸盐 |
| D.亚硫酸的酸性强于碳酸,所以硫酸的酸性也强于碳酸 |
您最近一年使用:0次
名校
解题方法
10 . 以下是一系列非金属元素间的置换反应,其中不能说明反应前的非金属单质的氧化性强于产物中非金属单质的氧化性的是
A. | B.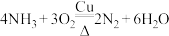 |
C. | D. |
您最近一年使用:0次