|
|
|
|
A.用 浓硫酸配制 浓硫酸配制 稀硫酸 稀硫酸 | B.制备 并长时间观察其颜色 并长时间观察其颜色 | C.比较 和 和 的氧化性强弱 的氧化性强弱 | D.吸收尾气中的Cl2 |
| A.A | B.B | C.C | D.D |
 将逐渐取代
将逐渐取代 成为自来水的消毒剂。工业上常通过如下反应制取:
成为自来水的消毒剂。工业上常通过如下反应制取: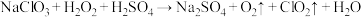 (未配平)。下列说法正确的是
(未配平)。下列说法正确的是| A.反应中氯元素被氧化,氧元素被还原 | B.还原性: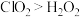 |
C.生成 转移 转移 电子 电子 | D.氧化剂和还原剂的物质的量之比为 |
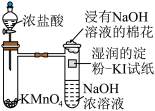
3 . 为达到实验目的,下列装置及方案设计合理的是
选项 |
|
|
|
|
实验目的 | 证明热稳定性: | 除去 | 干燥氯气 | 证明氧化性: |
装置及方案 |
|
|
|
|
| A.A | B.B | C.C | D.D |
4 . 实验小组用如图装置探究Cl2、Fe3+、I2的氧化性强弱(夹持装置和加热装置已省略,气密性已检验)。
已知:I2遇淀粉溶液变蓝

实验过程:
I.打开弹簧夹K1和K2,通入一段时间N2,再将导管插入B中,继续通入N2一段时间,然后夹紧K1;
Ⅱ.打开活塞a,滴加一定量浓盐酸后关闭活塞a,给A加热;
Ⅲ.当B中的溶液变为黄色时,停止加热,夹紧K2;
IV.打开活塞b,将少量B中溶液滴入C中,关闭活塞b。
(1)操作I中通入一段时间N2的目的是
(2)浸有NaOH溶液的棉花的作用是
(3)B中溶液变黄说明氧化性Cl2>Fe3+,反应的离子方程式是
(4)为探究Fe3+和I2的氧化性强弱,甲、乙、丙三位同学分别完成了上述实验,并检测B中黄色溶液和C中混合溶液中的部分微粒,结果如表所示(忽略空气中O2的影响)。
B中部分微粒 | C中部分微粒 | |
甲 | 既有Fe3+又有Fe2+ | 有I2 |
乙 | 有Fe3+无Fe2+ | 有I2 |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |
①检验B中黄色溶液中含有Fe3+的试剂是
②进一步检验IL的实验操作及现象是
③能证明该实验条件下氧化性Fe3+>I2的有
不能证明的请说明理由
④已知碘原子的原子结构示意图为 ,从原子结构角度解释碘原子的得电子能力弱于氯原子的原因
,从原子结构角度解释碘原子的得电子能力弱于氯原子的原因
| 选项 | A | B | C | D |
| 装置 |  | 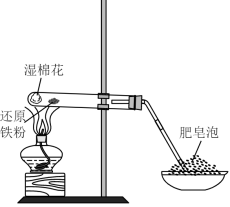 |  | 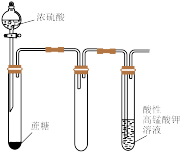 |
| 现象 | 紫红色溶液变浅并伴有黄绿色气体产生 | 产生大量肥皂泡 | 滴加硫酸后溶液显弱酸性,蓝色迅速褪去,无气体产生。 | 酸性 溶液中出现气泡,且颜色逐渐褪去 溶液中出现气泡,且颜色逐渐褪去 |
| 结论 | 氧化性顺序: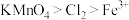 |  与水蒸气反应生成 与水蒸气反应生成 |  漂白性强于 漂白性强于 |  具有漂白性 具有漂白性 |
| A.A | B.B | C.C | D.D |
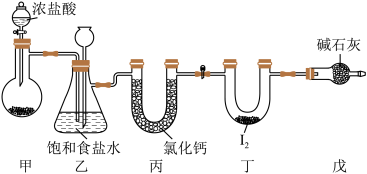
| A.利用装置甲应选用药品高锰酸钾和浓盐酸制氯气 |
| B.装置乙中长颈漏斗内液面上升说明丙装置可能发生堵塞 |
| C.可将装置丙中的药品氯化钙改为浓硫酸 |
| D.该反应说明氧化性Cl2>I2 |
7 . 下列实验的现象及相应的结论都正确的是
实验 | 现象 | 结论 | |
A | 向 溶液中滴入足量KI溶液,再加入 溶液中滴入足量KI溶液,再加入 振荡、静置 振荡、静置 | 下层液体呈紫红色 | 氧化性: |
B | 向某 |
|
|
C | 某溶液中加入 | 产生白色沉淀 | 溶液中一定含有 |
D | 用洁净铂丝蘸取某溶液进行焰色试验 | 火焰为黄色 | 溶液中无 |
| A.A | B.B | C.C | D.D |
 、NH
、NH 、Fe3+、H+和H2O六种粒子,测得Fe3+、NO
、Fe3+、H+和H2O六种粒子,测得Fe3+、NO 的质量分数(w)随时间变化的曲线如图所示,下列判断正确的是
的质量分数(w)随时间变化的曲线如图所示,下列判断正确的是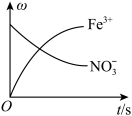
A.NO 发生氧化反应 发生氧化反应 | B.还原性:Fe2+>NH |
| C.还原剂与氧化剂的物质的量之比为1:8 | D.根据信息可知Fe(NO3)2溶液不宜加酸酸化 |
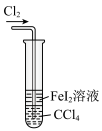 |  | 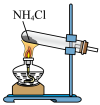 | 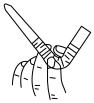 |
A.比较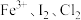 的氧化性强弱 的氧化性强弱 | B.配制一定物质的量浓度的硫酸 | C.实验室制取并收集 | D.为装有酸性 溶液的滴定管排气泡 溶液的滴定管排气泡 |
| A.A | B.B | C.C | D.D |
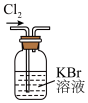
10 . 已知氧化性强弱顺序:Cl2>Br2>Fe3+>I2,则下列说法正确的是
| A.某溶液中含有Fe2+、Cl-、I-,为了除去I-而不减少其他离子,可加入适量Fe3+ |
| B.向FeBr2溶液中通入等物质的量Cl2,发生反应离子方程式为:2Br-+Cl2=Br2+2Cl- |
| C.Fe可以和I2在加热条件下生成FeI3 |
| D.向含有NaBr、NaI的溶液中通入适量氯气,充分作用后,将溶液蒸干、灼烧,可能得到NaCl和NaI的固体混合物 |

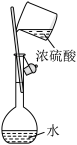







 中的
中的 杂质
杂质




 溶液中滴入酸性
溶液中滴入酸性 定为
定为
 溶液
溶液



