解题方法
1 . 综合利用粉煤灰既有利于环境保护,又有利于资源节约。某种粉煤灰(主要含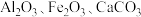 )的铝、铁分离工艺流程如下:
)的铝、铁分离工艺流程如下: 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
②提高浸出率的措施有_______ (写出一点即可)。
③当硫酸浓度大于 时,铝、铁的浸出率下降,可能的原因是
时,铝、铁的浸出率下降,可能的原因是_______ 。
(2)已知:部分氢氧化物开始沉淀和沉淀完全的 如下表所示。
如下表所示。
①“分离”过程中加入氨水调“浸出液” 的范围是
的范围是 ,其目的是
,其目的是_______ 。
②“浸出液”中加铁粉的作用是_______ 。
(3)燃煤烟气中 的捕集可通过如图所示的物质转化实现。
的捕集可通过如图所示的物质转化实现。 溶液与石灰乳反应的化学方程式为
溶液与石灰乳反应的化学方程式为_______ ,载人航天器内,常用 固体而很少用
固体而很少用 固体吸收空气中的
固体吸收空气中的 ,其原因是
,其原因是_______ 。
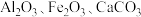 )的铝、铁分离工艺流程如下:
)的铝、铁分离工艺流程如下: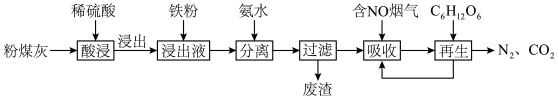
 发生反应的离子方程式为
发生反应的离子方程式为②提高浸出率的措施有
③当硫酸浓度大于
 时,铝、铁的浸出率下降,可能的原因是
时,铝、铁的浸出率下降,可能的原因是(2)已知:部分氢氧化物开始沉淀和沉淀完全的
 如下表所示。
如下表所示。| 氢氧化物 |  |  |  |
| 开始沉淀的pH | 1.5 | 3.2 | 7.1 |
| 沉淀完全的pH | 3.1 | 4.9 | 8.9 |
 的范围是
的范围是 ,其目的是
,其目的是②“浸出液”中加铁粉的作用是
(3)燃煤烟气中
 的捕集可通过如图所示的物质转化实现。
的捕集可通过如图所示的物质转化实现。
 溶液与石灰乳反应的化学方程式为
溶液与石灰乳反应的化学方程式为 固体而很少用
固体而很少用 固体吸收空气中的
固体吸收空气中的 ,其原因是
,其原因是
您最近半年使用:0次
名校
解题方法
2 . 某稀溶液中含有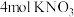 和
和 ,向其中加入
,向其中加入 ,充分反应(已知
,充分反应(已知 被还原为NO),最终溶液体积为
被还原为NO),最终溶液体积为 ,下列说法正确的是
,下列说法正确的是
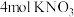 和
和 ,向其中加入
,向其中加入 ,充分反应(已知
,充分反应(已知 被还原为NO),最终溶液体积为
被还原为NO),最终溶液体积为 ,下列说法正确的是
,下列说法正确的是A.所得溶液中的溶质只有 、 、 |
B.所得溶液中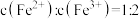 |
C.反应后生成NO的体积为 (标准状况下) (标准状况下) |
D.所得溶液中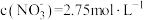 |
您最近半年使用:0次
解题方法
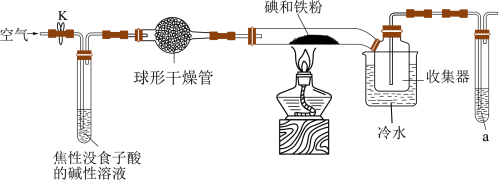
3 . 碘化亚铁( )在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收
)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收 )
)_______ ,若无此装置,写出铁粉参与的副反应的化学方程式:_______ ,硬质玻璃管中制备碘化亚铁的化学方程式为_______ 。
(2)硬质玻璃管直接接入收集器而不用导管的原因是_______ ,收集器浸泡在冷水中的原因是_______ 。
(3)试剂a的作用是_______ 。
(4)已知氧化性: 。往含
。往含 的溶液中通入
的溶液中通入 标准状况下的氯气,充分反应,请写出该反应的离子方程式:
标准状况下的氯气,充分反应,请写出该反应的离子方程式:_______ 。
 )在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收
)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收 )
)
(2)硬质玻璃管直接接入收集器而不用导管的原因是
(3)试剂a的作用是
(4)已知氧化性:
 。往含
。往含 的溶液中通入
的溶液中通入 标准状况下的氯气,充分反应,请写出该反应的离子方程式:
标准状况下的氯气,充分反应,请写出该反应的离子方程式:
您最近半年使用:0次
解题方法
4 . 根据下列实验操作和现象,所得到的结论不正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 检验铁锈中是否含有二价铁,将铁锈溶于浓盐酸,滴入 溶液,紫色褪去 溶液,紫色褪去 | 铁锈中含有二价铁 |
| B | 用醋酸浸泡水壶中的水垢,可将其清除 | 醋酸的酸性强于碳酸的酸性 |
| C | 将水蒸气通过灼热的铁粉,粉末变黑色 | 铁与水在高温下发生反应 |
| D | 取久置的氯水于试管中,加入几滴紫色石蕊溶液,溶液变为红色,且较长时间内不褪色 | 氯水已经完全变质 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
5 . 化学与生活、科技、社会发展息息相关。下列有关说法正确的是
| A.节日燃放烟花过程中产生焰色是化学变化 |
| B.太空探测器的结构材料大多采用高强度、高密度的不锈钢 |
C.擦干已洗净的铁锅,以防生锈变为 |
| D.食物腐败、金属的冶炼都与氧化还原反应有关 |
您最近半年使用:0次
解题方法
6 . 部分含铁物质的“价一类”关系如图所示。下列叙述错误的是
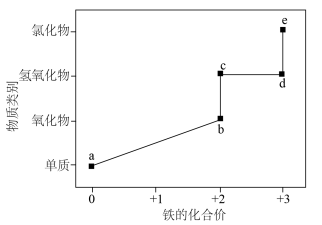
A. 的转化均能通过一步反应实现 的转化均能通过一步反应实现 | B.在沸水中滴加e的饱和溶液可制备d的胶体 |
C.在高温下a与水蒸气反应生成b和 | D.工业上,可用e溶液刻蚀铜电路板 |
您最近半年使用:0次
名校
解题方法
7 . 以硫铁矿(主要成分为 ,还有少量
,还有少量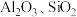 等杂质)为原料制备绿矾晶体
等杂质)为原料制备绿矾晶体 的工艺流程如图所示,下列说法错误的是
的工艺流程如图所示,下列说法错误的是
 ,还有少量
,还有少量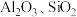 等杂质)为原料制备绿矾晶体
等杂质)为原料制备绿矾晶体 的工艺流程如图所示,下列说法错误的是
的工艺流程如图所示,下列说法错误的是
A.滤渣X的成分为 |
B.“焙烧”硫铁矿的主要反应中,还原剂与氧化剂的物质的量之比为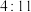 |
| C.“过滤”中分离操作所用的玻璃仪器有(普通)漏斗、玻璃棒和烧杯 |
D.“还原”中试剂Y可能为 |
您最近半年使用:0次
名校
解题方法
8 . NA为阿伏加德罗常数的值,下列有关叙述正确的是
| A.标准状况下,11.2L氖气中所含电子数为0.5NA |
B.32g环状S8( )分子中含有的 )分子中含有的 键的数目为NA 键的数目为NA |
C.常温常压下,3.6gD2O与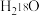 组成的体系中含有中子数2NA 组成的体系中含有中子数2NA |
D.某电池的总反应为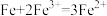 ,当有5.6gFe溶解时电路中有0.3NA电子通过 ,当有5.6gFe溶解时电路中有0.3NA电子通过 |
您最近半年使用:0次
解题方法
9 . 在一定条件下,不能由两种单质直接化合而生成的化合物是
| A.SO3 | B.Na2O2 | C.FeCl3 | D.Na2O |
您最近半年使用:0次
名校
10 . 下列物质的性质与用途的表述均正确且有对应关系的是
A. 两性,可用于制造耐高温陶瓷 两性,可用于制造耐高温陶瓷 |
| B.浓硝酸不与铁铝反应,可用铝制或铁制容器盛装浓硝酸 |
C. 具有还原性,可用作抗氧化剂添加到特定食品中 具有还原性,可用作抗氧化剂添加到特定食品中 |
D. 传输信号不衰减,可用做芯片 传输信号不衰减,可用做芯片 |
您最近半年使用:0次



