名校
1 . 哲学中“量变引起质变”规律广泛应用于化学反应。下列反应不符合这一规律的是
| A.铁和稀硝酸反应 | B.硫和铜在加热条件下反应 |
| C.碳酸钠与盐酸反应 | D.氯化铝溶液和氢氧化钠溶液反应 |
您最近半年使用:0次
名校
2 . 常温下,下列物质可用铁罐车装运的是
| A.浓硫酸 | B.浓盐酸 | C.稀硫酸 | D.稀硝酸 |
您最近半年使用:0次
名校
3 . 硝酸与金属的反应
①先将5.6克铁粉与200mL一定浓度的稀硝酸混合使其充分反应,固体完全溶解,并收集到气体VL(已折算为标准状况);
②往反应后的溶液中加入一定量铜粉,铜粉恰好完全溶解,且溶解过程中无气泡产生;
③继续往溶液中加入足量NaOH溶液并过滤,将滤渣充分加热后得共到12g固体X.
回答下列问题:
(1)①中产生的气体为______ ,其体积为______ (标况下),写出产生该气体的化学方程式______ 。
(2)铜粉的质量为______ 写出铜粉溶解的离子方程式______ 。
(3)固体X中主要成分的物质的量之比为______ 。
①先将5.6克铁粉与200mL一定浓度的稀硝酸混合使其充分反应,固体完全溶解,并收集到气体VL(已折算为标准状况);
②往反应后的溶液中加入一定量铜粉,铜粉恰好完全溶解,且溶解过程中无气泡产生;
③继续往溶液中加入足量NaOH溶液并过滤,将滤渣充分加热后得共到12g固体X.
回答下列问题:
(1)①中产生的气体为
(2)铜粉的质量为
(3)固体X中主要成分的物质的量之比为
您最近半年使用:0次
名校
4 .  表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是A.标准状况下,11.2L  ,溶于水,溶液中 ,溶于水,溶液中 和 和 的微粒数之和为0.5 的微粒数之和为0.5 |
B.常温常压下,28g  和CO混合气体所含的原子总数为2 和CO混合气体所含的原子总数为2 |
C.常温下,56g Fe与足量浓硫酸反应转移的电子数为3 |
D.25℃时,0.1 的 的 溶液中含有的 溶液中含有的 的总数为0.1 的总数为0.1 |
您最近半年使用:0次
名校
解题方法
5 . 下列化学方程式或离子方程式正确的是
A.少量 通入水玻璃中的反应: 通入水玻璃中的反应: |
B.用石英和焦炭制取粗硅: |
C.铁粉溶于过量稀硝酸: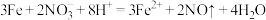 |
D.过量 通入 通入 溶液中: 溶液中: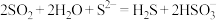 |
您最近半年使用:0次
名校
解题方法
6 . 下列离子方程式正确的是
A.铁与少量稀硝酸反应: |
B.通入 使酸性 使酸性 溶液褪色: 溶液褪色: |
C.向 溶液中加入过量的 溶液中加入过量的 溶液: 溶液: |
D.少量 通入 通入 溶液: 溶液: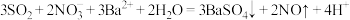 |
您最近半年使用:0次
7 . 能正确表示下列反应的离子方程式为
A.过量铁粉加入稀硝酸中:Fe+4H++NO =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
| B.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓ |
C.用Na2SO3溶液吸收少量Cl2:3SO +Cl2+H2O=2HSO +Cl2+H2O=2HSO +2Cl-+SO +2Cl-+SO |
D.同浓度同体积NH4HSO4溶液与NaOH溶液混合:NH +OH-=NH3•H2O +OH-=NH3•H2O |
您最近半年使用:0次
名校
解题方法
8 . 向100mL稀硫酸和稀硝酸的混合溶液中缓慢加入铁粉,产生气体的物质的量与铁粉质量的关系如下图所示(已知硝酸只被还原为NO)。下列有关判断正确的是
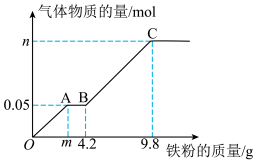

| A.m的值为3.5 |
B.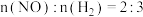 |
| C.B点溶液中溶质只含FeSO4 |
D.原混合溶液中 |
您最近半年使用:0次
名校
解题方法
9 . 下列说法正确的是
| A.苏打可以治疗胃酸过多 | B.氧化铝可用作耐火材料 |
| C.常温下铁片与浓硫酸不反应 | D.单质铜和单质硫混合加热生成CuS |
您最近半年使用:0次
名校
10 . 将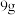 铜和铁的混合物投入
铜和铁的混合物投入 稀硝酸中,充分反应后得到标准状况下
稀硝酸中,充分反应后得到标准状况下 ,剩余
,剩余 金属;继续加入
金属;继续加入 等浓度的稀硝酸,金属完全溶解,又得到标准状况下
等浓度的稀硝酸,金属完全溶解,又得到标准状况下 。若向反应后的溶液中加入
。若向反应后的溶液中加入 溶液,溶液不变红,则下列说法不正确的是
溶液,溶液不变红,则下列说法不正确的是
A.原混合物中铜和铁各 |
B.稀硝酸的物质的量浓度为 |
C.第一次剩余的 金属为铜 金属为铜 |
D.向反应后的溶液中再加入该稀硝酸 ,又得到标准状况下的 ,又得到标准状况下的 |
您最近半年使用:0次



