2024届天津市十二区重点学校高三下学期毕业班联考二模化学试题
天津
高三
二模
2024-05-14
286次
整体难度:
适中
考查范围:
化学反应原理、有机化学基础、认识化学科学、物质结构与性质、常见无机物及其应用、化学实验基础、化学与STSE
2024届天津市十二区重点学校高三下学期毕业班联考二模化学试题
天津
高三
二模
2024-05-14
286次
整体难度:
适中
考查范围:
化学反应原理、有机化学基础、认识化学科学、物质结构与性质、常见无机物及其应用、化学实验基础、化学与STSE
一、单选题 添加题型下试题
单选题
|
容易(0.94)
解题方法
2. 下列化学用语或图示表达正确的是
A. 的结构式:Cl﹣S﹣S﹣Cl 的结构式:Cl﹣S﹣S﹣Cl |
B.中子数为18的氯原子: |
C.四氯化碳分子的空间填充模型: |
D.顺-2-丁烯的结构简式: |
您最近一年使用:0次
单选题
|
适中(0.65)
3. 化学处处呈现美。下列说法不正确的是
| A.雪花是天空中的水汽经凝华而来的一种晶体,其六角形形状与氢键的方向性有关 |
B. 与18-冠-6的空腔大小相近,形成稳定的超分子结构( 与18-冠-6的空腔大小相近,形成稳定的超分子结构(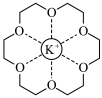 ),这体现出超分子的自组装特征 ),这体现出超分子的自组装特征 |
| C.缺角的NaCl晶体在饱和NaCl溶液中变为完美立方体块,体现晶体的自范性 |
| D.绚烂烟花的产生是电子由较高能量的激发态跃迁到较低能量的激发态乃至基态时,能量以光的形式释放引起的 |
【知识点】 氢键对物质性质的影响解读 晶体类型判断解读
您最近一年使用:0次
4. 下列物质的性质与用途对应关系错误的是
| A.聚合硫酸铁铝能水解形成胶体,可用作净水剂 |
| B.钠钾合金导热能力特别强,可用作原子反应堆的导热剂 |
| C.聚四氟乙烯具有抗酸碱、自润滑等性能,可用于制作滴定管活塞 |
| D.乙二醇水溶液凝固点很高,可作汽车发动机的抗冻剂 |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 已知咖啡酸苯乙酯是天然抗癌药一一蜂胶的主要活性成分,其结构简式如图所示。下列正确的是

| A.该物质含存在1个手性碳原子 |
B.1mol该物质最多能与 加成 加成 |
| C.该物质苯环上氢原子发生氯代时,一氯代物有6种 |
| D.该物质所有碳原子不可能全部共平面 |
【知识点】 含有酚羟基的物质性质的推断解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 下列实验能达到实验目的且操作正确的是
A.制备 ,并能较长时间观察到沉淀颜色 ,并能较长时间观察到沉淀颜色 | B.排出盛有 溶液滴定管尖嘴内的气泡 溶液滴定管尖嘴内的气泡 |
|
|
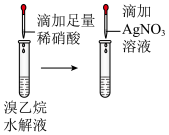
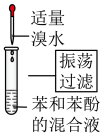
C.检验溴乙烷水解产物含有 | D.除去苯中少量苯酚 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
7. 磷酸氢二铵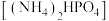 常用作干粉灭火剂,可用磷酸吸收氨气制备。设
常用作干粉灭火剂,可用磷酸吸收氨气制备。设 为阿伏加德罗常数的值,下列叙述错误的是
为阿伏加德罗常数的值,下列叙述错误的是
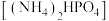 常用作干粉灭火剂,可用磷酸吸收氨气制备。设
常用作干粉灭火剂,可用磷酸吸收氨气制备。设 为阿伏加德罗常数的值,下列叙述错误的是
为阿伏加德罗常数的值,下列叙述错误的是A. 晶体中含有的离子总数为 晶体中含有的离子总数为 |
B.标准状况下,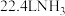 中含有的电子数为 中含有的电子数为 |
C.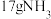 中含有的共价键数目为 中含有的共价键数目为 |
D.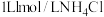 溶液中含有的阳离子数目小于 溶液中含有的阳离子数目小于 |
您最近一年使用:0次
单选题
|
适中(0.65)
8. 下列离子方程式或电极反应式书写不正确的是
A.CaS与浓硝酸反应: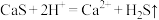 |
B.用硫化亚铁除去废水中的汞离子: |
C.泡沫灭火器的反应原理是: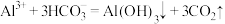 |
D. 溶液与过量 溶液与过量 反应: 反应: |
您最近一年使用:0次
单选题
|
适中(0.65)
9. 部分含N物质及含S物质的分类与相应化合价之间的关系如图所示,下列推断正确的是

| A.c'和d'分子中硫原子的杂化方式不相同 |
| B.c'通入到紫色石蕊溶液中,溶液褪色 |
| C.用两根玻璃棒分别蘸取浓的a溶液和浓的e'溶液,将两根玻璃棒靠近时有白烟产生 |
| D.常温下,可以用铁或铝制容器来盛装浓的e或e'溶液 |
【知识点】 利用杂化轨道理论判断化学键杂化类型解读
您最近一年使用:0次
单选题
|
适中(0.65)
10. 反应 可用于去除氮氧化物。
可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法不正确的是
催化该反应的过程如图所示。下列说法不正确的是
 可用于去除氮氧化物。
可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法不正确的是
催化该反应的过程如图所示。下列说法不正确的是
A.反应过程中, 参与反应,降低了反应的焓变 参与反应,降低了反应的焓变 |
B.该反应的平衡常数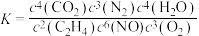 |
C.其他条件不变时,增大 ,NO的平衡转化率增大 ,NO的平衡转化率增大 |
D.步骤Ⅲ中每消耗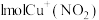 ,转移电子数目为 ,转移电子数目为 |
您最近一年使用:0次
单选题
|
适中(0.65)
11. 下列实验操作、现象或结论不正确的是
| 实验操作 | 现象 | 结论 | |
| A | 灼烧铜丝使其表面变黑,伸入盛有某有机物的试管中 | 铜丝恢复亮红色 | 该有机物中可能有醇羟基或羧基 |
| B | 常温下,分别测 的 的 和 和 溶液的 溶液的 | 两者的 之和等于14 之和等于14 | 常温下同浓度的 和 和 的电离程度相同 的电离程度相同 |
| C | 将熟石灰与 晶体在小烧杯中混合,滴入几滴水,搅拌 晶体在小烧杯中混合,滴入几滴水,搅拌 | 烧杯壁变凉 | 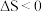 |
| D | 向两支盛有 溶液的试管中分别滴加淀粉溶液和 溶液的试管中分别滴加淀粉溶液和 溶液 溶液 | 前者溶液变蓝,后者有黄色沉淀生成 |  溶液中存在平衡: 溶液中存在平衡: |
| A.A | B.B | C.C | D.D |
【知识点】 熵判据解读 弱电解质在水溶液中的电离平衡解读
您最近一年使用:0次
单选题
|
较难(0.4)
12. 室温下,将 溶液与过量
溶液与过量 固体混合,溶液
固体混合,溶液 随时间变化如图所示。
随时间变化如图所示。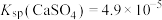
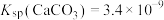
下列说法不正确的是
 溶液与过量
溶液与过量 固体混合,溶液
固体混合,溶液 随时间变化如图所示。
随时间变化如图所示。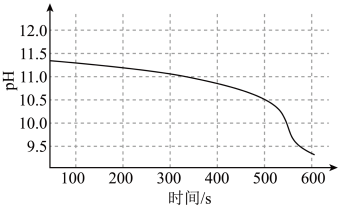
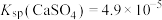
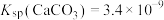
下列说法不正确的是
A.两者混合发生反应: |
B.随着反应的进行, 逆向移动,溶液 逆向移动,溶液 下降 下降 |
C.充分反应后上层清液中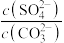 约为 约为 |
D.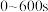 内上层清液中存在: 内上层清液中存在: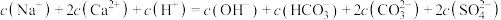 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-结构与性质
|
适中(0.65)
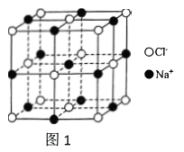
13. Ⅰ.氯化钠是一种典型且极具魅力的晶体,我们通过学习氯化钠可以更好地了解其他类似物质的结构。已知氯化钠的晶胞如图1所示。___________ 。
(2)已知NaCl的密度为 ,NaCl的摩尔质量为
,NaCl的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则在NaCl晶体里
,则在NaCl晶体里 和
和 的最短距离为
的最短距离为___________ pm。
(3)下列关于氯化钠的说法不正确的是___________。
(4)用离子方程式表示氯碱工业反应原理___________ 。
Ⅱ.我国某研究所于2022年研制出一种新型离子液体[CPMIm]Cl(如图2)可弥补该电池表面的 和
和 缺陷,进一步提高该电池的性能。
缺陷,进一步提高该电池的性能。___________ (填选项字母)。
A.离子键 B.共价键 C.氢键
(6)离子液体[CPMIm]Cl中不同杂化方式的碳原子个数比: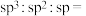
___________ 。
(7)相较于传统液态有机溶剂,该离子液体具有难挥发的优点,原因是:___________ 。
(2)已知NaCl的密度为
 ,NaCl的摩尔质量为
,NaCl的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则在NaCl晶体里
,则在NaCl晶体里 和
和 的最短距离为
的最短距离为(3)下列关于氯化钠的说法不正确的是___________。
A.基态 的电子有5种空间运动状态 的电子有5种空间运动状态 |
B.第三周期离子半径最大的是 |
C.第三电离能大小: |
| D.每个氯离子周围与它最近且等距的氯离子有12个 |
Ⅱ.我国某研究所于2022年研制出一种新型离子液体[CPMIm]Cl(如图2)可弥补该电池表面的
 和
和 缺陷,进一步提高该电池的性能。
缺陷,进一步提高该电池的性能。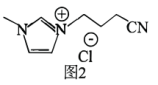
A.离子键 B.共价键 C.氢键
(6)离子液体[CPMIm]Cl中不同杂化方式的碳原子个数比:
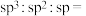
(7)相较于传统液态有机溶剂,该离子液体具有难挥发的优点,原因是:
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
14. 化合物G俗称依普黄酮,是一种抗骨质疏松药物的主要成分。以甲苯为原料合成该化合物的路线如下图所示:___________ 。
(2)H的名称为___________ 。
(3)G中含氧官能团的名称为___________ ,反应B→C的反应类型为___________ 。
(4)F与足量的 完全加成后所生成的化合物中手性碳原子的个数为
完全加成后所生成的化合物中手性碳原子的个数为___________ 。
(5)N的同分异构体中既能发生银镜反应又能发生水解反应的共有___________ 种。请写出其中核磁共振氢谱有五组峰的有机物在加热条件下,和足量的盐酸发生水解反应的化学方程式:___________ 。
(6)根据上述信息,设计以苯酚和为 原料,制备
原料,制备 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)___________ 。

已知:
(2)H的名称为
(3)G中含氧官能团的名称为
(4)F与足量的
 完全加成后所生成的化合物中手性碳原子的个数为
完全加成后所生成的化合物中手性碳原子的个数为(5)N的同分异构体中既能发生银镜反应又能发生水解反应的共有
(6)根据上述信息,设计以苯酚和为
 原料,制备
原料,制备 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
解题方法
15. 某化学小组设计如图1所示实验装置制备硝酸并探究其性质。
Ⅰ.硝酸的制备:___________ (填“图2”或“图3")。
(2)装置b中Na2O2的作用是___________ 。
Ⅱ.硝酸的性质探究:
(3)常温下,同学甲在硝酸的制备实验结束后,用pH计测得装置e中溶液的pH=1.00。同学乙做同样实验,测得溶液的pH=6.00,可能的原因是___________ 。
(4)用图4装置进行硝酸与铜的反应。某实验小组在研究硝酸与铜的反应时,发现稀硝酸和铜反应后的混合液为蓝色,而浓硝酸和铜反应后的混合液为绿色,对产生绿色的原因开展探究。
①甲同学推测溶液显绿色的原因是NO2在溶液中达到饱和,NO2的饱和溶液呈黄色,硝酸铜稀溶液呈蓝色,两者混合后呈绿色。甲同学取少量该绿色溶液,向其中加入适量水后溶液变为蓝色,可能的原因是___________ (用化学方程式表示)。
②乙同学认为甲同学所做实验不足以支撑他的推测,还有可能是___________ 。
③丙同学进一步探究反应后溶液呈绿色是否与NO2的溶解有关,设计实验:用不同气体将反应后溶液中的NO2赶出,观察并分析现象。实验记录如下:
注:实验过程中气体流速均已保持一致
实验2 不能将大理石与稀盐酸反应产生的气体直接通入溶液中,请说明原因:___________ 。该实验说明反应后的溶液呈绿色的主要原因___________ (填“是”或“不是”) NO2的溶解所导致的。
(5)丁同学结合上述实验继续推测溶液显绿色源于铜的亚硝酸化合物,铜和浓硝酸的反应过程中,还生成了亚硝酸,进而与Cu2+结合形成绿色物质。资料显示 为绿色。
为绿色。
①查阅资料后发现尿素 可以和亚硝酸发生反应但不会影响NO2的生成,在与亚硝酸的反应中可生成两种无污染的气体,其化学方程式为
可以和亚硝酸发生反应但不会影响NO2的生成,在与亚硝酸的反应中可生成两种无污染的气体,其化学方程式为___________ 。
②丙同学往反应结束后的试管中加入一勺尿素,溶液立刻恢复蓝色。随后小组成员又做了补充实验:在铜和浓硝酸反应开始前,提前加入一定量的尿素,反应现象变为___________ ,则说明丁同学的推测具有一定科学性。
Ⅰ.硝酸的制备:

(2)装置b中Na2O2的作用是
Ⅱ.硝酸的性质探究:
(3)常温下,同学甲在硝酸的制备实验结束后,用pH计测得装置e中溶液的pH=1.00。同学乙做同样实验,测得溶液的pH=6.00,可能的原因是
(4)用图4装置进行硝酸与铜的反应。某实验小组在研究硝酸与铜的反应时,发现稀硝酸和铜反应后的混合液为蓝色,而浓硝酸和铜反应后的混合液为绿色,对产生绿色的原因开展探究。
①甲同学推测溶液显绿色的原因是NO2在溶液中达到饱和,NO2的饱和溶液呈黄色,硝酸铜稀溶液呈蓝色,两者混合后呈绿色。甲同学取少量该绿色溶液,向其中加入适量水后溶液变为蓝色,可能的原因是
②乙同学认为甲同学所做实验不足以支撑他的推测,还有可能是
③丙同学进一步探究反应后溶液呈绿色是否与NO2的溶解有关,设计实验:用不同气体将反应后溶液中的NO2赶出,观察并分析现象。实验记录如下:
注:实验过程中气体流速均已保持一致
| 实验编号 | 1 | 2 | 3 |
| 通入气体 | N2 | CO2 | O2 |
| 实现现象 | 大量红棕色气体逸出,约25min后溶液变为蓝色 | 大量红棕色气体逸出,约25min后溶液变为蓝色 | 大量红棕色气体逸出,约5min后溶液变为蓝色 |
(5)丁同学结合上述实验继续推测溶液显绿色源于铜的亚硝酸化合物,铜和浓硝酸的反应过程中,还生成了亚硝酸,进而与Cu2+结合形成绿色物质。资料显示
 为绿色。
为绿色。①查阅资料后发现尿素
 可以和亚硝酸发生反应但不会影响NO2的生成,在与亚硝酸的反应中可生成两种无污染的气体,其化学方程式为
可以和亚硝酸发生反应但不会影响NO2的生成,在与亚硝酸的反应中可生成两种无污染的气体,其化学方程式为②丙同学往反应结束后的试管中加入一勺尿素,溶液立刻恢复蓝色。随后小组成员又做了补充实验:在铜和浓硝酸反应开始前,提前加入一定量的尿素,反应现象变为
您最近一年使用:0次
解答题-原理综合题
|
较难(0.4)
16. 合成氨工业对国民经济和社会发展具有重要的意义,工业合成氮的流程如下:
(1)步骤①中需对原料气进行净化,目的是___________ 。
(2)下列说法正确的是___________。
(3) 过渡金属复合催化剂可用于催化合成氨,已知
过渡金属复合催化剂可用于催化合成氨,已知 被吸附发生反应
被吸附发生反应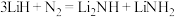 ,用一个化学方程式表示
,用一个化学方程式表示 被吸附发生的反应
被吸附发生的反应___________ 。
(4)早在二十世纪初,工业上以 和
和 为原料在一定温度和压强下合成尿素。反应分两步:
为原料在一定温度和压强下合成尿素。反应分两步:
Ⅰ.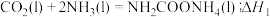
Ⅱ.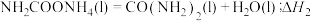
①
___________  (用图中字母表示)。
(用图中字母表示)。___________ (填“Ⅰ”或“Ⅱ”)。
(5)实验室利用以下装置模拟了硝酸盐还原为氨的反应,总反应为: 。
。___________ 。
②每产生11.2L (标准状况),B区溶液质量减少
(标准状况),B区溶液质量减少___________ 克。
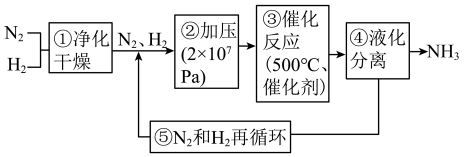
(1)步骤①中需对原料气进行净化,目的是
(2)下列说法正确的是___________。
A.步骤①除原料气中CO反应: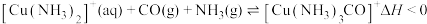 ,适宜低温高压环境 ,适宜低温高压环境 |
| B.步骤②“加压”可以加快反应速率,但压强过高,氨的产率会降低 |
| C.步骤③500℃左右比室温更有利于合成氨的反应,提高氨气的产率 |
| D.步骤④⑤有利于提高原料的利用率,能节约生产成本 |
(3)
 过渡金属复合催化剂可用于催化合成氨,已知
过渡金属复合催化剂可用于催化合成氨,已知 被吸附发生反应
被吸附发生反应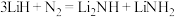 ,用一个化学方程式表示
,用一个化学方程式表示 被吸附发生的反应
被吸附发生的反应(4)早在二十世纪初,工业上以
 和
和 为原料在一定温度和压强下合成尿素。反应分两步:
为原料在一定温度和压强下合成尿素。反应分两步:Ⅰ.
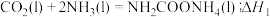
Ⅱ.
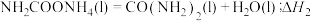
①

 (用图中字母表示)。
(用图中字母表示)。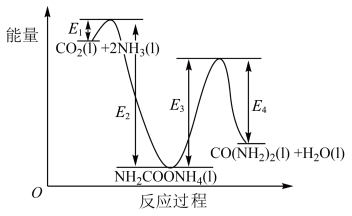
(5)实验室利用以下装置模拟了硝酸盐还原为氨的反应,总反应为:
 。
。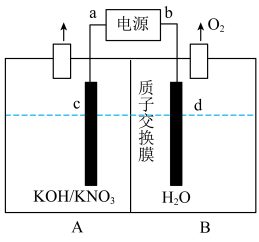
②每产生11.2L
 (标准状况),B区溶液质量减少
(标准状况),B区溶液质量减少
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学反应原理、有机化学基础、认识化学科学、物质结构与性质、常见无机物及其应用、化学实验基础、化学与STSE
试卷题型(共 16题)
题型
数量
单选题
12
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 金属的防护 蛋白质的变性 | |
| 2 | 0.94 | 化学用语综合判断 有机物的结构式、结构简式、比例模型、球棍模型、最简式 烯烃的顺反异构 原子中相关数值及其之间的相互关系 | |
| 3 | 0.65 | 氢键对物质性质的影响 晶体类型判断 | |
| 4 | 0.65 | 明矾的净水作用及原理 醇类的物理性质 常用仪器及使用 金属与合金性能比较 | |
| 5 | 0.65 | 含有酚羟基的物质性质的推断 | |
| 6 | 0.65 | 酸碱中和滴定实验相关仪器 卤代烃中卤素原子的检验 苯酚与溴水的反应 化学实验方案的设计与评价 | |
| 7 | 0.65 | 阿伏加德罗常数的应用 22.4L/mol适用条件 物质的量有关计算 盐类水解的原理 | |
| 8 | 0.65 | 离子方程式的正误判断 硝酸的强氧化性 盐类双水解反应 沉淀转化 | |
| 9 | 0.65 | 利用杂化轨道理论判断化学键杂化类型 | |
| 10 | 0.65 | 化学平衡常数的概念及表达方式 转化率的相关计算及判断 | |
| 11 | 0.65 | 熵判据 弱电解质在水溶液中的电离平衡 | |
| 12 | 0.4 | 盐溶液中离子浓度大小的比较 浓度对难溶电解质溶解平衡的影响 溶度积常数相关计算 | |
| 二、解答题 | |||
| 13 | 0.65 | 电离能变化规律 利用杂化轨道理论判断分子的空间构型 简单配合物的成键 晶胞的有关计算 | 结构与性质 |
| 14 | 0.4 | 苯的同系物的卤代反应 根据题给物质选择合适合成路线 有机合成综合考查 酰胺的性质与应用 | 有机推断题 |
| 15 | 0.65 | 二氧化氮与水反应 配合物的概念、组成及形成条件 物质性质实验方案的设计 铜的化合物的制备 | 实验探究题 |
| 16 | 0.4 | 氮气 化学反应热的计算 化学平衡的移动及其影响因素 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |