1 . A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B元素原子最外层电子数比次外层多2;A、B两元素的核电荷数之差等于它们的原子最外层电子数之和;D和E的原子序数和为30;在元素周期表中,C是E的不同周期邻族元素。五种元素两两形成的化合物有甲、乙、两、丁四种分子中原子个数比如下表:
(1)写出元素符号:B___________ ,E___________ 。
(2)A元素某原子核内中子数比质子数多1,则该核素的组成符号为___________ 。物质丁的分子为___________ 分子(填“极性”或“非极性”)。
(3)向甲的水溶液中加入MnO2,氧化产物是___________ 。
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会产生大量气体和难溶物,有关离子方程式为___________ 。
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中各元素原子个比 | A∶C=1∶1 | B∶A=1∶2 | D∶E=1∶3 | B∶E=1∶4 |
(1)写出元素符号:B
(2)A元素某原子核内中子数比质子数多1,则该核素的组成符号为
(3)向甲的水溶液中加入MnO2,氧化产物是
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会产生大量气体和难溶物,有关离子方程式为
您最近半年使用:0次
解题方法
2 . 下列各组离子在指定溶液中一定能大量共存的是
A.在 的溶液中: 的溶液中: 、 、 、 、 、CO 、CO |
B.使甲基橙变红的溶液中: 、 、 、 、 、 、 |
C.透明溶液中: 、 、 、 、 、 、 |
D.常温下,水电离出的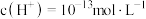 溶液中: 溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
3 . 室温下,探究0.1 mol·L-1 FeCl3溶液的性质,下列实验方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向两支试管中分别加入5 mL 5%的H2O2溶液,再向两支试管中滴入3滴浓度均为0.1 mol·L-1 的FeCl3和CuSO4,观察产生气体的速率 | 比较Fe3+和Cu2+的催化效率 |
| B | 向2 mL 0.1 mol·L-1 FeCl3溶液中加入1 mL 0.1 mol·L-1 KI溶液,充分振荡后滴加KSCN溶液,观察颜色变化 | 2Fe3++2I-=2Fe2++I2是否为可逆反应 |
| C | 向苯酚溶液中滴加几滴0.1 mol·L-1 FeCl3溶液,溶液呈紫色 | FeCl3与苯酚发生了氧化还原反应 |
| D | 将5 mL 0.1 mol·L-1 FeCl3溶液和15 mL 0.1 mol·L-1 NaHCO3溶液混合,生成红褐色沉淀和气体 | Fe3+与 发生了双水解反应 发生了双水解反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
4 . 下列有关铁及其化合物的实验方案,对应的现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 将红热的铁与水蒸气在高温条件下反应,反应结束后,将磁铁靠近产物 | 反应结束后有黑色固体生成,且该固体被磁铁吸引 | 铁与水蒸气在高温下反应,生成Fe3O4 |
| B | 取5mLFeCl3溶液于试管中,逐滴加入Na2SO3溶液至过量。再加入过量稀盐酸和BaCl2溶液 | 加入稀盐酸前,溶液由黄色变为红棕色。加入稀盐酸和BaCl2溶液后产生白色沉淀 | Fe3+和 既发生氧化还原反应,也发生双水解 既发生氧化还原反应,也发生双水解 |
| C | 为了验证Fe2+的还原性,取FeCl2溶液于试管中,加入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液紫色褪去 | Fe2+具有还原性 |
| D | 向少量蒸馏水的试管里滴加2滴K3[Fe(CN)6]溶液,然后再滴加2滴硫氰化钾溶液 | 溶液变血红色 | CN-与Fe3+的配位能力小于SCN- |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
5 . a、b、c、d四种短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示.下列说法正确的是
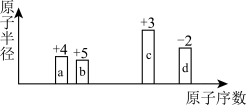
| A.离子半径的大小顺序:b<c<d | B.简单氢化物的沸点:d>b>a |
| C.b、d的氢化物可化合生成离子化合物 | D.分别含c3+与d2-的盐溶液相混会生成c2d3沉淀 |
您最近半年使用:0次
名校
解题方法
6 . 下列各组离子在溶液中可以大量共存的是
A.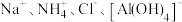 | B. |
C.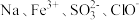 | D.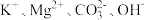 |
您最近半年使用:0次
解题方法
7 . 常温下,下列各组离子在相应条件下可能大量共存的是
A.水电离出来的c(H+)<10-7mol/L的溶液中:Cl-、K+、 、S2- 、S2- |
B.遇甲基橙变红色的溶液中: 、Na+、Cl-、 、Na+、Cl-、 |
C.含Al3+的溶液中:K+、Na+、Cl-、 |
D.透明中性溶液中:Fe3+、 、 、 、Cl- 、Cl- |
您最近半年使用:0次
解题方法
8 . I. 溶液可用于多种气体的处理。
溶液可用于多种气体的处理。
(1) 是温室气体,可用
是温室气体,可用 溶液吸收得到
溶液吸收得到 或
或 。
。
① 俗称纯碱,已知25℃时,
俗称纯碱,已知25℃时, 第一步水解的平衡常数
第一步水解的平衡常数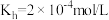 ,当溶液中
,当溶液中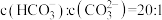 时,溶液的
时,溶液的
_______ 。
②泡沫灭火器中通常装有 溶液和
溶液和 溶液,请写出这两种溶液混合反应时的离子方程式
溶液,请写出这两种溶液混合反应时的离子方程式_______ 。
(2)金属与浓硝酸反应产生的 可用
可用 溶液吸收,反应方程式为:
溶液吸收,反应方程式为: ,含
,含 的水溶液与
的水溶液与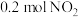 恰好完全反应得
恰好完全反应得 溶液A,溶液B为
溶液A,溶液B为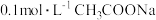 溶液,则两份溶液中
溶液,则两份溶液中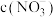 、
、 和
和 由大到小的顺序为
由大到小的顺序为_______ 。(已知 的电离常数
的电离常数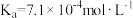 ,
, 的电离常数
的电离常数 )。
)。
(3)直接排放含 的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的
的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的 。吸收液吸收
。吸收液吸收 的过程中,
的过程中, 随
随 变化关系如下表所示:
变化关系如下表所示:
 溶液中溶液离子浓度关系正确的是(选填字母)
溶液中溶液离子浓度关系正确的是(选填字母)_______ 。
a.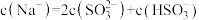
b.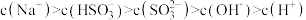
c.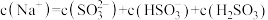
d.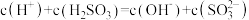
Ⅱ.滴定是一种重要的定量实验方法:某实验小组为测定碱式碳酸铜的纯度,取制得的碱式碳酸铜产品5.0g,加适量硫酸,再加 水,加热溶解,冷却后配成
水,加热溶解,冷却后配成 溶液,量取配成的
溶液,量取配成的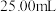 溶液于碘量瓶中,加入适量缓冲溶液控制溶液的
溶液于碘量瓶中,加入适量缓冲溶液控制溶液的 在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用
在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用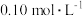 的
的 溶液进行滴定,至临近滴定终点时再加入
溶液进行滴定,至临近滴定终点时再加入 淀粉溶液做指示剂,继续滴入
淀粉溶液做指示剂,继续滴入 溶液至滴定终点。平行测定3次,实验数据如下表所示。
溶液至滴定终点。平行测定3次,实验数据如下表所示。
已知: ,
, 。
。
(4)判断滴定到达终 溶液点的现象是
溶液点的现象是_______ 。
(5)经数据处理可得该实验中滴定所用标准溶液的体积为_______  。
。
(6)下列操作会导致测定结果偏高的是_______ 。
a.装Na2S2O3溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失
b.锥形瓶未用待测液润洗
c.读 溶液体积时,若滴定前仰视,滴定后俯视
溶液体积时,若滴定前仰视,滴定后俯视
d.滴定过程中使用的碱式滴定管未润洗就装标准液滴定
 溶液可用于多种气体的处理。
溶液可用于多种气体的处理。(1)
 是温室气体,可用
是温室气体,可用 溶液吸收得到
溶液吸收得到 或
或 。
。①
 俗称纯碱,已知25℃时,
俗称纯碱,已知25℃时, 第一步水解的平衡常数
第一步水解的平衡常数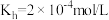 ,当溶液中
,当溶液中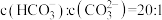 时,溶液的
时,溶液的
②泡沫灭火器中通常装有
 溶液和
溶液和 溶液,请写出这两种溶液混合反应时的离子方程式
溶液,请写出这两种溶液混合反应时的离子方程式(2)金属与浓硝酸反应产生的
 可用
可用 溶液吸收,反应方程式为:
溶液吸收,反应方程式为: ,含
,含 的水溶液与
的水溶液与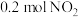 恰好完全反应得
恰好完全反应得 溶液A,溶液B为
溶液A,溶液B为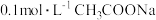 溶液,则两份溶液中
溶液,则两份溶液中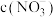 、
、 和
和 由大到小的顺序为
由大到小的顺序为 的电离常数
的电离常数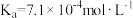 ,
, 的电离常数
的电离常数 )。
)。(3)直接排放含
 的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的
的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的 。吸收液吸收
。吸收液吸收 的过程中,
的过程中, 随
随 变化关系如下表所示:
变化关系如下表所示: | 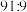 |  |  |
 | 8.2 | 7.2 | 6.2 |
 溶液中溶液离子浓度关系正确的是(选填字母)
溶液中溶液离子浓度关系正确的是(选填字母)a.
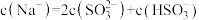
b.
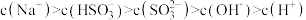
c.
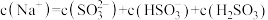
d.
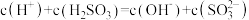
Ⅱ.滴定是一种重要的定量实验方法:某实验小组为测定碱式碳酸铜的纯度,取制得的碱式碳酸铜产品5.0g,加适量硫酸,再加
 水,加热溶解,冷却后配成
水,加热溶解,冷却后配成 溶液,量取配成的
溶液,量取配成的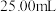 溶液于碘量瓶中,加入适量缓冲溶液控制溶液的
溶液于碘量瓶中,加入适量缓冲溶液控制溶液的 在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用
在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用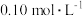 的
的 溶液进行滴定,至临近滴定终点时再加入
溶液进行滴定,至临近滴定终点时再加入 淀粉溶液做指示剂,继续滴入
淀粉溶液做指示剂,继续滴入 溶液至滴定终点。平行测定3次,实验数据如下表所示。
溶液至滴定终点。平行测定3次,实验数据如下表所示。已知:
 ,
, 。
。| 实验编号 | 滴定前 溶液的体积读数/ 溶液的体积读数/ | 滴定后 溶液的体积读数/ 溶液的体积读数/ |
| 1 | 0.10 | 20.12 |
| 2 | 1.20 | 23.21 |
| 3 | 1.50 | 21.48 |
 溶液点的现象是
溶液点的现象是(5)经数据处理可得该实验中滴定所用标准溶液的体积为
 。
。(6)下列操作会导致测定结果偏高的是
a.装Na2S2O3溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失
b.锥形瓶未用待测液润洗
c.读
 溶液体积时,若滴定前仰视,滴定后俯视
溶液体积时,若滴定前仰视,滴定后俯视d.滴定过程中使用的碱式滴定管未润洗就装标准液滴定
您最近半年使用:0次
9 . 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在新制饱和氯水中: 、 、 、 、 、 、 |
B.在能使酚酞变红的溶液中: 、 、 、 、 、 、 |
C.在加入铝粉能产生 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.在 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
解题方法
10 . 常温下,下列各组离子在指定条件下可能大量共存的是
A.含有Al3+的溶液中: |
B. 的溶液中: 的溶液中: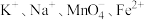 |
C.澄清透明的溶液中: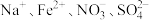 |
D.水电离出的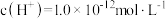 的溶液中: 的溶液中: |
您最近半年使用:0次



