名校
1 . 下列气体中,不能用浓硫酸干燥的是
A. | B. | C. | D. |
您最近半年使用:0次
2 . 研究氮的循环和转化对生产,生活有重要的价值。
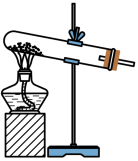
(1)写出用如图所示装置进行实验室制备氨气的化学方程式___________ 。___________ ;___________ 。
②设备2中通入的物质A是___________ 。
(3)氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以 和
和 的形式存在。某工厂处理氨氮废水的流程如图:
的形式存在。某工厂处理氨氮废水的流程如图:
含 的废水
的废水 低浓度氨氮废水
低浓度氨氮废水 含余氯废水
含余氯废水 达标
达标
①过程①的目的是将 转化为
转化为 ,并通过鼓入大量空气将氨气吹出,写出
,并通过鼓入大量空气将氨气吹出,写出 转化为
转化为 的离子方程式
的离子方程式___________ 。
②过程②加入 溶液可将氨氮物质转化为无毒物质氮气,请用离子方程式表示该转化过程
溶液可将氨氮物质转化为无毒物质氮气,请用离子方程式表示该转化过程___________ 。
③含余氯废水的主要成分是 以及
以及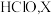 可选用以下哪种溶液以达到将余氯转化为无毒物质的目的
可选用以下哪种溶液以达到将余氯转化为无毒物质的目的___________ (填字母)。
a. b.
b. c.
c. d.
d.
写出其中一个反应的离子方程式:___________ 。
(4) 是燃油汽车尾气中的主要污染物之一、在催化剂和加热条件下,
是燃油汽车尾气中的主要污染物之一、在催化剂和加热条件下, 与
与 可反应生成无害物质,请写出反应的化学方程式
可反应生成无害物质,请写出反应的化学方程式___________ 。
(1)写出用如图所示装置进行实验室制备氨气的化学方程式
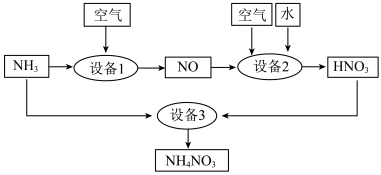
②设备2中通入的物质A是
(3)氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以
 和
和 的形式存在。某工厂处理氨氮废水的流程如图:
的形式存在。某工厂处理氨氮废水的流程如图:含
 的废水
的废水 低浓度氨氮废水
低浓度氨氮废水 含余氯废水
含余氯废水 达标
达标①过程①的目的是将
 转化为
转化为 ,并通过鼓入大量空气将氨气吹出,写出
,并通过鼓入大量空气将氨气吹出,写出 转化为
转化为 的离子方程式
的离子方程式②过程②加入
 溶液可将氨氮物质转化为无毒物质氮气,请用离子方程式表示该转化过程
溶液可将氨氮物质转化为无毒物质氮气,请用离子方程式表示该转化过程③含余氯废水的主要成分是
 以及
以及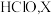 可选用以下哪种溶液以达到将余氯转化为无毒物质的目的
可选用以下哪种溶液以达到将余氯转化为无毒物质的目的a.
 b.
b. c.
c. d.
d.
写出其中一个反应的离子方程式:
(4)
 是燃油汽车尾气中的主要污染物之一、在催化剂和加热条件下,
是燃油汽车尾气中的主要污染物之一、在催化剂和加热条件下, 与
与 可反应生成无害物质,请写出反应的化学方程式
可反应生成无害物质,请写出反应的化学方程式
您最近半年使用:0次
名校
解题方法
3 . 下图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是
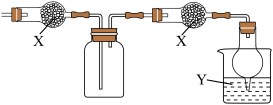
选项 | 试剂X | 收集气体 | 试剂Y |
A. | 碱石灰 | 氯化氢 | 水 |
B. | 碱石灰 | 氨气 | 水 |
C. | 五氧化二磷 | 二氧化硫 | 氢氧化钠溶液 |
D. | 氯化钙 | 一氧化氮 | 氢氧化钠溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
4 . 下列反应的离子方程式正确的是
A.将足量 通入 通入 溶液中: 溶液中: |
B.FeO与稀硝酸反应: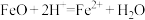 |
C.用足量的氨水吸收烟气中的 : :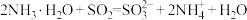 |
D.向硫化钠溶液通入足量二氧化硫: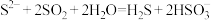 |
您最近半年使用:0次
解题方法
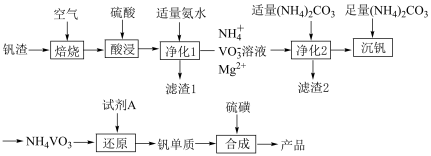
5 . 一个由北理工、北大、南阳理工等科学家组成的联合研究团队,首次提出并构筑出全新的2D-1D的本征异维超结构形式,该异维超结构由2DVS2和1DVS相互交叉排列,实现了多重研究突破。某科研小组以钒渣(主要成分是V2O3、Fe2O3、Al2O3、MgO、CuO和有机杂质)为主要原料制备VS、VS2的流程如下:
①含钒元素的离子在溶液中的主要存在形式与pH如下表所示。
②钒酸(H3VO4)是强酸,NH4VO3是白色粉末,微溶于冷水,可溶于热水。
请回答下列问题:
(1)写两种质子数和电子数均与 相同的离子:
相同的离子:_______ (填化学式)。
(2)废料中有机杂质在_______ (填工序名称)中被除去。
(3)“净化1”中pH=6时Fe3+、Al3+、Cu2+已完全沉淀,但在实际生产中仍然调节pH=7左右,其目的是_______ 。
(4)滤渣2的主要成分是_______ (填化学式)。
(5)洗涤NH4VO3沉淀时,与选用热水洗涤相比,流程中选用冷水洗涤的优点为_______ ;检验是否洗涤干净的方法是_______ 。
(6)试剂A可能是Al、CO、H2,若选择Al,除了生成钒单质,还会生成铝的氧化物和一种能使湿润的红色石蕊试纸变蓝的气体,其化学方程式为_______ 。若制备等质量的钒,需要还原剂Al、CO、H2的质量之比为_______ 。
①含钒元素的离子在溶液中的主要存在形式与pH如下表所示。
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 | VO | VO | V2O | VO |
请回答下列问题:
(1)写两种质子数和电子数均与
 相同的离子:
相同的离子:(2)废料中有机杂质在
(3)“净化1”中pH=6时Fe3+、Al3+、Cu2+已完全沉淀,但在实际生产中仍然调节pH=7左右,其目的是
(4)滤渣2的主要成分是
(5)洗涤NH4VO3沉淀时,与选用热水洗涤相比,流程中选用冷水洗涤的优点为
(6)试剂A可能是Al、CO、H2,若选择Al,除了生成钒单质,还会生成铝的氧化物和一种能使湿润的红色石蕊试纸变蓝的气体,其化学方程式为
您最近半年使用:0次
6 . 氮元素是生命物质中重要的组成元素之一,氮气经过一系列的变化可以生成氨、氮的氧化物、硝酸等重要的化工原料。工业合成氨是人类科学技术的一项重大突破,其合成原理为
 。实验室中可通过铵盐与强碱共热制取少量的
。实验室中可通过铵盐与强碱共热制取少量的 并验证其性质。下列装置用于实验室制取
并验证其性质。下列装置用于实验室制取 ,其中能达到实验目的的是
,其中能达到实验目的的是

 。实验室中可通过铵盐与强碱共热制取少量的
。实验室中可通过铵盐与强碱共热制取少量的 并验证其性质。下列装置用于实验室制取
并验证其性质。下列装置用于实验室制取 ,其中能达到实验目的的是
,其中能达到实验目的的是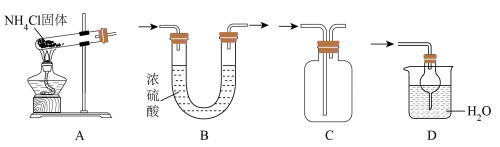
A.制取 | B.干燥 | C.收集 | D.吸收尾气 |
您最近半年使用:0次
名校
7 . 下列方程式或转化关系不正确的是
A.氨催化氧化生成N2O的化学方程式为2NH3+2O2 N2O+3H2O N2O+3H2O |
B.NH4Cl溶液与稀NaOH溶液反应的离子方程式为 +OH-=NH3∙H2O +OH-=NH3∙H2O |
C.N2 NH3 NH3 NH4Cl NH4Cl |
D.NH3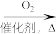 NO2 NO2 O2 O2 |
您最近半年使用:0次
名校
解题方法
8 . 下列离子方程式书写错误的是
A.碳酸氢钠溶液与硫酸氢钠溶液反应: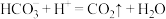 |
B. 通入 通入 溶液中: 溶液中: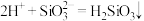 |
C. 通入氯水中: 通入氯水中: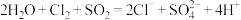 |
D. 通入过量氨水中: 通入过量氨水中: |
您最近半年使用:0次
7日内更新
|
374次组卷
|
4卷引用:河北省保定市定州市第二中学2023-2024学年高一下学期3月月考化学试题
9 . I.某实验小组利用以下装置制取氨气并探究氨气的性质:___________ 。
(2)装置B中的干燥剂是___________ (填名称)。
(3)装置C中的现象是___________ 。
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到非常明显的现象是___________ ,请写出发生反应的化学方程式___________ 。
(5)为防止过量氨气外逸,需在上述装置末端增加尾气吸收装置,应选用的装置是___________ (填“E”或“F”)。
II.二氧化硅、高纯硅、硅胶是现代信息、半导体和光伏发电等产业都需要的基础材料。
(6)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为___________ 。
(7)1molSi中含Si-Si键的数目为___________ 。
(8)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:___________ 。
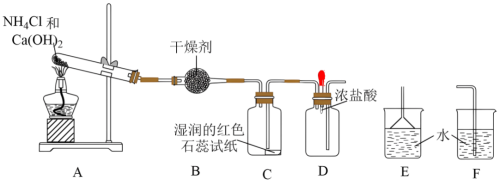
(2)装置B中的干燥剂是
(3)装置C中的现象是
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到非常明显的现象是
(5)为防止过量氨气外逸,需在上述装置末端增加尾气吸收装置,应选用的装置是
II.二氧化硅、高纯硅、硅胶是现代信息、半导体和光伏发电等产业都需要的基础材料。
(6)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
(7)1molSi中含Si-Si键的数目为
(8)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:
您最近半年使用:0次
10 . 到目前为止,我们学习了 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等气体。
等气体。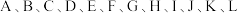 各代表以上气体中一种气体,它们具有如下性质:
各代表以上气体中一种气体,它们具有如下性质:
①A能使湿润的红色石蕊试纸变蓝,A和B相遇时,会产生大量白烟;
②将C和D分别通入品红溶液时,品红溶液都会褪色,但给褪色后的溶液加热时,通入D的溶液会重新变红,通入C的溶液不会重新变红;
③E和F相遇生成红棕色气体K;
④G有臭鸡蛋气味,G在足量F中燃烧生成D和 ;
;
⑤H在C中燃烧时,生成B,同时在集气瓶口会有白雾出现;
⑥D和I都能使澄清石灰水变浑浊;⑦J在F中燃烧生成I.
⑧在加热及催化剂催化下,J和E反应生成I和L.
(1)写出A与B反应的化学方程式______ 。
(2)写出E和F反应的化学方程式______ 。
(3)写出G在足量F中燃烧的方程式______ 。
(4)④中发生反应的化学方程式为______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等气体。
等气体。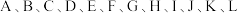 各代表以上气体中一种气体,它们具有如下性质:
各代表以上气体中一种气体,它们具有如下性质:①A能使湿润的红色石蕊试纸变蓝,A和B相遇时,会产生大量白烟;
②将C和D分别通入品红溶液时,品红溶液都会褪色,但给褪色后的溶液加热时,通入D的溶液会重新变红,通入C的溶液不会重新变红;
③E和F相遇生成红棕色气体K;
④G有臭鸡蛋气味,G在足量F中燃烧生成D和
 ;
;⑤H在C中燃烧时,生成B,同时在集气瓶口会有白雾出现;
⑥D和I都能使澄清石灰水变浑浊;⑦J在F中燃烧生成I.
⑧在加热及催化剂催化下,J和E反应生成I和L.
(1)写出A与B反应的化学方程式
(2)写出E和F反应的化学方程式
(3)写出G在足量F中燃烧的方程式
(4)④中发生反应的化学方程式为
您最近半年使用:0次



