名校
解题方法
1 . 下列物质的转化在给定条件下能实现的是
A.浓盐酸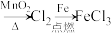 |
B.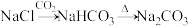 |
C.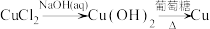 , , |
D.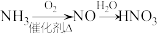 |
您最近半年使用:0次
名校
解题方法
2 . 下列关于一氧化氮的说法不正确 的是
| A.是无色气体 | B.属于非金属氧化物 | C.能与水反应 | D.常温下易与氧气反应 |
您最近半年使用:0次
名校
3 . 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是

| A.洗气瓶中产生的沉淀是硫酸钡 |
| B.在Z导管出来的气体中无二氧化碳 |
| C.洗气瓶中产生的沉淀是碳酸钡 |
| D.在Z导管口无明显现象 |
您最近半年使用:0次
名校
4 . 绿水青山,保护环境是当今社会发展必须关注的重要课题。氮氧化物和硫氧化物是造成大气污染的主要原因之一,消除氮氧化物有多种方法。
 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图1所示。
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图1所示。___________ (任写一点)。
(2) 与
与 反应的化学方程式
反应的化学方程式___________ 。
(3)用Fe做催化剂时,在氨气足量的情况下,不同 对应的脱氮率如图2所示,脱氮效果最佳的
对应的脱氮率如图2所示,脱氮效果最佳的
___________ 。 B.
B. C.
C.
 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图1所示。
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图1所示。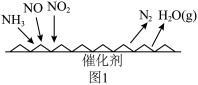
(2)
 与
与 反应的化学方程式
反应的化学方程式(3)用Fe做催化剂时,在氨气足量的情况下,不同
 对应的脱氮率如图2所示,脱氮效果最佳的
对应的脱氮率如图2所示,脱氮效果最佳的
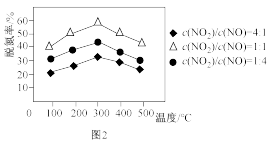
 B.
B. C.
C.
您最近半年使用:0次
5 . 下列关于氮元素及其化合物的说法正确的是
| A.机动车发动机中氮气和氧气会在高温条件下直接生成二氧化氮 |
| B.NO、NO2都是酸性氧化物 |
| C.液氨可用作制冷剂,因为其汽化要吸收大量的热 |
| D.氮氧化物易形成酸雨,酸雨是pH值大于5.6的雨水 |
您最近半年使用:0次
名校
6 . 在指定条件下,下列选项所示的物质间转化能实现的是
A.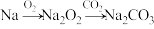 | B.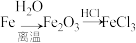 |
C.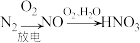 | D.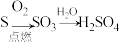 |
您最近半年使用:0次
名校
解题方法
7 . 亚硝酸钠广泛用于工业、建筑业及食品加工业.某课外活动小组的同学拟制备亚硝酸钠、测定其产品的纯度并验证亚硝酸钠的某些性质。
(1)甲组同学采用下图装置制取亚硝酸钠。______ 。
②A中用 的硫酸而不用稀硫酸的原因是
的硫酸而不用稀硫酸的原因是______ 。
③若通入装置 中的
中的 与
与 按物质的量之比1:1被
按物质的量之比1:1被 溶液完全吸收,反应过程中无气体生成,则装置
溶液完全吸收,反应过程中无气体生成,则装置 中发生反应的化学方程式为
中发生反应的化学方程式为______ 。
(2)乙组同学测定甲组制得的产品中 的纯度。称取
的纯度。称取 试样于锥形瓶中,加入适量水溶解,与
试样于锥形瓶中,加入适量水溶解,与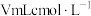 的酸性
的酸性 溶液恰好完全反应,则产品的纯度为
溶液恰好完全反应,则产品的纯度为______ (用含c、m、V的代数式表示)。
(3)现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应气体产物的成分。已知:气体液化的温度 为
为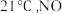 为
为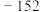 ℃。
℃。 中生成的气体产物,仪器的连接顺序(按左
中生成的气体产物,仪器的连接顺序(按左 右连接)为
右连接)为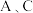 、
、______ 、______ 、______ 。
②装置 的作用是
的作用是______ 。
③滴入硫酸后,观察到A中有红棕色气体产生。依据______ 的现象,确定该气体中还有NO。
④通过上述实验探究过程,可得出装置A中反应的化学方程式是______ 。
(1)甲组同学采用下图装置制取亚硝酸钠。
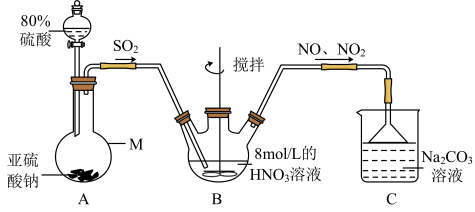
②A中用
 的硫酸而不用稀硫酸的原因是
的硫酸而不用稀硫酸的原因是③若通入装置
 中的
中的 与
与 按物质的量之比1:1被
按物质的量之比1:1被 溶液完全吸收,反应过程中无气体生成,则装置
溶液完全吸收,反应过程中无气体生成,则装置 中发生反应的化学方程式为
中发生反应的化学方程式为(2)乙组同学测定甲组制得的产品中
 的纯度。称取
的纯度。称取 试样于锥形瓶中,加入适量水溶解,与
试样于锥形瓶中,加入适量水溶解,与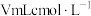 的酸性
的酸性 溶液恰好完全反应,则产品的纯度为
溶液恰好完全反应,则产品的纯度为(3)现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应气体产物的成分。已知:气体液化的温度
 为
为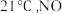 为
为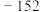 ℃。
℃。
 中生成的气体产物,仪器的连接顺序(按左
中生成的气体产物,仪器的连接顺序(按左 右连接)为
右连接)为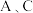 、
、②装置
 的作用是
的作用是③滴入硫酸后,观察到A中有红棕色气体产生。依据
④通过上述实验探究过程,可得出装置A中反应的化学方程式是
您最近半年使用:0次
名校
解题方法
8 . 含氮的化合物在化学反应中变化复杂。
Ⅰ.现用下图所示仪器(夹持装置已省略及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:①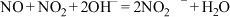 ;
;
②气体液化的温度: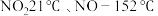 。
。___________ 。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是:___________ 。
(3)在关闭弹簧夹,滴入70%硫酸后,A中产生红棕色气体。
①盛装70%硫酸的仪器名称是___________ ;
②实验确认有NO的现象是___________ 。
(4)通过上述实验探究过程,可得出装置A中反应的化学方程式是___________ 。
Ⅱ.NH3经一系列反应可以得到HNO3和NH4NO3,如图所示。
a.NH4NO3是一种白色晶体,易溶于水,微溶于乙醇。
b.在230℃以上时,同时有弱光: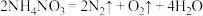
c.在400℃以上时,剧烈分解发生爆炸:
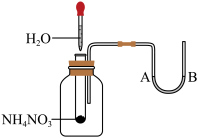
(5)如图将水滴入盛有硝酸铵的试管中,观察到的A处液面上升,B处液面下降,产生该现象的原因___________ 。___________ ,___________ (填“能”或“不能”)用硝酸铵代替氯化铵。
(7)完成离子反应Ⅳ:________ 。
 。
。
Ⅰ.现用下图所示仪器(夹持装置已省略及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:①
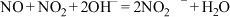 ;
;②气体液化的温度:
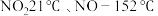 。
。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是:
(3)在关闭弹簧夹,滴入70%硫酸后,A中产生红棕色气体。
①盛装70%硫酸的仪器名称是
②实验确认有NO的现象是
(4)通过上述实验探究过程,可得出装置A中反应的化学方程式是
Ⅱ.NH3经一系列反应可以得到HNO3和NH4NO3,如图所示。
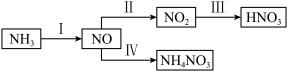
a.NH4NO3是一种白色晶体,易溶于水,微溶于乙醇。
b.在230℃以上时,同时有弱光:
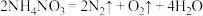
c.在400℃以上时,剧烈分解发生爆炸:

(5)如图将水滴入盛有硝酸铵的试管中,观察到的A处液面上升,B处液面下降,产生该现象的原因
(7)完成离子反应Ⅳ:
 。
。
您最近半年使用:0次
9 . A、B、C、D、E、F、G为中学化学常见物质,它们之间有如图转化关系(反应条件已略去)。已知:A、C、D、E均含有同种非金属元素,A为 ,B为
,B为 ;G是一种紫红色的金属单质;光照条件下,E的浓溶液分解可得到B、D、F。根据所学知识,按要求回答下列问题:
;G是一种紫红色的金属单质;光照条件下,E的浓溶液分解可得到B、D、F。根据所学知识,按要求回答下列问题:_______ 个。
(2)下列有关 的说法中,不正确的是_______(填字母)。
的说法中,不正确的是_______(填字母)。
(3)写出反应①的化学方程式:_______ 。
(4)写出反应④的离子方程式:_______ 。
(5)合成氨工业中,气体经由分离器实现氨与原料气的分离,分离器中压强约为15MPa,温度约为-20℃,分离时应用了氨的_______ 性质。
 ,B为
,B为 ;G是一种紫红色的金属单质;光照条件下,E的浓溶液分解可得到B、D、F。根据所学知识,按要求回答下列问题:
;G是一种紫红色的金属单质;光照条件下,E的浓溶液分解可得到B、D、F。根据所学知识,按要求回答下列问题: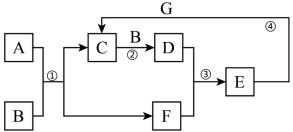
(2)下列有关
 的说法中,不正确的是_______(填字母)。
的说法中,不正确的是_______(填字母)。A.工业合成 需要在高温、高压、催化剂下进行 需要在高温、高压、催化剂下进行 |
B. 可用来生产碳铵和尿素等化肥 可用来生产碳铵和尿素等化肥 |
C. 可用浓硫酸或无水氯化钙干燥 可用浓硫酸或无水氯化钙干燥 |
D. 受热易分解,须置于冷暗处保存 受热易分解,须置于冷暗处保存 |
(3)写出反应①的化学方程式:
(4)写出反应④的离子方程式:
(5)合成氨工业中,气体经由分离器实现氨与原料气的分离,分离器中压强约为15MPa,温度约为-20℃,分离时应用了氨的
您最近半年使用:0次
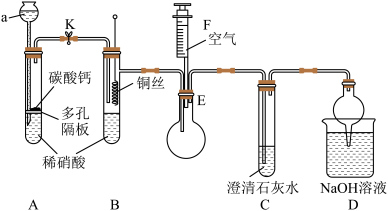
10 . 某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是一半空的注射器。请回答有关问题:
(1)仪器a的名称为___________ 。
(2)装置A制取 的目的是
的目的是___________ 。
(3)当___________ (填某装置中出现的实验现象)时,关闭K,将装置B中铜丝插入稀硝酸,并微热之,装置B中生成 时发生反应的离子方程式为
时发生反应的离子方程式为___________ 。
(4)验证装置B中生成的是 气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为
气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为___________ 。
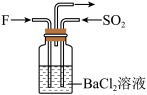
(5)气体NO2和气体SO2在通常条件下同时通入盛有BaCl2溶液的洗气瓶中(如图所示),洗气瓶中是否有沉淀生成?(填“有”或“没有”)___________ ,理由是___________ 。___________ 。
(1)仪器a的名称为
(2)装置A制取
 的目的是
的目的是(3)当
 时发生反应的离子方程式为
时发生反应的离子方程式为(4)验证装置B中生成的是
 气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为
气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为(5)气体NO2和气体SO2在通常条件下同时通入盛有BaCl2溶液的洗气瓶中(如图所示),洗气瓶中是否有沉淀生成?(填“有”或“没有”)
您最近半年使用:0次



