名校
解题方法
1 . 下列方程式的书写,不正确 的是
A. 溶液暴露在空气中: 溶液暴露在空气中: |
B.铅酸蓄电池放电的负极反应: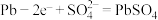 |
C.葡萄糖与新制氢氧化铜反应: |
D.煅烧黄铁矿制 |
您最近半年使用:0次
名校
2 . 新制Cu(OH)2悬浊液在医疗上用于检验糖尿病,其与Na2SO3(aq)反应也产生相同现象。
(1)葡萄糖与新制Cu(OH)2加热反应得到的有机产物经酸化后的结构简式为___________ 。
(2)写出Na2SO3(aq)与新制Cu(OH)2反应的离子方程式___________ 。
(3)已知:25℃时,Cu(OH)2(s)+2OH-
 K=1×10-3。在1LNaOH(aq)中,欲使0.01 mol Cu(OH)2溶解,则c(NaOH)>
K=1×10-3。在1LNaOH(aq)中,欲使0.01 mol Cu(OH)2溶解,则c(NaOH)>___________ mol/L(保留2位小数)。
(1)葡萄糖与新制Cu(OH)2加热反应得到的有机产物经酸化后的结构简式为
(2)写出Na2SO3(aq)与新制Cu(OH)2反应的离子方程式
(3)已知:25℃时,Cu(OH)2(s)+2OH-

 K=1×10-3。在1LNaOH(aq)中,欲使0.01 mol Cu(OH)2溶解,则c(NaOH)>
K=1×10-3。在1LNaOH(aq)中,欲使0.01 mol Cu(OH)2溶解,则c(NaOH)>
您最近半年使用:0次
名校
解题方法
3 . 下列实验的设计方案、现象和结论有错误的是
选项 | 实验目的 | 设计方案和实验现象 | 结论 |
A | 检验菠菜中是否含有铁元素 | 取少量菠菜叶剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硝酸后,再加入KSCN溶液,溶液变红 | 菠菜中含有铁元素 |
B | 检验尿液中是否含有葡萄糖 | 取尿液适量,向其中加入NaOH至溶液呈碱性,加入新制的 悬浊液,加热煮沸,产生砖红色沉淀 悬浊液,加热煮沸,产生砖红色沉淀 | 尿液中含有葡萄糖 |
C | 向 的水溶液中滴加硝酸银溶液 的水溶液中滴加硝酸银溶液 | 无明显现象 | 该配合物中 的配位数是6 的配位数是6 |
D | 比较配离子 、 、 的稳定性 的稳定性 | 将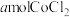 固体溶于水,加入适量浓盐酸后,再加入 固体溶于水,加入适量浓盐酸后,再加入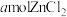 固体。溶液先由粉红色变为蓝色,再由蓝色变成粉红色(已知: 固体。溶液先由粉红色变为蓝色,再由蓝色变成粉红色(已知: 呈粉红色, 呈粉红色, 呈蓝色, 呈蓝色, 呈无色) 呈无色) | 稳定性: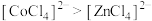 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
4 . 下列分离提纯及其性质鉴别方法正确的是
| A.除去乙醇中少量的水,加入新制的生石灰,蒸发 |
| B.很多蛋白质与浓硝酸作用时呈黄色,可用于蛋白质的检验 |
| C.除去乙酸乙酯中的乙酸,可加入 NaOH 溶液后分液 |
| D.葡萄糖在一定条件下可以与新制氢氧化铜反应,生成黑色氧化铜沉淀 |
您最近半年使用:0次
23-24高一下·全国·课前预习
解题方法
5 . 葡萄糖、果糖
(1)二者分子式相同,但结构_____ ,互为同分异构体。均属于多羟基醛,官能团有_____ ,既有_____ 的性质,又有_____ 的性质。
(2)葡萄糖中醛基的检验
(1)二者分子式相同,但结构
(2)葡萄糖中醛基的检验
| 实验内容 | 实验操作 | 实验现象 | 解释或结论 |
| 用银氨溶液检验醛基 |  | ||
| 用新制氢氧化铜悬浊液检验醛基 | 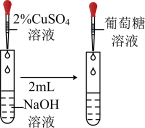 |
您最近半年使用:0次
6 . 纳米Cu2O的制备方法有多种,常见的有还原法、电解法等。
(1)还原法以葡萄糖作为主要原料。能用葡萄糖制备Cu2O是因为其分子中含有
(2)电解法制备Cu2O的装置如图所示,电解过程中阳极依次发生反应:
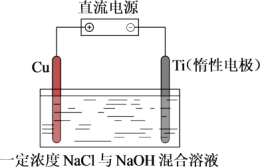
①Cu-e-+Cl-=CuCl
②CuCl(s)+OH-(aq)=CuOH(s)+Cl-(aq)
③2CuOH=Cu2O+H2O
阴极的电极反应式为
您最近半年使用:0次
解题方法
7 . 下列实验操作、现象和结论均正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向甲苯中加入酸性高锰酸钾溶液,紫色褪去 | 甲苯及其同系物均可被酸性高锰酸钾溶液氧化 |
| B | 向某稀溶液中加入NaOH溶液,产生使湿润的红色石蕊试纸变蓝的气体 | 溶液中含有 |
| C | 向 溶液中缓慢滴加硫酸,溶液由黄色变为橙红色(已知水溶液中 溶液中缓慢滴加硫酸,溶液由黄色变为橙红色(已知水溶液中 为黄色, 为黄色, 为橙红色) 为橙红色) | 增大氢离子浓度可使 转化为 转化为 |
| D | 向 溶液中加入少量 溶液中加入少量 溶液,再滴加葡萄糖溶液并加热,产生砖红色沉淀 溶液,再滴加葡萄糖溶液并加热,产生砖红色沉淀 | 新制 可检验葡萄糖 可检验葡萄糖 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
8 . 草酸晶体(H2C2O4⋅2H2O)用途广泛,易溶于水,其制备及纯度测定实验如下。
I.制备
步骤1:将mg淀粉溶于水与少量硫酸加入反应器中,保持85~90℃约30min,然后逐渐降温至60℃左右。
步骤2:控制反应温度在55~60℃条件下,边搅拌边缓慢滴加含有适量催化剂的混酸(65%硝酸与98%硫酸),主要反应为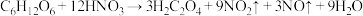 。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体
。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体 。
。
Ⅱ.纯度测定
称取制得的草酸晶体 ,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。对于上述实验,下列做法正确的是
,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。对于上述实验,下列做法正确的是
I.制备
步骤1:将mg淀粉溶于水与少量硫酸加入反应器中,保持85~90℃约30min,然后逐渐降温至60℃左右。
步骤2:控制反应温度在55~60℃条件下,边搅拌边缓慢滴加含有适量催化剂的混酸(65%硝酸与98%硫酸),主要反应为
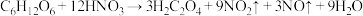 。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体
。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体 。
。Ⅱ.纯度测定
称取制得的草酸晶体
 ,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。对于上述实验,下列做法正确的是
,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。对于上述实验,下列做法正确的是| A.配制“混酸”时应将65%硝酸缓慢加入98%硫酸中,边加边搅拌 |
B.检验“步骤1”水解液中的葡萄糖,操作为取水解液加入新制 悬浊液并加热 悬浊液并加热 |
| C.“精制”过程为溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
| D.滴定过程中滴定速度先快后慢,眼睛密切观察滴定管的液面变化 |
您最近半年使用:0次
9 . 关于有机物检测,下列说法正确的是
| A.用浓溴水可鉴别溴乙烷、乙醛和苯酚 |
| B.用红外光谱可确定有机物的元素组成 |
| C.质谱法测得某有机物的相对分子质量为72,可推断其分子式为C5H12 |
| D.检验葡萄糖中醛基的方法:取样,加新制Cu(OH)2悬浊液观察是否产生砖红色沉淀 |
您最近半年使用:0次
23-24高二下·全国·课前预习
10 . 葡萄糖
(1)存在与物理性质
葡萄糖存在于___________ 、蜂蜜,以及植物的___________ 、___________ 、___________ 、___________ 中。动物的血液和淋巴液中也含有葡萄糖。葡萄糖是易溶于水的无色晶体,熔点为146 ℃,有甜味,但甜度不如蔗糖。
(2)分子式与结构特点
分子式为___________ ,分子中含有___________ 和___________ ,属于醛糖。结构简式为___________ 。
(3)化学性质
葡萄糖具有醛和醇的特征反应
①还原性:与新制Cu(OH)2悬浊液反应、银镜反应、使溴水和酸性高锰酸钾溶液褪色。
②不饱和性:与H2发生___________ 反应。
③与羧酸等发生取代反应。1 mol葡萄糖可以与___________ 乙酸发生酯化反应。
④体内氧化反应提供能量,是一种重要的营养物质。
C6H12O6+6O2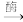 6CO2+6H2O
6CO2+6H2O
(1)存在与物理性质
葡萄糖存在于
(2)分子式与结构特点
分子式为
(3)化学性质
葡萄糖具有醛和醇的特征反应
①还原性:与新制Cu(OH)2悬浊液反应、银镜反应、使溴水和酸性高锰酸钾溶液褪色。
②不饱和性:与H2发生
③与羧酸等发生取代反应。1 mol葡萄糖可以与
④体内氧化反应提供能量,是一种重要的营养物质。
C6H12O6+6O2
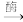 6CO2+6H2O
6CO2+6H2O
您最近半年使用:0次



