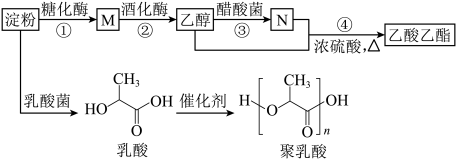
葡萄糖、果糖
(1)二者分子式相同,但结构_____ ,互为同分异构体。均属于多羟基醛,官能团有_____ ,既有_____ 的性质,又有_____ 的性质。
(2)葡萄糖中醛基的检验
(1)二者分子式相同,但结构
(2)葡萄糖中醛基的检验
| 实验内容 | 实验操作 | 实验现象 | 解释或结论 |
| 用银氨溶液检验醛基 |  | ||
| 用新制氢氧化铜悬浊液检验醛基 | 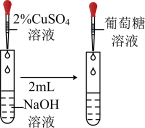 |
23-24高一下·全国·课前预习 查看更多[2]
更新时间:2024-03-27 10:55:46
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】Ⅰ.为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程;
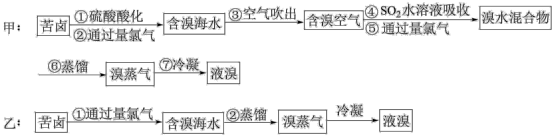
(1)甲同学步骤④所发生反应的离子方程式为___________ 。
(2)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是___________ (填“甲”或“乙”),理由是___________ 。
Ⅱ.如图是乙酸乙酯的绿色合成路线之一:
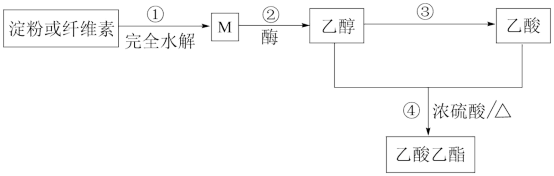
(1)M的分子式为___________ 。
(2)下列说法不正确的是___________ (填字母)
A.淀粉和纤维素都属于天然高分子化合物
B.M可与新制的氢氧化铜在加热条件下反应生成砖红色沉淀
C.所有的糖类都有甜味,都可以发生水解反应
D.用饱和碳酸钠溶液可以鉴别乙醇、乙酸和乙酸乙酯
(3)乙醇和乙酸在一定条件下制备乙酸乙酯。
①乙酸中官能团的名称是___________ 。
②生成乙酸乙酯的反应是可逆反应,下列能说明该反应已达到化学平衡状态的是___________ (填字母)。
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的物质的量相等

(1)甲同学步骤④所发生反应的离子方程式为
(2)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是
Ⅱ.如图是乙酸乙酯的绿色合成路线之一:

(1)M的分子式为
(2)下列说法不正确的是
A.淀粉和纤维素都属于天然高分子化合物
B.M可与新制的氢氧化铜在加热条件下反应生成砖红色沉淀
C.所有的糖类都有甜味,都可以发生水解反应
D.用饱和碳酸钠溶液可以鉴别乙醇、乙酸和乙酸乙酯
(3)乙醇和乙酸在一定条件下制备乙酸乙酯。
①乙酸中官能团的名称是
②生成乙酸乙酯的反应是可逆反应,下列能说明该反应已达到化学平衡状态的是
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的物质的量相等
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】葡萄糖酸钙是一种可促进骨骼生长的营养物质。制取葡萄糖酸钙的流程如图。
葡萄糖溶液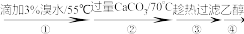 悬浊液
悬浊液 Ca(C6H11O7)2
Ca(C6H11O7)2
已知:a.CH2OH(CHOH)4CHO+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr;
b.2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑;
c.相关物质的溶解性见表:
d.酸性:盐酸>葡萄糖酸>碳酸。
请回答下列问题:
(1)制备葡萄糖酸钙涉及的反应类型有___ 。
(2)第①步中溴水氧化葡萄糖时,下列装置最合适的是___ (填序号)。
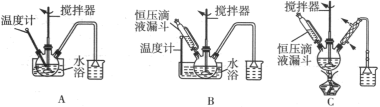
(3)第②步反应CaCO3需过量的原因是____ 。
(4)本实验中不宜用CaCl2替代CaCO3,理由是___ 。
(5)第③步需趁热过滤,其原因是__ 。
(6)若制备时葡萄糖溶液中含有9.0g葡萄糖,步骤⑦后得到8.2g葡萄糖酸钙,则葡萄糖酸钙的产率为___ 。
葡萄糖溶液
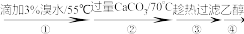 悬浊液
悬浊液 Ca(C6H11O7)2
Ca(C6H11O7)2已知:a.CH2OH(CHOH)4CHO+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr;
b.2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑;
c.相关物质的溶解性见表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 在水中的溶解性 | 可溶于冷水,易溶于热水 | 可溶 | 易溶 | 易溶 |
| 在乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
d.酸性:盐酸>葡萄糖酸>碳酸。
请回答下列问题:
(1)制备葡萄糖酸钙涉及的反应类型有
(2)第①步中溴水氧化葡萄糖时,下列装置最合适的是

(3)第②步反应CaCO3需过量的原因是
(4)本实验中不宜用CaCl2替代CaCO3,理由是
(5)第③步需趁热过滤,其原因是
(6)若制备时葡萄糖溶液中含有9.0g葡萄糖,步骤⑦后得到8.2g葡萄糖酸钙,则葡萄糖酸钙的产率为
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有7瓶失去标签的试剂瓶,已知它们盛装的液体可能是乙醇、乙酸、苯、乙酸乙酯、油脂、葡萄糖溶液、蔗糖溶液。现通过如下实验来确定各试剂中所装液体的名称。
试写出下列序号代表的液体名称:
A___________________ ,B___________________ ,C___________________ ,D___________________ ,E___________________ ,F___________________ ,G___________________ 。
| 实验步骤和方法 | 实验现象 |
| ①把7瓶液体依次标号为A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
| ②各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
③分别取少量7种液体于试管中加新制的 悬浊液并加热 悬浊液并加热 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
④各取C、D、E少量于试管中,加稀 溶液并加执 溶液并加执 | 只有C中仍有分层现象,且在D的试管中闻到特殊香味 |
A
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】(1)乙烯的产量通常用来衡量一个国家的石油化工水平。以乙烯为主要原料合成重要的有机化合物路线如下图所示,请回答下列问题。
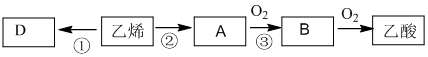
A物质所含官能团的名称是________ 。
(2)反应③的化学方程式是____________________________________________ 。
(3)下列物质中,不能通过乙烯加成反应得到的是________ (填序号)。
a. CH3CH3 b. CH3CHCl2 c. CH3CH2Br
(4)葡萄可用于酿酒。检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是________________________________________ 。
(5)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用下图所示装置制备乙酸乙酯:
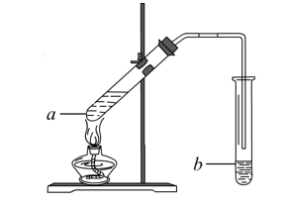
①试管a中生成乙酸乙酯的化学方程式是_______ 。
②实验开始时,试管b中的导管不伸入液面下的原因是________ 。

A物质所含官能团的名称是
(2)反应③的化学方程式是
(3)下列物质中,不能通过乙烯加成反应得到的是
a. CH3CH3 b. CH3CHCl2 c. CH3CH2Br
(4)葡萄可用于酿酒。检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是
(5)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用下图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是
②实验开始时,试管b中的导管不伸入液面下的原因是
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】(Ⅰ)糖尿病是由于体内胰岛素紊乱导致的代谢紊乱综合症,以高血糖为主要标志。长期摄入高热量食品和缺少运动都易导致糖尿病。
(1)血糖是指血液中的葡萄糖(C6H12O6)。下列说法正确的是_____ (填字母序号)。
A.葡萄糖属于碳水化合物,分子可表示为C6(H2O)6,则每个葡萄糖分子中含6个H2O
B.糖尿病人尿糖也高,可用新制的氢氧化铜悬浊液来检测病人尿液中的葡萄糖
C.葡萄糖可用于制镜工业
D.淀粉水解的最终产物是葡萄糖
(2)糖尿病人不可饮酒,酒精在肝脏内可被转化成有机物M。M的实验结果如下:
①通过样品的质谱测得M的相对分子质量为60。
②核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:乙醇(CH3CH2OH)有三种氢原子(图1)。经测定,有机物M的按磁共振氢谱示意图如下图2。
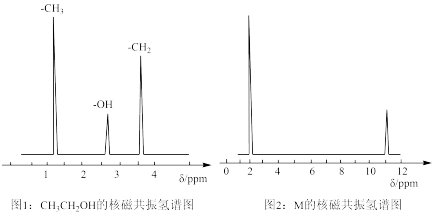
③将M溶于水,滴入石蕊试液,发现溶液变红。试推导写出M的结构简式为____________ 。
(Ⅱ)已知物质A显酸性,F为七原子组成的环状结构,请根据以下框图回答问题:
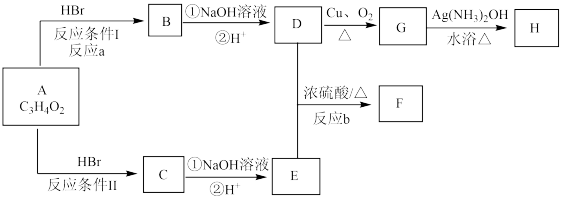
(1) A、H的结构简式为_____________________ 、_____________________ 。
(2)a、b的反应类型分别为_____________________ 、_____________________ 。
(3)D和E生成F的化学方程式_____________________ 。
(4)写出C的同分异构体中属于酯类物质的结构简式_________ 、_________ (任写2种)。
(1)血糖是指血液中的葡萄糖(C6H12O6)。下列说法正确的是
A.葡萄糖属于碳水化合物,分子可表示为C6(H2O)6,则每个葡萄糖分子中含6个H2O
B.糖尿病人尿糖也高,可用新制的氢氧化铜悬浊液来检测病人尿液中的葡萄糖
C.葡萄糖可用于制镜工业
D.淀粉水解的最终产物是葡萄糖
(2)糖尿病人不可饮酒,酒精在肝脏内可被转化成有机物M。M的实验结果如下:
①通过样品的质谱测得M的相对分子质量为60。
②核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:乙醇(CH3CH2OH)有三种氢原子(图1)。经测定,有机物M的按磁共振氢谱示意图如下图2。

③将M溶于水,滴入石蕊试液,发现溶液变红。试推导写出M的结构简式为
(Ⅱ)已知物质A显酸性,F为七原子组成的环状结构,请根据以下框图回答问题:

(1) A、H的结构简式为
(2)a、b的反应类型分别为
(3)D和E生成F的化学方程式
(4)写出C的同分异构体中属于酯类物质的结构简式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有A、B、C、D、E、F、G、H八种白色固体,它们是:KHSO4 、C6 H12O6 (葡萄糖)、HOOCCOOH、MgCO3 、Na2CO3 、MgSO4 、Al(OH)3 、Ba(NO3 )2 ,对这些物质进行实验,结果如下:①各取部分固体分别加入水,除C、F外均能溶解得到澄清溶液;②C(固)+D溶液→固体溶解放出气体,C(固)+H溶液→固体溶解放出气体;③E溶液+H溶液→白色沉淀,E溶液+G溶液→白色沉淀,E溶液+B溶液→白色沉淀;④B溶液+H溶液→放出气体;根据上述实验,判断这八种固体分别是: A__________ ,B_________ ,C___________ ,D_____________ ,E____________ ,F______________ ,G__________ ,H___________ 。要进一步证实某固体为葡萄糖,应用___________ 作试剂,根据_______________ 现象来确证。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下实验流程制得:
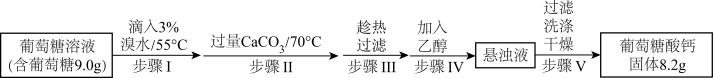
已知:a.反应原理: ;
;

b.相关物质的溶解性见下表
c.相关物质酸性:氢溴酸>葡萄糖酸>碳酸
d.相关物质相对分子质量:葡萄糖180,葡萄糖酸钙430
回答下列问题:
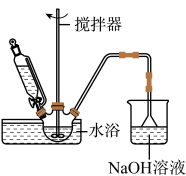
(1)步骤Ⅰ中溴水氧化葡萄糖时,甲同学设计了如图所示装置。你认为缺少的仪器是___________ ,盛放 溶液的烧杯中主要发生反应的离子方程式
溶液的烧杯中主要发生反应的离子方程式___________ 。
(2)检验葡萄糖是否完全被氧化,需要用的试剂有___________ 。
(3)步骤Ⅱ中加入过量 ,除了能提高葡萄糖酸的转化率,还有的作用是
,除了能提高葡萄糖酸的转化率,还有的作用是___________ 。
(4)步骤Ⅲ的过滤过程需要趁热进行的原因是___________ 。
(5)步骤Ⅳ加入乙醇的作用是___________ 。
(6)步骤Ⅴ中,下列洗涤剂最合适的是___________。
(7)该实验中葡萄糖酸钙的产率为___________ (保留3位有效数字)。

已知:a.反应原理:
 ;
;
b.相关物质的溶解性见下表
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 |
| 在水中的溶解性 | 可溶于冷水,易溶于热水 | 可溶 | 极易溶 |
| 在乙醇中的溶解性 | 微溶 | 微溶 | 可溶 |
d.相关物质相对分子质量:葡萄糖180,葡萄糖酸钙430
回答下列问题:
(1)步骤Ⅰ中溴水氧化葡萄糖时,甲同学设计了如图所示装置。你认为缺少的仪器是
 溶液的烧杯中主要发生反应的离子方程式
溶液的烧杯中主要发生反应的离子方程式
(2)检验葡萄糖是否完全被氧化,需要用的试剂有
(3)步骤Ⅱ中加入过量
 ,除了能提高葡萄糖酸的转化率,还有的作用是
,除了能提高葡萄糖酸的转化率,还有的作用是(4)步骤Ⅲ的过滤过程需要趁热进行的原因是
(5)步骤Ⅳ加入乙醇的作用是
(6)步骤Ⅴ中,下列洗涤剂最合适的是___________。
| A.冷水 | B.热水 | C.乙醇—水混合溶液 | D.乙醇 |
(7)该实验中葡萄糖酸钙的产率为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】铜及其化合物在生产、生活中应用广泛。回答下列问题:
(1)用新制Cu(OH)2与葡萄糖反应可制备Cu2O,该反应中葡萄糖是___________ (填“氧化剂”或“还原剂”)。
(2)用H2O2、H2SO4混合溶液浸泡废印刷电路板可制备CuSO4以实现铜的回收利用,其离子方程式为______________________ 。
(3)用NH4NO3氧化海绵铜(含Cu的CuO)生产CuCl的部分流程如下:

①步骤I中反应温度不宜过高的原因是______ ,当0.5 mol NH4NO3参加反应时,反应中有4 mol电子发生转移,则铜参加反应的离子方程式为 ______________ 。
②步骤Ⅱ中物质X可选用____ (填字母),该物质需过量的原因,其一是加快反应速率,其二是____________ 。
a.Cu b.Cl2 c.H2O2 d.(NH4)2SO3
(1)用新制Cu(OH)2与葡萄糖反应可制备Cu2O,该反应中葡萄糖是
(2)用H2O2、H2SO4混合溶液浸泡废印刷电路板可制备CuSO4以实现铜的回收利用,其离子方程式为
(3)用NH4NO3氧化海绵铜(含Cu的CuO)生产CuCl的部分流程如下:

①步骤I中反应温度不宜过高的原因是
②步骤Ⅱ中物质X可选用
a.Cu b.Cl2 c.H2O2 d.(NH4)2SO3
您最近半年使用:0次