Ⅰ.为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程;
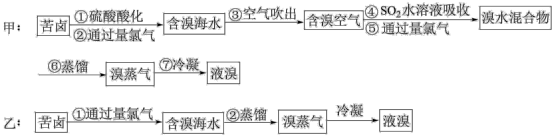
(1)甲同学步骤④所发生反应的离子方程式为___________ 。
(2)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是___________ (填“甲”或“乙”),理由是___________ 。
Ⅱ.如图是乙酸乙酯的绿色合成路线之一:
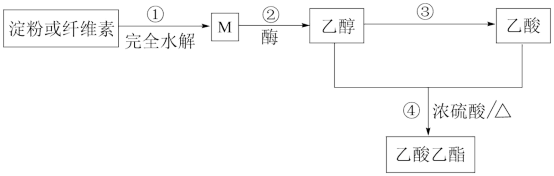
(1)M的分子式为___________ 。
(2)下列说法不正确的是___________ (填字母)
A.淀粉和纤维素都属于天然高分子化合物
B.M可与新制的氢氧化铜在加热条件下反应生成砖红色沉淀
C.所有的糖类都有甜味,都可以发生水解反应
D.用饱和碳酸钠溶液可以鉴别乙醇、乙酸和乙酸乙酯
(3)乙醇和乙酸在一定条件下制备乙酸乙酯。
①乙酸中官能团的名称是___________ 。
②生成乙酸乙酯的反应是可逆反应,下列能说明该反应已达到化学平衡状态的是___________ (填字母)。
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的物质的量相等

(1)甲同学步骤④所发生反应的离子方程式为
(2)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是
Ⅱ.如图是乙酸乙酯的绿色合成路线之一:

(1)M的分子式为
(2)下列说法不正确的是
A.淀粉和纤维素都属于天然高分子化合物
B.M可与新制的氢氧化铜在加热条件下反应生成砖红色沉淀
C.所有的糖类都有甜味,都可以发生水解反应
D.用饱和碳酸钠溶液可以鉴别乙醇、乙酸和乙酸乙酯
(3)乙醇和乙酸在一定条件下制备乙酸乙酯。
①乙酸中官能团的名称是
②生成乙酸乙酯的反应是可逆反应,下列能说明该反应已达到化学平衡状态的是
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的物质的量相等
更新时间:2021-07-07 16:51:40
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某学生在实验室制取乙酸乙酯的主要步骤如下:

①配制 2mL 浓硫酸、3mL 乙醇和 2mL 乙酸的混合溶液。
②按如图所示连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置 分层。分离出乙酸乙酯,洗涤、干燥。
(1)反应中浓硫酸的作用是___________ ;
(2)上述实验中饱和碳酸钠溶液的作用是___________ ;
(3)欲将乙试管中的物质分离以得到乙酸乙酯,进行的操作是___________ ,必须使用的仪器有___________ 和小烧杯,分离时,乙酸乙酯应从仪器___________ (填“下口放”或“上口倒”)出。
(4)该反应为可逆反应,要提高乙酸乙酯的产率,可以采取的措施有___________ 。

①配制 2mL 浓硫酸、3mL 乙醇和 2mL 乙酸的混合溶液。
②按如图所示连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置 分层。分离出乙酸乙酯,洗涤、干燥。
(1)反应中浓硫酸的作用是
(2)上述实验中饱和碳酸钠溶液的作用是
(3)欲将乙试管中的物质分离以得到乙酸乙酯,进行的操作是
(4)该反应为可逆反应,要提高乙酸乙酯的产率,可以采取的措施有
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】下图是实验室制备乙酸乙酯的实验装置。试回答:
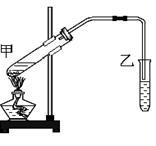
(1)试管甲中加入的试剂顺序是( )
A.乙醇、浓硫酸、乙酸
B.浓硫酸、乙醇、乙酸
C.浓硫酸、乙酸、乙醇
(2)甲处的试管内发生反应的化学方程式为:_________________________________
(3)小试管乙中饱和Na2CO3的作用是( )
A、吸收乙醇
B、中和乙酸
C、增大溶液密度,降低乙酸乙酯在里面的溶解度
(4)乙装置中的导管未插入溶液的目的是_______________________________ 。

(1)试管甲中加入的试剂顺序是
A.乙醇、浓硫酸、乙酸
B.浓硫酸、乙醇、乙酸
C.浓硫酸、乙酸、乙醇
(2)甲处的试管内发生反应的化学方程式为:
(3)小试管乙中饱和Na2CO3的作用是
A、吸收乙醇
B、中和乙酸
C、增大溶液密度,降低乙酸乙酯在里面的溶解度
(4)乙装置中的导管未插入溶液的目的是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D四种有机物分别由碳、氢、氧元素中的两种或三种元素组成,各取四种有机物0.100mol,分别完全燃烧,均能得到4.48L (标准状况下)二氧化碳;D的水溶液显酸性。四种有机物转化关系如图:
A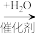 B
B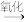 C
C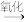 D
D
回答下列问题:
(1)D分子中所含官能团的名称是___________ 。
(2)amolA、B的混合气体完全燃烧,消耗氧气的体积为___________ (标准状况)。
(3)B→C的化学方程式为___________ 。
(4)在实验室里可以用如图所示的装置制取乙酸乙酯。

写出用CH3CH218OH与乙酸发生酯化反应的化学方程式为___________ 。
(5)对所得乙酸乙酯粗产品的提纯过程如下(氯化钙与乙醇生成难溶物)。

操作Ⅲ的名称为___________ 。
A
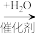 B
B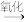 C
C D
D回答下列问题:
(1)D分子中所含官能团的名称是
(2)amolA、B的混合气体完全燃烧,消耗氧气的体积为
(3)B→C的化学方程式为
(4)在实验室里可以用如图所示的装置制取乙酸乙酯。

写出用CH3CH218OH与乙酸发生酯化反应的化学方程式为
(5)对所得乙酸乙酯粗产品的提纯过程如下(氯化钙与乙醇生成难溶物)。

操作Ⅲ的名称为
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】秸秆(含多糖物质)的综合应用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子化合物的路线:
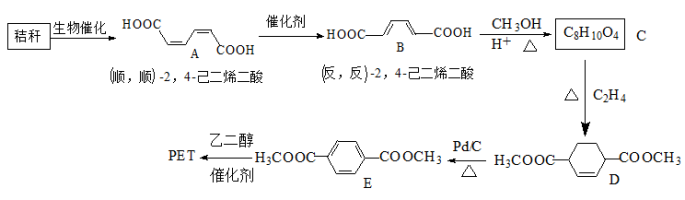
回答下列问题:
(1)下列关于糖类的说法正确的是_____ 。(填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为______ 。
(3)D中官能团名称为_____ ,D生成E的反应类型为_______ 。
(4)具有一种官能团的二取代芳香化合物W是E的同分异构体,0.5mol W与足量碳酸氢钠溶液反应共生成44g CO2,W共有_____ 种(不含立体结构),其中核磁共振氢谱为三组峰的结构简式为______ 。
(5)参照上述合成路线,以(反,反)﹣2,4﹣己二烯和C2H4为原料(无机试剂任选),设计制备对苯二甲酸的合成路线______ 。

回答下列问题:
(1)下列关于糖类的说法正确的是
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为
(3)D中官能团名称为
(4)具有一种官能团的二取代芳香化合物W是E的同分异构体,0.5mol W与足量碳酸氢钠溶液反应共生成44g CO2,W共有
(5)参照上述合成路线,以(反,反)﹣2,4﹣己二烯和C2H4为原料(无机试剂任选),设计制备对苯二甲酸的合成路线
您最近半年使用:0次
【推荐2】正误判断
(1)氨基酸、淀粉均属于高分子化合物____
(2)蛋白质是结构复杂的高分子化合物,分子中都含有C、H、O、N____
(3)若两种二肽互为同分异构体,则二者的水解产物一定不一致____
(4)蛋白质溶液里加入饱和硫酸铵溶液,有沉淀析出,再加入蒸馏水,沉淀不溶解____
(5)重金属盐能使蛋白质变性,所以误食重金属盐会中毒____
(6)浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸与蛋白质发生了显色反应____
(7)蛋白质溶液里的蛋白质能透过半透膜____
(8)用甘氨酸( )和丙氨酸(
)和丙氨酸(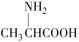 )缩合最多可形成四种二肽
)缩合最多可形成四种二肽____
(9)在紫外线、饱和Na2SO4、CuSO4溶液、福尔马林等作用下,蛋白质均会发生变性____
(10)在一定条件下,氨基酸之间能发生反应,合成更加复杂的化合物____
(11)从混合物中分离提纯蛋白质可采用过滤的方法____
(12)淀粉、油脂和蛋白质都能在NaOH溶液中发生水解____
(1)氨基酸、淀粉均属于高分子化合物
(2)蛋白质是结构复杂的高分子化合物,分子中都含有C、H、O、N
(3)若两种二肽互为同分异构体,则二者的水解产物一定不一致
(4)蛋白质溶液里加入饱和硫酸铵溶液,有沉淀析出,再加入蒸馏水,沉淀不溶解
(5)重金属盐能使蛋白质变性,所以误食重金属盐会中毒
(6)浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸与蛋白质发生了显色反应
(7)蛋白质溶液里的蛋白质能透过半透膜
(8)用甘氨酸(
 )和丙氨酸(
)和丙氨酸(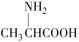 )缩合最多可形成四种二肽
)缩合最多可形成四种二肽(9)在紫外线、饱和Na2SO4、CuSO4溶液、福尔马林等作用下,蛋白质均会发生变性
(10)在一定条件下,氨基酸之间能发生反应,合成更加复杂的化合物
(11)从混合物中分离提纯蛋白质可采用过滤的方法
(12)淀粉、油脂和蛋白质都能在NaOH溶液中发生水解
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】某同学称取9 g淀粉溶于水,测定淀粉的水解百分率。其程序如下:
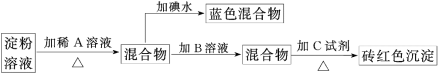
(1)各步加入的试剂为(写化学式):A________ 、B________ 、C________ 。
(2)若加入A溶液不加入B溶液_______ (填“是”或“否”)合理,其理由是_______________ 。
(3)已知1 mol葡萄糖与新制Cu(OH)2悬浊液反应生成1 mol Cu2O,当生成1.44 g砖红色沉淀时,淀粉的水解率是________ 。
(4)某淀粉的相对分子质量为13 932,则它是由________ 个葡萄糖分子缩合而成的。

(1)各步加入的试剂为(写化学式):A
(2)若加入A溶液不加入B溶液
(3)已知1 mol葡萄糖与新制Cu(OH)2悬浊液反应生成1 mol Cu2O,当生成1.44 g砖红色沉淀时,淀粉的水解率是
(4)某淀粉的相对分子质量为13 932,则它是由
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】可再生的生物质资源的应用是科学家研究的重大课题。我国科学家研发了葡萄糖的各种应用。
Ⅰ.淀粉是绿色植物光合作用的产物,淀粉在酸或酶的作用下水解,生成一系列产物,最终生成葡萄糖。
(1)写出淀粉在稀硫酸作催化剂发生水解反应的化学方程式____ 。
(2)某小组同学欲检验淀粉水解后产生葡萄糖,按如图进行实验,未观察到产生红色沉淀,原因是____ 。

Ⅱ.聚乳酸是一种可生物降解的高分子材料,主要用于制造可降解纤维、可降解塑料和医用材料。以葡萄糖为原料可以制备聚乳酸,相互转化关系如图:



(3)反应②的化学方程式为____ 。
(4)两分子的乳酸发生酯化反应可以生成六元环状化合物,写出该反应的化学方程式___ 。
Ⅲ.葡萄糖在不同的氧化剂作用下可以发生以下转化关系:
 →
→ →
→
已知A和B都不能发生银镜反应,且以下几类有机化合物被氧化的容易程度:RCHO>R—CH2OH>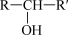 。
。
(5)A脱水可得到具有五元环状结构的酯C或具有六元环状结构的酯D,写出C的结构简式____ 。
(6)写出B的结构简式____ 。
Ⅰ.淀粉是绿色植物光合作用的产物,淀粉在酸或酶的作用下水解,生成一系列产物,最终生成葡萄糖。
(1)写出淀粉在稀硫酸作催化剂发生水解反应的化学方程式
(2)某小组同学欲检验淀粉水解后产生葡萄糖,按如图进行实验,未观察到产生红色沉淀,原因是

Ⅱ.聚乳酸是一种可生物降解的高分子材料,主要用于制造可降解纤维、可降解塑料和医用材料。以葡萄糖为原料可以制备聚乳酸,相互转化关系如图:
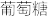



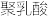
(3)反应②的化学方程式为
(4)两分子的乳酸发生酯化反应可以生成六元环状化合物,写出该反应的化学方程式
Ⅲ.葡萄糖在不同的氧化剂作用下可以发生以下转化关系:
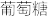 →
→ →
→
已知A和B都不能发生银镜反应,且以下几类有机化合物被氧化的容易程度:RCHO>R—CH2OH>
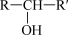 。
。(5)A脱水可得到具有五元环状结构的酯C或具有六元环状结构的酯D,写出C的结构简式
(6)写出B的结构简式
您最近半年使用:0次
【推荐2】淀粉是一种多糖,以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如图所示。
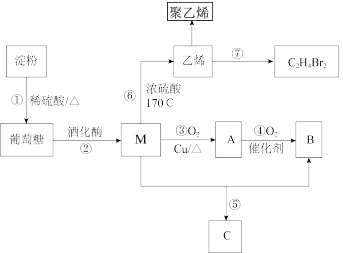
(1)葡萄糖的结构简式为____ 。
(2)M中的官能团的名称为____ ,⑦的反应类型是____ 。
(3)③的化学方程式是____ 。
(4)聚乙烯和聚丙烯都是生产塑料的合成树脂,写出由丙烯制备聚丙烯的化学方程式:____ 。
(5)⑤的化学方程式是____ 。
(6)C是一种油状、有香味的物质,实验室制取C的装置如图所示。
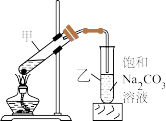
试管乙中饱和Na2CO3溶液的作用是____ 。

(1)葡萄糖的结构简式为
(2)M中的官能团的名称为
(3)③的化学方程式是
(4)聚乙烯和聚丙烯都是生产塑料的合成树脂,写出由丙烯制备聚丙烯的化学方程式:
(5)⑤的化学方程式是
(6)C是一种油状、有香味的物质,实验室制取C的装置如图所示。

试管乙中饱和Na2CO3溶液的作用是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】近年来,乳酸[CH3CH(OH)COOH]成为人们的研究热点之一。乳酸可由淀粉为原料,通过生物发酵法制备。

请回答下列有关问题:
(1)淀粉遇到单质碘呈__ 色。
(2)葡萄糖是自然界中分布最广的单糖,写出葡萄糖的结构简式__ 。
(3)在一定条件下,下列物质不能 与葡萄糖发生反应的是__ 。
a.溴水 b.NaOH溶液 c.Cu(OH)2悬浊液 d.CH3COOH
(4)乳酸在一定条件下可发生多种反应。例如:
①乳酸在一定条件下反应的产物可使Br2的CCl4溶液褪色,写出乳酸反应的化学方程式___ 。
②乳酸在一定条件下反应可生成六元环状化合物,写出该六元环状化合物的结构简式___ 。
③乳酸在一定条件下反应可生成高分子聚合物(聚乳酸),写出该反应的化学方程式___ 。
(5)1mol乳酸分别与足量的Na、Na2CO3、NaHCO3反应时,消耗三种物质的物质的量之比为__ 。

请回答下列有关问题:
(1)淀粉遇到单质碘呈
(2)葡萄糖是自然界中分布最广的单糖,写出葡萄糖的结构简式
(3)在一定条件下,下列物质
a.溴水 b.NaOH溶液 c.Cu(OH)2悬浊液 d.CH3COOH
(4)乳酸在一定条件下可发生多种反应。例如:
①乳酸在一定条件下反应的产物可使Br2的CCl4溶液褪色,写出乳酸反应的化学方程式
②乳酸在一定条件下反应可生成六元环状化合物,写出该六元环状化合物的结构简式
③乳酸在一定条件下反应可生成高分子聚合物(聚乳酸),写出该反应的化学方程式
(5)1mol乳酸分别与足量的Na、Na2CO3、NaHCO3反应时,消耗三种物质的物质的量之比为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】海洋中蕴含着丰富的资源。利用海水提取淡水、溴和镁的部分过程如图所示。
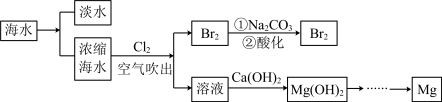
(1)海水淡化的方法有___________ 、离子交换法和电渗析法等。
(2)用纯碱吸收浓缩海水吹出的Br2:3Br2+ 6Na2CO3+3H2O=5NaBr + NaBrO3+6NaHCO3。若吸收3 mol Br2时,转移的电子是________ mol。
(3)海水中部分离子的含量如下:
其中,Mg2+的物质的量浓度是_____________ mol/L。若从100 L的海水中提取镁,理论上加入沉淀剂Ca(OH)2的质量是____________ g。
(4)由Mg(OH)2得到单质Mg,以下方法最合适的是__________ (填序号)。
A.Mg(OH)2 MgO
MgO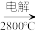 Mg
Mg
B.Mg(OH)2 MgO
MgO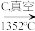 Mg
Mg
C.Mg(OH)2 无水MgCl2
无水MgCl2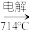 Mg
Mg
D.Mg(OH)2 MgCl2溶液
MgCl2溶液 Mg
Mg

(1)海水淡化的方法有
(2)用纯碱吸收浓缩海水吹出的Br2:3Br2+ 6Na2CO3+3H2O=5NaBr + NaBrO3+6NaHCO3。若吸收3 mol Br2时,转移的电子是
(3)海水中部分离子的含量如下:
| 成分 | 含量(mg/L) | 成分 | 含量(mg/L) |
| Na+ | 10560 | Cl- | 18980 |
| Mg2+ | 1272 | Br- | 64 |
| Ca2+ | 400 | SO42- | 2560 |
(4)由Mg(OH)2得到单质Mg,以下方法最合适的是
A.Mg(OH)2
 MgO
MgO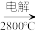 Mg
MgB.Mg(OH)2
 MgO
MgO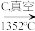 Mg
MgC.Mg(OH)2
 无水MgCl2
无水MgCl2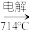 Mg
MgD.Mg(OH)2
 MgCl2溶液
MgCl2溶液 Mg
Mg
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】海洋是一座资源的宝库,下图是利用海洋资源生产卤素单质的工艺流程。
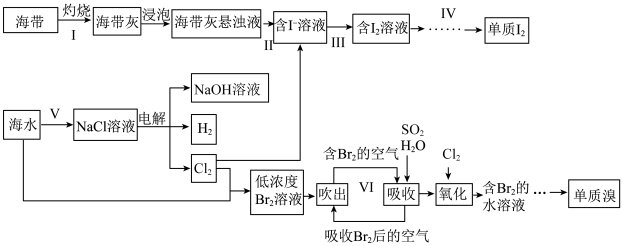
已知氧化性:
(1)实验室灼烧海带时,除三脚架、泥三角、酒精灯外,还需要用到的仪器是_______ ,步骤Ⅱ的操作名称为_______ 。
(2)步骤Ⅲ中需要严格控制 的用量,原因是
的用量,原因是_______ 。
(3)步骤Ⅳ中,采用萃取、分液、蒸馏等方法获得 。可用
。可用 作为含
作为含 溶液的萃取剂,原因是
溶液的萃取剂,原因是_______ (填标号)。
a. 不与
不与 反应 b.
反应 b. 与水互不相溶
与水互不相溶
c. 的密度比水大 d.
的密度比水大 d. 在CCl4中的溶解度比水更大
在CCl4中的溶解度比水更大
(4)步骤Ⅴ中,从海水提取的粗盐中主要含 、
、 、
、 等杂质离子,除去这些离子可加入的试剂有①盐酸②
等杂质离子,除去这些离子可加入的试剂有①盐酸② 溶液③
溶液③ 溶液④
溶液④ 溶液,加入试剂的正确顺序为
溶液,加入试剂的正确顺序为_______ (填标号)。
a.①②③④ b.②③④① c.③②④① d.②④③①
(5)步骤Ⅵ中,用 和水吸收
和水吸收 的离子方程式为
的离子方程式为_______ 。
(6)提取 的流程中,两次通入
的流程中,两次通入 的目的是富集浓缩溴。若最终获得240g
的目的是富集浓缩溴。若最终获得240g ,理论上需消耗标准状况下
,理论上需消耗标准状况下 的体积为
的体积为_______ 。

已知氧化性:

(1)实验室灼烧海带时,除三脚架、泥三角、酒精灯外,还需要用到的仪器是
(2)步骤Ⅲ中需要严格控制
 的用量,原因是
的用量,原因是(3)步骤Ⅳ中,采用萃取、分液、蒸馏等方法获得
 。可用
。可用 作为含
作为含 溶液的萃取剂,原因是
溶液的萃取剂,原因是a.
 不与
不与 反应 b.
反应 b. 与水互不相溶
与水互不相溶c.
 的密度比水大 d.
的密度比水大 d. 在CCl4中的溶解度比水更大
在CCl4中的溶解度比水更大(4)步骤Ⅴ中,从海水提取的粗盐中主要含
 、
、 、
、 等杂质离子,除去这些离子可加入的试剂有①盐酸②
等杂质离子,除去这些离子可加入的试剂有①盐酸② 溶液③
溶液③ 溶液④
溶液④ 溶液,加入试剂的正确顺序为
溶液,加入试剂的正确顺序为a.①②③④ b.②③④① c.③②④① d.②④③①
(5)步骤Ⅵ中,用
 和水吸收
和水吸收 的离子方程式为
的离子方程式为(6)提取
 的流程中,两次通入
的流程中,两次通入 的目的是富集浓缩溴。若最终获得240g
的目的是富集浓缩溴。若最终获得240g ,理论上需消耗标准状况下
,理论上需消耗标准状况下 的体积为
的体积为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】海水是巨大的资源宝库。下图是人类从海水资源获取某些重要化工原料的流程示意图。回答下列问题:
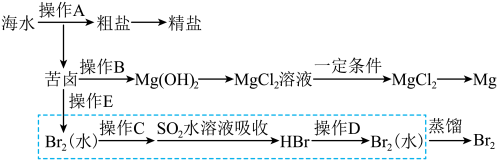
(1)操作A是___________ (填实验基本操作名称)。
(2)要知道海水晒盐的过程中溶液里食盐含量在逐渐提高的简易方法是___________ 。
A.分析氯化钠含量 B.测定溶液密度 C.观察是否有沉淀析出
(3)操作B需加入下列试剂中的一种,最合适的是___________。
(4)操作C是___________ ;上图中虚线框内流程的主要作用是___________ 。
(5)操作E中除了需要添加液氯外,还额外需要添加硫酸,但同样将需要添加上述试剂的操作D无需额外添加硫酸,其原因是___________ (用化学方程式表示原因)。
(6)已知苦卤的主要成分如下:
理论上,1L苦卤最多可得到 的质量为
的质量为___________ g。
(7)小乔by同学查阅资料后,向饱和食盐水由通入 和
和 ,发现产生了
,发现产生了 沉淀和
沉淀和 溶液。请书写相关的离子方程式
溶液。请书写相关的离子方程式___________ 。

(1)操作A是
(2)要知道海水晒盐的过程中溶液里食盐含量在逐渐提高的简易方法是
A.分析氯化钠含量 B.测定溶液密度 C.观察是否有沉淀析出
(3)操作B需加入下列试剂中的一种,最合适的是___________。
| A.氢氧化钠溶液 | B.澄清石灰水 | C.石灰乳 | D.碳酸钠溶液 |
(4)操作C是
(5)操作E中除了需要添加液氯外,还额外需要添加硫酸,但同样将需要添加上述试剂的操作D无需额外添加硫酸,其原因是
(6)已知苦卤的主要成分如下:
| 离子 |  |  |  |  |
浓度/( ) ) | 63.7 | 28.8 | 144.6 | 46.4 |
 的质量为
的质量为(7)小乔by同学查阅资料后,向饱和食盐水由通入
 和
和 ,发现产生了
,发现产生了 沉淀和
沉淀和 溶液。请书写相关的离子方程式
溶液。请书写相关的离子方程式
您最近半年使用:0次



