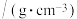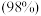名校
解题方法
1 . 下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
[实验目的]制取乙酸乙酯。
[实验原理]
(1)甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,该反应中浓硫酸的作用是_______ 。
[装置设计]甲、乙、丙三位同学分别设计了如下图所示三套实验装置:_______ (填“甲”或“乙”),反应方程式是_______ 。乙中导管a的作用为_______ 。丙同学将甲装置中的玻璃管改成了球形的干燥管,除了起上述作用外,另一重要作用是_______ 。
[实验步骤]
A.按所选择的装置组装仪器,在试管①中先加入3mL体积分数为95%的乙醇,并在摇动下缓缓加入2mL浓硫酸充分摇匀,冷却后再加入2mL冰醋酸。
B.将试管固定在铁架台上。
C.在试管②中加入5mL饱和Na2CO3溶液。
D.用酒精灯对试管①加热。
E.当观察到试管②中有明显现象时停止实验。
[问题讨论]
(3)步骤A组装好实验装置,加入样品前还应检查_______ 。
(4)试管②中观察到的现象是_______ 。
(5)试管②中饱和Na2CO3溶液的作用是_______ 。
[实验目的]制取乙酸乙酯。
[实验原理]
(1)甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,该反应中浓硫酸的作用是
[装置设计]甲、乙、丙三位同学分别设计了如下图所示三套实验装置:
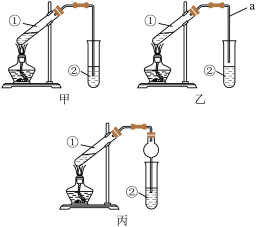
[实验步骤]
A.按所选择的装置组装仪器,在试管①中先加入3mL体积分数为95%的乙醇,并在摇动下缓缓加入2mL浓硫酸充分摇匀,冷却后再加入2mL冰醋酸。
B.将试管固定在铁架台上。
C.在试管②中加入5mL饱和Na2CO3溶液。
D.用酒精灯对试管①加热。
E.当观察到试管②中有明显现象时停止实验。
[问题讨论]
(3)步骤A组装好实验装置,加入样品前还应检查
(4)试管②中观察到的现象是
(5)试管②中饱和Na2CO3溶液的作用是
您最近半年使用:0次
名校
解题方法
2 . 某化学兴趣小组设计实验利用苯甲酸(沸点249℃)和异丙醇(沸点82℃)制备苯甲酸异丙酯(沸点218℃),实验装置如图:
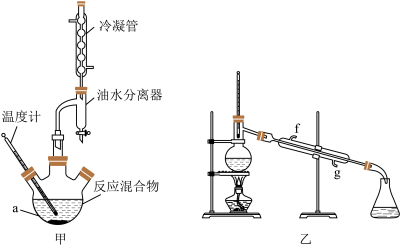
| A.在仪器a中加入三种试剂的先后顺序是:浓硫酸、异丙醇、苯甲酸 |
| B.实验采用水浴加热,若温度过高会使产率减小 |
| C.加入的苯甲酸和异丙醇中,需过量的是苯甲酸 |
| D.步骤③操作时应收集218℃的馏分,如果温度计水银球偏下,则收集的精制产品中可能混有的杂质为苯甲酸 |
您最近半年使用:0次
名校
解题方法
3 . 丙炔酸甲酯(CH≡C-COOCH3)是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为CH≡C-COOH+CH3OH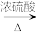 CH≡C-COOCH3+H2O。
CH≡C-COOCH3+H2O。
实验步骤如下:
步骤1:在反应瓶中,加入14.00 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
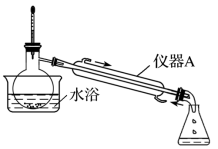
步骤2:蒸出过量的甲醇(装置如图)。
步骤3:反应液冷却后,依次用饱和NaCl溶液、5% Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯10.08 g。___________ 。
(2)步骤2中,如图所示的装置中仪器A的名称是___________ ;蒸馏烧瓶中加入碎瓷片的目的是___________ 。
(3)步骤3中,用5% Na2CO3溶液洗涤,主要除去的物质是___________ ;分离出有机相的操作名称为___________ 。
(4)步骤4中,蒸馏时不能用水浴加热的原因是___________ 。
(5)实验中丙炔酸甲酯的产率为___________ 。
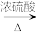 CH≡C-COOCH3+H2O。
CH≡C-COOCH3+H2O。实验步骤如下:
步骤1:在反应瓶中,加入14.00 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
步骤2:蒸出过量的甲醇(装置如图)。
步骤3:反应液冷却后,依次用饱和NaCl溶液、5% Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯10.08 g。
(2)步骤2中,如图所示的装置中仪器A的名称是
(3)步骤3中,用5% Na2CO3溶液洗涤,主要除去的物质是
(4)步骤4中,蒸馏时不能用水浴加热的原因是
(5)实验中丙炔酸甲酯的产率为
您最近半年使用:0次
4 . 根据实验操作及现象,下列结论中正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 用铂丝蘸取NaCl溶液,在酒精灯外焰上灼烧,火焰呈现黄色 | 灼烧过程中NaCl一定发生了化学变化 |
| B | 取少量某 溶液于试管中,滴入几滴KSCN溶液。溶液呈现红色 溶液于试管中,滴入几滴KSCN溶液。溶液呈现红色 | 该 溶液已经不含有 溶液已经不含有 |
| C | 在乙酸乙酯的制备实验中,将产生的蒸气导入足量的饱和碳酸钠溶液上方,充分反应后上层存在油状液体 | 该油状液体为乙酸乙酯 |
| D | 将一定量的铜片,加入试管中的某硝酸溶液中,可观察到有红棕色气体生成 | 所产生的气体中,只可能有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 乙酸乙酯是一种重要的化工原料。查阅资料得到下列数据:
请回答:
(1)实验室常用下图装置来制备乙酸乙酯。______ ;浓硫酸对反应有催化作用,但加入的浓硫酸不能太多也不能太少,原因是______ 。
②防止加热时液体暴沸,需要在试管加入碎瓷片,如果加热一段时间后发现忘记了加碎瓷片,应该采取的正确操作是______ 。
A. 立即补加 B. 冷却后补加 C. 不需补加 D. 重新配料
(2)产品纯化。分液法从试管B中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,首先向乙酸乙酯中加入无水氯化钙,除去__________ (填名称);然后再加入无水硫酸钠除去水,最后进行__________ (填操作名称)得到较纯净的乙酸乙酯。
(3)该实验中用 乙酸与
乙酸与 乙醇反应,如果实际得到的乙酸乙酯的质量是
乙醇反应,如果实际得到的乙酸乙酯的质量是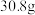 ,则该实验中乙酸乙酯的产率是
,则该实验中乙酸乙酯的产率是________ 。(产率指的是某种生成物的实际产量与理论产量的比值)
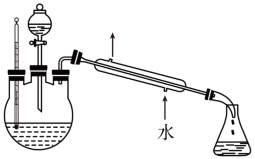
(4)另一化学小组设计下图所示的装置制取乙酸乙酯(铁架台、铁夹、加热装置均已略去)。此装置和上图装置相比的优点是________ (写出一条即可)。
物质 | 沸点 | 密度 | 相对分子质量 | 水溶性 |
乙醇 | 78.0 | 0.8 | 46 | 互溶 |
乙酸 | 118.0 | 1.1 | 60 | 可溶 |
乙酸乙酯 | 77.5 | 0.9 | 88 | 微溶 |
乙醚 |
| 0.7 | 74 | 微溶 |
浓硫酸 | 338.0 | 1.8 | 98 | 易溶 |
无水氯化钙 | 可与乙醇形成难溶于水的 | |||
(1)实验室常用下图装置来制备乙酸乙酯。
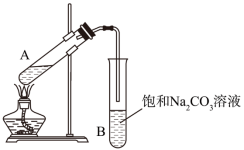
②防止加热时液体暴沸,需要在试管加入碎瓷片,如果加热一段时间后发现忘记了加碎瓷片,应该采取的正确操作是
A. 立即补加 B. 冷却后补加 C. 不需补加 D. 重新配料
(2)产品纯化。分液法从试管B中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,首先向乙酸乙酯中加入无水氯化钙,除去
(3)该实验中用
 乙酸与
乙酸与 乙醇反应,如果实际得到的乙酸乙酯的质量是
乙醇反应,如果实际得到的乙酸乙酯的质量是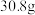 ,则该实验中乙酸乙酯的产率是
,则该实验中乙酸乙酯的产率是(4)另一化学小组设计下图所示的装置制取乙酸乙酯(铁架台、铁夹、加热装置均已略去)。此装置和上图装置相比的优点是
您最近半年使用:0次
名校
6 . 乙酰乙酸乙酯是有机合成的中间体,用乙酸乙酯合成乙酰乙酸乙酯的原理如下:
已知:乙酰乙酸乙酯在95℃开始分解。
现用市售乙酸乙酯(含2%乙醇)合成乙酰乙酸乙酯的步骤如下:
①制备钠珠:将1.0g金属 迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
③酸化:向橘红色溶液中加入50%醋酸使其呈弱酸性( )。
)。
④分液:将反应液转入分液漏斗,加入等体积的饱和氯化钠溶液,振摇,静置,分液。将有机层倒入锥形瓶中,并加适量的无水 充分振荡静置后过滤。
充分振荡静置后过滤。
⑤蒸馏:将步骤④所得有机混合液水浴加热蒸馏出未反应的乙酸乙酯,停止蒸馏,冷却。再将蒸馏得到的剩余物进行减压蒸馏,收集馏分。
回答下列问题:
(1)步骤①中溶剂A最好选择___________ (填标号)。
a.乙醇 b.水 c.二甲苯 d.苯
(2)制备钠珠采用步骤①中操作方法的原因是___________ 。
(3)分离回收溶剂A采用的方法是___________ (填标号)。
a.蒸馏 b.分液 c.蒸发 d.倾倒法
(4)乙醇钠是制备乙酰乙酸乙酯的催化剂,写出生成乙醇钠的化学方程式___________ ,乙酸乙酯中乙醇含量过少或过多均不利于乙酰乙酸乙酯的生成,原因是___________ 。
(5)步骤④中加入饱和氯化钠溶液的目的是___________ 。
(6)下列仪器在步骤⑤中无需使用的是___________ (填名称);采用减压蒸馏获得乙酰乙酸乙酯的原因___________ 。
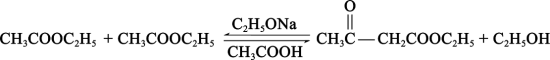
| 名称 | 熔点/℃ | 沸点/℃ | 密度/ | 溶解度 | ||
 | 乙醇 | 乙醚 | ||||
| 苯 | 5.5 | 80.1 | 0.88 | 不溶 | 互溶 | 互溶 |
| 二甲苯 | -25.18 | 144.4 | 0.8802 | 不溶 | 互溶 | 互溶 |
| 乙酸乙酯 | -83.6 | 77.1 | 0.9003 | 难溶 | 互溶 | 互溶 |
| 金属钠 | 97.82 | 881.4 | 0.968 | 反应 | 反应 | 不溶 |
| 乙酰乙酸乙酯 | <-80 | 180.4 | 1.0282 | 微溶 | 互溶 | 互溶 |
现用市售乙酸乙酯(含2%乙醇)合成乙酰乙酸乙酯的步骤如下:
①制备钠珠:将1.0g金属
 迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。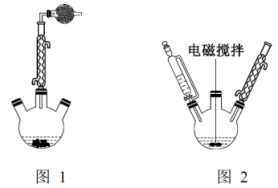
③酸化:向橘红色溶液中加入50%醋酸使其呈弱酸性(
 )。
)。④分液:将反应液转入分液漏斗,加入等体积的饱和氯化钠溶液,振摇,静置,分液。将有机层倒入锥形瓶中,并加适量的无水
 充分振荡静置后过滤。
充分振荡静置后过滤。⑤蒸馏:将步骤④所得有机混合液水浴加热蒸馏出未反应的乙酸乙酯,停止蒸馏,冷却。再将蒸馏得到的剩余物进行减压蒸馏,收集馏分。
回答下列问题:
(1)步骤①中溶剂A最好选择
a.乙醇 b.水 c.二甲苯 d.苯
(2)制备钠珠采用步骤①中操作方法的原因是
(3)分离回收溶剂A采用的方法是
a.蒸馏 b.分液 c.蒸发 d.倾倒法
(4)乙醇钠是制备乙酰乙酸乙酯的催化剂,写出生成乙醇钠的化学方程式
(5)步骤④中加入饱和氯化钠溶液的目的是
(6)下列仪器在步骤⑤中无需使用的是

您最近半年使用:0次
7 . 实验室制乙酸乙酯的主要装置如图中A所示,主要步骤如下:9.实验室制取乙酸正丁酯(沸点:126℃,反应温度115-120℃)的装置如图所示,将冰醋酸(沸点118℃)、正丁醇(沸点118℃)、浓硫酸混合物装入三颈烧瓶中加热,最后将分水器中的酯层与烧瓶中反应物混合后分离提纯得到产品,对该实验的说法错误的是


| A.使用分水器可以提高乙酸正丁酯的产率 |
| B.分离提纯时的洗涤操作在分液漏斗中进行 |
| C.反应开始后发现A装置中没加碎瓷片,应该立即补加以防暴沸 |
| D.用饱和Na2CO3溶液可洗去混合液中的酸性物质 |
您最近半年使用:0次
名校
8 . Ⅰ.某研究小组利用无水乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如下图所示,请回答:
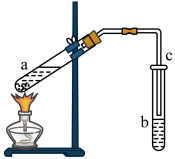
(1)利用无水乙醇、乙酸和浓硫酸制取乙酸乙酯反应的化学方程式为:___________ 。
(2)实验时下列做法正确的是_______ (填序号)
A.先加入浓硫酸,然后边振荡边加入乙醇和乙酸
B.试管a中应加入碎瓷片
C.试管b中应加入饱和 溶液
溶液
D.导管c下端管口不能伸入试管b的溶液中
E.加入过量无水乙醇,可以使乙酸完全反应
F.可以用稀硫酸代替浓硫酸
(3)试管b中溶液作用是:吸收乙醇、_______ 和________ 。
Ⅱ.某有机物G的合成路线如下
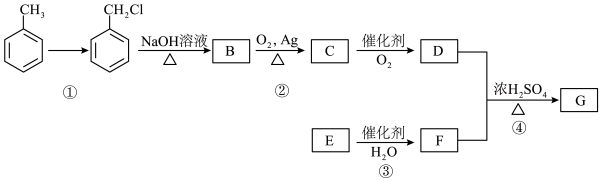
已知:①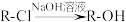 (R代表烃基,下同)
(R代表烃基,下同)
②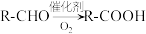
③E的产量可衡量一个国家石油化工的发展水平
回答下列问题:
(4)反应①的反应物(除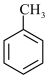 外)及反应条件分别是
外)及反应条件分别是_______ 、________ 。
(5)B中所含官能团名称为________ ;G的结构简式为_______ 。
(6)反应②的化学方程式为________ ,属于氧化反应。
(7)写出分子式为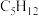 且一氯代物只有1种的有机物的结构简式
且一氯代物只有1种的有机物的结构简式________ ,该有机物的习惯命名是_______ 。

(1)利用无水乙醇、乙酸和浓硫酸制取乙酸乙酯反应的化学方程式为:
(2)实验时下列做法正确的是
A.先加入浓硫酸,然后边振荡边加入乙醇和乙酸
B.试管a中应加入碎瓷片
C.试管b中应加入饱和
 溶液
溶液 D.导管c下端管口不能伸入试管b的溶液中
E.加入过量无水乙醇,可以使乙酸完全反应
F.可以用稀硫酸代替浓硫酸
(3)试管b中溶液作用是:吸收乙醇、
Ⅱ.某有机物G的合成路线如下

已知:①
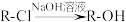 (R代表烃基,下同)
(R代表烃基,下同)②
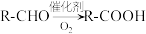
③E的产量可衡量一个国家石油化工的发展水平
回答下列问题:
(4)反应①的反应物(除
 外)及反应条件分别是
外)及反应条件分别是(5)B中所含官能团名称为
(6)反应②的化学方程式为
(7)写出分子式为
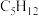 且一氯代物只有1种的有机物的结构简式
且一氯代物只有1种的有机物的结构简式
您最近半年使用:0次
名校
解题方法
9 . 实验室将乙酸、正丁醇、浓硫酸加入圆底烧瓶中,加热条件下制备乙酸正丁酯的装置(加热和夹持装置已省略)和有关信息如下:
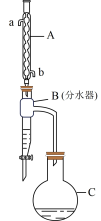
下列说法正确的是
乙酸 | 正丁醇 | 乙酸正丁酯 | |
熔点/℃ | 16.6 | -89.5 | -73.5 |
沸点/℃ | 117.9 | 117 | 126.0 |
密度( | 1.1 | 0.80 | 0.88 |

下列说法正确的是
| A.应从A的a口通入冷凝水 |
| B.浓硫酸在该反应中起催化剂的作用,可以改变反应热从而提高化学反应速率 |
| C.装置B的作用是不断分离出产生的水,使反应向正向移动,提高产率 |
| D.提纯乙酸正丁酯可采取水洗、氢氧化钠溶液洗、无水氯化钙干燥、过滤一系列操作 |
您最近半年使用:0次
名校
解题方法
10 . 某化学兴趣小组同学利用如图所示装置进行乙酸乙酯的制备实验,回答下列问题:______ 。
(2)往试管a中加入一定量的试剂时,加入次序正确的是______ (填标号)。
A.乙醇→浓硫酸→冰醋酸
B.浓硫酸→乙醇→冰醋酸
C.冰醋酸→乙醇→浓硫酸
(3)试管b中所盛装的试剂为______(填标号),该试剂的作用有______。
(4)试管b处的导管______ (填“能”或“不能”)伸入液面以下,原因为______ 。
(5)试管a中发生反应的化学方程式为______ ,每消耗0.1mol乙醇,此时生成的乙酸乙酯的质量为______ g。

(2)往试管a中加入一定量的试剂时,加入次序正确的是
A.乙醇→浓硫酸→冰醋酸
B.浓硫酸→乙醇→冰醋酸
C.冰醋酸→乙醇→浓硫酸
(3)试管b中所盛装的试剂为______(填标号),该试剂的作用有______。
| A.稀硫酸 | B.饱和氢氧化钠溶液 |
| C.饱和碳酸钠溶液 | D.澄清石灰水 |
(4)试管b处的导管
(5)试管a中发生反应的化学方程式为
您最近半年使用:0次
2024-04-02更新
|
45次组卷
|
2卷引用:河北省保定市清苑中学等校2023-2024学年高二下学期3月月考化学试题