海洋中蕴含着丰富的资源。利用海水提取淡水、溴和镁的部分过程如图所示。
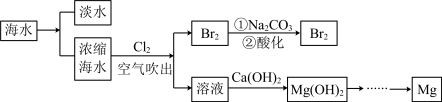
(1)海水淡化的方法有___________ 、离子交换法和电渗析法等。
(2)用纯碱吸收浓缩海水吹出的Br2:3Br2+ 6Na2CO3+3H2O=5NaBr + NaBrO3+6NaHCO3。若吸收3 mol Br2时,转移的电子是________ mol。
(3)海水中部分离子的含量如下:
其中,Mg2+的物质的量浓度是_____________ mol/L。若从100 L的海水中提取镁,理论上加入沉淀剂Ca(OH)2的质量是____________ g。
(4)由Mg(OH)2得到单质Mg,以下方法最合适的是__________ (填序号)。
A.Mg(OH)2 MgO
MgO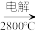 Mg
Mg
B.Mg(OH)2 MgO
MgO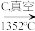 Mg
Mg
C.Mg(OH)2 无水MgCl2
无水MgCl2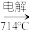 Mg
Mg
D.Mg(OH)2 MgCl2溶液
MgCl2溶液 Mg
Mg

(1)海水淡化的方法有
(2)用纯碱吸收浓缩海水吹出的Br2:3Br2+ 6Na2CO3+3H2O=5NaBr + NaBrO3+6NaHCO3。若吸收3 mol Br2时,转移的电子是
(3)海水中部分离子的含量如下:
| 成分 | 含量(mg/L) | 成分 | 含量(mg/L) |
| Na+ | 10560 | Cl- | 18980 |
| Mg2+ | 1272 | Br- | 64 |
| Ca2+ | 400 | SO42- | 2560 |
(4)由Mg(OH)2得到单质Mg,以下方法最合适的是
A.Mg(OH)2
 MgO
MgO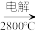 Mg
MgB.Mg(OH)2
 MgO
MgO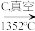 Mg
MgC.Mg(OH)2
 无水MgCl2
无水MgCl2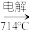 Mg
MgD.Mg(OH)2
 MgCl2溶液
MgCl2溶液 Mg
Mg
更新时间:2017-07-13 19:38:09
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】孔雀石的主要成分为CuCO3·Cu(OH)2。某同学设计从孔雀石中冶炼铜的方案如下:

回答下列问题:
(1)将孔雀石粉碎的目的是_________ ,加入过量稀硫酸,可观察到的现象是_________ 。
(2)操作a的名称是________ ,在滤液中加入过量铁粉发生的反应有_______ 、________ (用离子方程式表示)。
(3)A的化学式为_________ ,在悬浊液中加入A的目的是___________ 。
(4)从滤液中获得铜的另外一种方案是:2CuSO4+ 2H2O 2Cu+O2↑+2H2SO4。现有111 kgCuCO3·Cu(OH)2,通过这种方案理论上可以制取
2Cu+O2↑+2H2SO4。现有111 kgCuCO3·Cu(OH)2,通过这种方案理论上可以制取_________ kg铜。
(5)请你根据提供的试剂,设计由孔雀石冶炼铜的另外一种方案(请用简洁的文字说明)__________ 。(可供选择试剂:铁粉、稀硫酸)

回答下列问题:
(1)将孔雀石粉碎的目的是
(2)操作a的名称是
(3)A的化学式为
(4)从滤液中获得铜的另外一种方案是:2CuSO4+ 2H2O
 2Cu+O2↑+2H2SO4。现有111 kgCuCO3·Cu(OH)2,通过这种方案理论上可以制取
2Cu+O2↑+2H2SO4。现有111 kgCuCO3·Cu(OH)2,通过这种方案理论上可以制取(5)请你根据提供的试剂,设计由孔雀石冶炼铜的另外一种方案(请用简洁的文字说明)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】(1)古代的“药金”外观与金相似,常被误认为是金子。其冶炼方法如下:将碳酸锌、赤铜(Cu2O)、木炭按一定比例混合加热到800℃,即得金光闪闪的“药金”。
①“药金”的主要成分是__ (填化学式)。
②有关冶炼的化学方程式是__ 。
(2)某地出产的孔雀石的主要成分是Cu2(OH)2CO3。
①试写出该孔雀石在加热条件下分解的化学方程式:__ 。
②试以①中所得金属氧化物为原料,分别采用湿法冶炼和高温冶炼的方法制取金属铜。供选择的试剂有木炭、铁屑、生石灰、稀硫酸,不得另选其他试剂。写出两种方法制取金属铜的化学方程式。
a.湿法冶炼:__ 、__ (可不填满,也可补充,下同)。
b.高温冶炼:__ 。
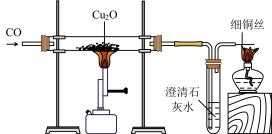
(3)利用一氧化碳还原赤铜矿(Cu2O)冶炼铜。实验室可用如图所示装置进行实验,当硬质玻璃管中的反应结束时,应进行的实验操作是___ 。
(4)利用辉铜矿(Cu2S)冶炼铜的原理如下:
Ⅰ.取一定质量的Cu2S在空气中高温焙烧,完全反应后生成一种铜的氧化物和二氧化硫;
Ⅱ.再取上述一半质量的Cu2S,与Ⅰ中生成的铜的氧化物混合均匀,隔绝空气高温煅烧,恰好完全反应,生成铜和二氧化硫。结合质量守恒定律,推断这种铜的氧化物的化学式为__ 。
①“药金”的主要成分是
②有关冶炼的化学方程式是
(2)某地出产的孔雀石的主要成分是Cu2(OH)2CO3。
①试写出该孔雀石在加热条件下分解的化学方程式:
②试以①中所得金属氧化物为原料,分别采用湿法冶炼和高温冶炼的方法制取金属铜。供选择的试剂有木炭、铁屑、生石灰、稀硫酸,不得另选其他试剂。写出两种方法制取金属铜的化学方程式。
a.湿法冶炼:
b.高温冶炼:
(3)利用一氧化碳还原赤铜矿(Cu2O)冶炼铜。实验室可用如图所示装置进行实验,当硬质玻璃管中的反应结束时,应进行的实验操作是

(4)利用辉铜矿(Cu2S)冶炼铜的原理如下:
Ⅰ.取一定质量的Cu2S在空气中高温焙烧,完全反应后生成一种铜的氧化物和二氧化硫;
Ⅱ.再取上述一半质量的Cu2S,与Ⅰ中生成的铜的氧化物混合均匀,隔绝空气高温煅烧,恰好完全反应,生成铜和二氧化硫。结合质量守恒定律,推断这种铜的氧化物的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】明代《天工开物》记载了“火法”炼锌方法:“炉甘石(碳酸锌)十斤,装载入一泥罐内,然后逐层用煤炭饼垫盛,…,发火煅红,…,毁罐取出,即倭铅也”。现代工业开发了用NH3—NH4Cl水溶液浸出氧化锌烟灰(主要成分为ZnO 、Pb、CuO和As2O3)制取高纯锌的工艺流程如图所示。

已知浸出液含[Zn(NH3)4]2+、[Cu(NH3)4]2+、AsCl 。
。
(1)《天工开物》记载的炼锌方法要求罐体用泥封严,目的是___________ 。
(2)滤渣1的主要成分是___________ (填化学式)。一段时间内锌浸出率与温度的关系如图所示,分析出现该现象的原因___________ 。

(3) “氧化除杂”的目的是将AsCl 转化为As2O5胶体,再经吸附聚沉除去,溶液始终接近中性,该反应的离子方程式是
转化为As2O5胶体,再经吸附聚沉除去,溶液始终接近中性,该反应的离子方程式是___________ 。
(4) “电解”含[Zn(NH3)4]2+的溶液,阴极电极反应式是___________ 。阳极区产生一种无色无味的气体,将其通入滴有KSCN的FeCl2溶液中,无明显现象,该气体是___________ (填化学式)。
(5) ZnCl2溶液在T1℃水解可得某碱式盐,取11.38g该碱式盐,T2℃完全水解后并煅烧,可得纯氧化锌8.1g。则该碱式盐的化学式为___________ 。

已知浸出液含[Zn(NH3)4]2+、[Cu(NH3)4]2+、AsCl
 。
。(1)《天工开物》记载的炼锌方法要求罐体用泥封严,目的是
(2)滤渣1的主要成分是

(3) “氧化除杂”的目的是将AsCl
 转化为As2O5胶体,再经吸附聚沉除去,溶液始终接近中性,该反应的离子方程式是
转化为As2O5胶体,再经吸附聚沉除去,溶液始终接近中性,该反应的离子方程式是(4) “电解”含[Zn(NH3)4]2+的溶液,阴极电极反应式是
(5) ZnCl2溶液在T1℃水解可得某碱式盐,取11.38g该碱式盐,T2℃完全水解后并煅烧,可得纯氧化锌8.1g。则该碱式盐的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】溴及其化合物广泛用于医药、塑料阻燃剂等。溴主要以 形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程如下:
形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程如下:
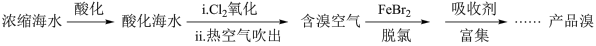
(1)酸化:将海水酸化的主要目的是避免___________ (填离子反应方程式)。
(2)脱氯:除去含溴空气中残留的
①具有脱氯作用的离子是___________ 。
②溶液失去脱氯作用后,补加 或加入
或加入___________ ,脱氯作用恢复。
③富集、制取 :
: 吸收了
吸收了 后,
后, 歧化为
歧化为 和
和 。则
。则 是
是___________ (填字母)。
a、 溶液 b、
溶液 b、 溶液 c、
溶液 c、 气体
气体
(3)再用 酸化歧化后的溶液得到
酸化歧化后的溶液得到 ,其离子反应方程式为
,其离子反应方程式为___________ 。
(4)探究 溶液与
溶液与 溶液反应时
溶液反应时 浓度对生成
浓度对生成 的影响,实验如下:
的影响,实验如下:
① 中溶液呈棕红色说明产生了
中溶液呈棕红色说明产生了___________ 。
②分析C中溶液颜色变浅的原因,甲同学认为是发生了化学反应所致;乙同学认为是用水稀释所致。若认为甲同学的分析合理,请用具体的反应说明理由;若认为乙同学的分析合理,进一步设计实验方案说明。理由或方案:___________ 。
③酸化歧化后的溶液宜选用的酸是___________ (填“稀硫酸”或“浓硫酸”)。
 形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程如下:
形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程如下: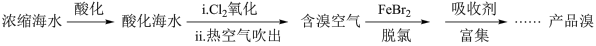
(1)酸化:将海水酸化的主要目的是避免
(2)脱氯:除去含溴空气中残留的

①具有脱氯作用的离子是
②溶液失去脱氯作用后,补加
 或加入
或加入③富集、制取
 :
: 吸收了
吸收了 后,
后, 歧化为
歧化为 和
和 。则
。则 是
是a、
 溶液 b、
溶液 b、 溶液 c、
溶液 c、 气体
气体(3)再用
 酸化歧化后的溶液得到
酸化歧化后的溶液得到 ,其离子反应方程式为
,其离子反应方程式为(4)探究
 溶液与
溶液与 溶液反应时
溶液反应时 浓度对生成
浓度对生成 的影响,实验如下:
的影响,实验如下:| 序号 | A | B | C |
| 试剂组成 | 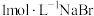 溶液 溶液 | 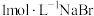 溶液 溶液 | 将B中反应后溶液 |
20% | 98% | 用水稀释 | |
| 实验现象 | 无明显现象 | 溶液呈棕红色放热 | 溶液颜色变得很浅 |
①
 中溶液呈棕红色说明产生了
中溶液呈棕红色说明产生了②分析C中溶液颜色变浅的原因,甲同学认为是发生了化学反应所致;乙同学认为是用水稀释所致。若认为甲同学的分析合理,请用具体的反应说明理由;若认为乙同学的分析合理,进一步设计实验方案说明。理由或方案:
③酸化歧化后的溶液宜选用的酸是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图:

(1)步骤①反应的离子方程式是___________________ 。
(2)步骤③反应的化学方程式是___________________ ,从理论上考虑,下列也能吸收Br2的是___________________ 。
A.FeCl2 B.Na2SO3 C.H2O
(3)步骤①中已获得Br2,步骤③中又将Br2还原为Br-,步骤④又生成Br2,这样做的目的为___________________ 。
(4)已知海水中Br-含量为64mg/L,依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为___________________ L(忽略Cl2的溶解)。

(1)步骤①反应的离子方程式是
(2)步骤③反应的化学方程式是
A.FeCl2 B.Na2SO3 C.H2O
(3)步骤①中已获得Br2,步骤③中又将Br2还原为Br-,步骤④又生成Br2,这样做的目的为
(4)已知海水中Br-含量为64mg/L,依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:
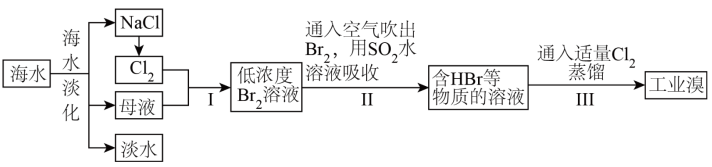
(1)请列举海水淡化的三种方法:_______ 。
(2)用惰性电极,将 溶液进行电解,写出化学方程式
溶液进行电解,写出化学方程式_______ 。
(3)步骤I中已获得 ,步骤II中将
,步骤II中将 还原为
还原为 ,其目的为
,其目的为_______ 。
(4)步骤II用 水溶液吸收
水溶液吸收 ,吸收率可达
,吸收率可达 ,有关反应的离子方程式为
,有关反应的离子方程式为_______ ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_______ 。
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料, 的沸点为
的沸点为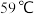 。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,做了如下装置简图:
。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,做了如下装置简图:

请你参与分析讨论:
①图中仪器 的名称:
的名称:_______ 。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是_______ 。
③为除去该产物中仍残留的少量 ,可向其中加入
,可向其中加入 溶液,充分反应后,再进行的分离操作是
溶液,充分反应后,再进行的分离操作是_______ 。

(1)请列举海水淡化的三种方法:
(2)用惰性电极,将
 溶液进行电解,写出化学方程式
溶液进行电解,写出化学方程式(3)步骤I中已获得
 ,步骤II中将
,步骤II中将 还原为
还原为 ,其目的为
,其目的为(4)步骤II用
 水溶液吸收
水溶液吸收 ,吸收率可达
,吸收率可达 ,有关反应的离子方程式为
,有关反应的离子方程式为(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,
 的沸点为
的沸点为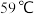 。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,做了如下装置简图:
。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,做了如下装置简图:
请你参与分析讨论:
①图中仪器
 的名称:
的名称:②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是
③为除去该产物中仍残留的少量
 ,可向其中加入
,可向其中加入 溶液,充分反应后,再进行的分离操作是
溶液,充分反应后,再进行的分离操作是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务。如图是某工厂海水综合利用的流程图。
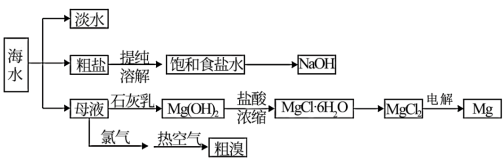
请根据以上信息回答下列问题:
(1)请列举一种海水淡化的方法__ 。
(2)粗盐中含有Ca2+、Mg2+、SO 等杂质,精制时所用试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,添加以上试剂合理的顺序是
等杂质,精制时所用试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,添加以上试剂合理的顺序是__ (填字母)。
A.②③④① B.③④②① C.④③②① D.③②①④
(3)以电解饱和食盐水为基础制取氯气、烧碱等产品的工业称为氯碱工业,请写出该反应的化学方程式___ 。
(4)请写出提取镁过程中Mg(OH)2与盐酸反应的离子方程式___ 。
(5)将氯气通入母液中,可将溶液中的溴离子转化为溴单质,请写出该反应的离子方程式__ 。以下是为该工厂氯气寻找货源的设想,其中较合理的是__ (填字母)。
A.从外地购买
B.在当地新建生产厂
C.从本厂生产烧碱处循环
D.从本厂生产镁单质处循环

请根据以上信息回答下列问题:
(1)请列举一种海水淡化的方法
(2)粗盐中含有Ca2+、Mg2+、SO
 等杂质,精制时所用试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,添加以上试剂合理的顺序是
等杂质,精制时所用试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,添加以上试剂合理的顺序是A.②③④① B.③④②① C.④③②① D.③②①④
(3)以电解饱和食盐水为基础制取氯气、烧碱等产品的工业称为氯碱工业,请写出该反应的化学方程式
(4)请写出提取镁过程中Mg(OH)2与盐酸反应的离子方程式
(5)将氯气通入母液中,可将溶液中的溴离子转化为溴单质,请写出该反应的离子方程式
A.从外地购买
B.在当地新建生产厂
C.从本厂生产烧碱处循环
D.从本厂生产镁单质处循环
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海水资源的利用具有非常广阔的前景。下面是海水综合利用联合工业体系的简图:

回答下列问题:
Ⅰ.海水淡化
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法有_______ 。(写出一种即可)
Ⅱ.海水制盐
(2)过程Ⅰ采用的操作是_______ ;
(3)粗盐中可溶性的杂质离子主要有 、
、 、
、 。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、
。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、 溶液、
溶液、 溶液、盐酸,其中
溶液、盐酸,其中 溶液的作用是
溶液的作用是_______ 。
Ⅲ.海水提溴
(4)工业上从海水中提取溴单质的流程图中,步骤④的离子方程式为_______ ;从理论上考虑下列也能吸收 的是
的是_______ 。
A.NaCl B. C.
C. D.
D.
(5)经过步骤①②已获得 ,不直接用含
,不直接用含 的海水进行蒸馏得到液溴,而要经过“空气吹出、
的海水进行蒸馏得到液溴,而要经过“空气吹出、 吸收、通入氯气”后再蒸馏,其目的是
吸收、通入氯气”后再蒸馏,其目的是_______ ;
Ⅳ.海水提镁
(6)该工业生产过程中,为了使 转化为
转化为 ,应加入的试剂为
,应加入的试剂为_______ ;
(7)写出电解 冶炼金属Mg的化学方程式
冶炼金属Mg的化学方程式_______ 。

回答下列问题:
Ⅰ.海水淡化
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法有
Ⅱ.海水制盐
(2)过程Ⅰ采用的操作是
(3)粗盐中可溶性的杂质离子主要有
 、
、 、
、 。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、
。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、 溶液、
溶液、 溶液、盐酸,其中
溶液、盐酸,其中 溶液的作用是
溶液的作用是Ⅲ.海水提溴
(4)工业上从海水中提取溴单质的流程图中,步骤④的离子方程式为
 的是
的是A.NaCl B.
 C.
C. D.
D.
(5)经过步骤①②已获得
 ,不直接用含
,不直接用含 的海水进行蒸馏得到液溴,而要经过“空气吹出、
的海水进行蒸馏得到液溴,而要经过“空气吹出、 吸收、通入氯气”后再蒸馏,其目的是
吸收、通入氯气”后再蒸馏,其目的是Ⅳ.海水提镁
(6)该工业生产过程中,为了使
 转化为
转化为 ,应加入的试剂为
,应加入的试剂为(7)写出电解
 冶炼金属Mg的化学方程式
冶炼金属Mg的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】海洋资源的利用具有广阔前景。
(1)海水淡化的方法有_____ (选填一种即可)。
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是____ 。
(3)下图是从海水中提取镁的简单流程。
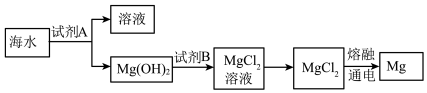
工业上常用于沉淀Mg2+的试剂A 的俗名是___ ,Mg(OH)2转化为MgCl2的离子方程式是_______ 。
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:
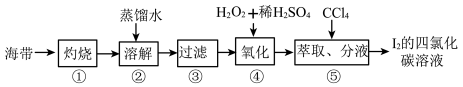
①灼烧海带至灰烬时所用的主要仪器名称是_______ 。步骤②加热煮沸一会的目的是______________ 。
② 步骤④向滤液中加H2O2和稀H2SO4溶液,写出该反应的离子方程式_______________ 。反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈____________ 色。
(1)海水淡化的方法有
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是
(3)下图是从海水中提取镁的简单流程。

工业上常用于沉淀Mg2+的试剂A 的俗名是
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是
② 步骤④向滤液中加H2O2和稀H2SO4溶液,写出该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】海水是巨大的资源宝库:

(1)操作A是_______ 、过滤(填实验基本操作名称)
(2)除去粗盐中杂质( 、
、 、
、 ),加入的药品顺序正确的是_______。
),加入的药品顺序正确的是_______。
(3)虚线框中已获得 ,而后又将
,而后又将 还原为
还原为 ,其目的是
,其目的是_______ 。写出操作C中发生反应的离子方程式:_______ 。
(4)工业上也可以用 溶液吸收吹出的
溶液吸收吹出的 ,生成溴化钠和溴酸钠,同时放出
,生成溴化钠和溴酸钠,同时放出 ,写出反应的离子方程式
,写出反应的离子方程式_______ 。
(5)工业上由无水 制取镁的化学方程式为
制取镁的化学方程式为_______ 。

(1)操作A是
(2)除去粗盐中杂质(
 、
、 、
、 ),加入的药品顺序正确的是_______。
),加入的药品顺序正确的是_______。A. 溶液→NaOH溶液 溶液→NaOH溶液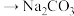 溶液→过滤后加盐酸 溶液→过滤后加盐酸 |
B.NaOH溶液→ 溶液→ 溶液→ 溶液→过滤后加盐酸 溶液→过滤后加盐酸 |
C.NaOH溶液→ 溶液→ 溶液→ 溶液→过滤后加盐酸 溶液→过滤后加盐酸 |
D. 溶液→NaOH溶液→ 溶液→NaOH溶液→ 溶液→过滤后加盐酸 溶液→过滤后加盐酸 |
 ,而后又将
,而后又将 还原为
还原为 ,其目的是
,其目的是(4)工业上也可以用
 溶液吸收吹出的
溶液吸收吹出的 ,生成溴化钠和溴酸钠,同时放出
,生成溴化钠和溴酸钠,同时放出 ,写出反应的离子方程式
,写出反应的离子方程式(5)工业上由无水
 制取镁的化学方程式为
制取镁的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】从海水提取镁和溴的流程如下,请回答相关问题:

(1)操作1的名称_______ 。试剂a为_______ (填化学式),通入试剂a发生反应的离子方程式_______ 。
(2)富集溴一般先用空气和水蒸气吹出单质溴,再用SO2的水溶液将其还原吸收,吹出塔中通入热空气的目的是_______ 。发生反应的离子方程式为_______ 。也可用纯碱吸收溴,主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),吸收1.5molBr2时,转移的电子为_______ mol。
(3)提取溴的过程中,经过2次Br-→Br2转化的目的是_______
(4)据上述流程从1m3海水中提取溴,最终得到48gBr2,若提取率为80%,则原海水中溴元素的浓度为_______ mg/L

(1)操作1的名称
(2)富集溴一般先用空气和水蒸气吹出单质溴,再用SO2的水溶液将其还原吸收,吹出塔中通入热空气的目的是
(3)提取溴的过程中,经过2次Br-→Br2转化的目的是
(4)据上述流程从1m3海水中提取溴,最终得到48gBr2,若提取率为80%,则原海水中溴元素的浓度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上从海水中提取金属镁,工艺流程如图:
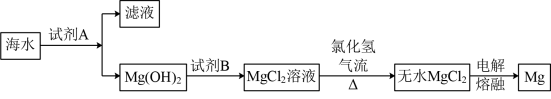
(1)试剂A为____ (填名称,下同),试剂B为____ 。
(2)为探究制得的金属镁与金属铜、钛的金属活动性强弱,某兴趣小组将打磨过的钛片投入硫酸铜溶液中,一段时间后在钛片的表面析出红色固体,则钛和铜的金属活泼性:Ti____ Cu(填“>”,“<”或“=”),上述反应的离子方程式为____ 。(已知Ti在化合物中一般显+4价)。为比较镁与钛的金属活泼性强弱,该兴趣小组设计原电池如图所示:
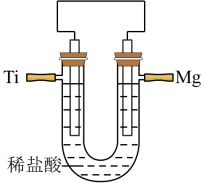
若Mg片不断溶解,Ti片上有无色气泡产生,则可证明Ti____ Mg(填“>”、“<”或“=”)。请写出该电池的负极的电极反应式:____ 。

(1)试剂A为
(2)为探究制得的金属镁与金属铜、钛的金属活动性强弱,某兴趣小组将打磨过的钛片投入硫酸铜溶液中,一段时间后在钛片的表面析出红色固体,则钛和铜的金属活泼性:Ti

若Mg片不断溶解,Ti片上有无色气泡产生,则可证明Ti
您最近一年使用:0次



