1 . 铬酸铅俗称铬黄,主要用于油漆、油墨、塑料以及橡胶等行业。一种以含铬废水(含 、
、 、
、 )和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下:
)和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下:
(1)草酸泥渣“粉碎”的目的是___________ ,“焙烧”时加入碳酸钠是为了将硫酸铅转化为氧化铅PbO,同时放出 ,该转化过程的化学方程式为
,该转化过程的化学方程式为___________ 。
(2)滤渣的主要成分为___________ 、___________ 。(填化学式)
(3)“沉淀除杂”所得滤液中含铬化合物主要为___________ 。(填化学式)
(4)“氧化”步骤加入过氧化氢溶液发生反应的离子方程式为___________ 。
(5)为了提高沉铬率,用平衡移动原理解释“酸溶”过程中所加硝酸不能过量的原因___________ 。
(6)处理含 的废水时,Cr(VI)被还原成Cr(Ⅲ)。若投入
的废水时,Cr(VI)被还原成Cr(Ⅲ)。若投入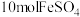 ,使金属阳离子恰好完全形成铁铬氧体(
,使金属阳离子恰好完全形成铁铬氧体( )沉淀,理论上还需要
)沉淀,理论上还需要 的物质的量为
的物质的量为___________ mol。
 、
、 、
、 )和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下:
)和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下: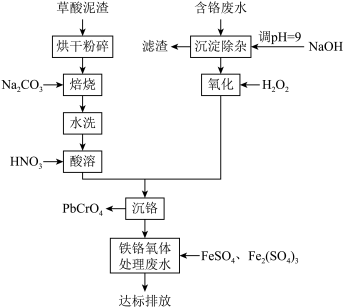

(1)草酸泥渣“粉碎”的目的是
 ,该转化过程的化学方程式为
,该转化过程的化学方程式为(2)滤渣的主要成分为
(3)“沉淀除杂”所得滤液中含铬化合物主要为
(4)“氧化”步骤加入过氧化氢溶液发生反应的离子方程式为
(5)为了提高沉铬率,用平衡移动原理解释“酸溶”过程中所加硝酸不能过量的原因
(6)处理含
 的废水时,Cr(VI)被还原成Cr(Ⅲ)。若投入
的废水时,Cr(VI)被还原成Cr(Ⅲ)。若投入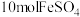 ,使金属阳离子恰好完全形成铁铬氧体(
,使金属阳离子恰好完全形成铁铬氧体( )沉淀,理论上还需要
)沉淀,理论上还需要 的物质的量为
的物质的量为
您最近半年使用:0次
名校
解题方法
2 . 下列反应的离子方程式书写正确的是
A.碘化亚铁溶液中通入足量的氯气: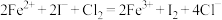 |
B.加碘盐与药物碘化钾片尽量不要同时服用: |
C.向 溶液中加入过量的NaOH溶液: 溶液中加入过量的NaOH溶液: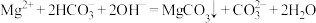 |
D.向 溶液中滴入 溶液中滴入 使 使 反应完全: 反应完全: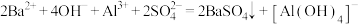 |
您最近半年使用:0次
今日更新
|
601次组卷
|
3卷引用:湖南省“一起考”大联考2023-2024学年高三下学期3月模拟考试(模拟一)化学试题
湖南省“一起考”大联考2023-2024学年高三下学期3月模拟考试(模拟一)化学试题江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷 (已下线)题型4 离子反应 氧化还原反应(25题)-2024年高考化学常考点必杀300题(新高考通用)
解题方法
3 . 下列离子方程式书写正确的是
A. NaAlO2溶液中通入过量CO2: NaAlO2溶液中通入过量CO2: |
B. 溶液中加入过量氨水: 溶液中加入过量氨水: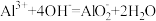 |
C.过量的Fe溶于少量稀硝酸中: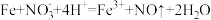 |
D.在强碱溶液中,次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3=2FeO +3Cl-+H2O+4H+ +3Cl-+H2O+4H+ |
您最近半年使用:0次
名校
解题方法
4 . X、Y、Z、W、M、N是原子序数依次增大的短周期主族元素,它们的结构或性质信息如表所示,请回答下列问题:
(1)M在元素周期表中的位置为________ ,请写出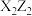 的电子式:
的电子式:________ 。
(2)Z、W、M、N的简单离子半径由大到小的顺序为______________ (写离子符号)。
(3)
________ (填“是”或“不是”)电解质,向其水溶液中滴加少量M的盐酸盐溶液,发生反应的离子方程式为__________________ 。
(4)Y的最简单氢化物与过量的N的最高价氧化物对应的水化物反应得到一种酸式盐a,a在水中的电离方程式为_______________ ,向a溶液中滴加少量 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_____________________ 。
元素 | 结构或性质信息 |
X | 元素周期表中,X的半径最小 |
Y | K层电子数比L层少3 |
Z | 最外层电子数是其周期数的3倍 |
W | 其单质的氧化性最强 |
M | W的核外电子数是M的最外层电子数的3倍 |
N | 最外层电子数是其周期数的2倍 |
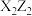 的电子式:
的电子式:(2)Z、W、M、N的简单离子半径由大到小的顺序为
(3)

(4)Y的最简单氢化物与过量的N的最高价氧化物对应的水化物反应得到一种酸式盐a,a在水中的电离方程式为
 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
您最近半年使用:0次
名校
解题方法
5 . 下列离子方程式书写正确的是
A.向稀硫酸中加入铜粉: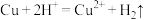 |
B.向稀硝酸中加入少量小苏打: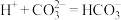 |
C. 与稀盐酸反应: 与稀盐酸反应: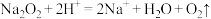 |
D.盛装NaOH溶液的试剂瓶不能用磨口玻璃塞: |
您最近半年使用:0次
名校
6 . 利用含钴废料(主要成分为Co3O4,还含有少量SiO2、Fe2O3、Al2O3等杂质)制备LiCoO2的工艺如下。
回答下列问题:
(1)“酸浸”时_______ (填“可”或“不可”)用SO2代替H2O2。
(2)写出沉钴的离子反应方程式:_______ 。
(3)“调pH”的范围为4.5~7.8,滤液中残留的
_______ 。
(4)“高温焙烧"时的化学方程式:_______ 。

| 金属离子 | Fe2+ | Fe3+ | Al3+ | Co2+ |
| 开始沉淀的pH | 8.5 | 2.2 | 3.4 | 7.8 |
| 完全沉淀[c(金属离子)≤1×10-5mol/L]的pH | 10.0 | 3.0 | 4.5 | 9.4 |
(1)“酸浸”时
(2)写出沉钴的离子反应方程式:
(3)“调pH”的范围为4.5~7.8,滤液中残留的

(4)“高温焙烧"时的化学方程式:
您最近半年使用:0次
名校
7 . 锶的化合物应用广泛, 可用于陶瓷工业,
可用于陶瓷工业,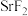 可作防蛀牙膏的添加剂。
可作防蛀牙膏的添加剂。
(1)以天青石精矿(主要含 )为原料制备高纯
)为原料制备高纯 的部分工艺流程如图所示:
的部分工艺流程如图所示:
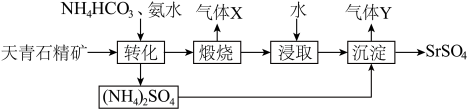
①“转化”中用 和过量氨水的混合溶液浸取天青石精矿,可制得
和过量氨水的混合溶液浸取天青石精矿,可制得 沉淀。写出该过程的离子方程式:
沉淀。写出该过程的离子方程式:_______ 。
②“转化”中维持反应温度70℃且控制氨水过量,氨水过量的主要原因是_______ 。
③该工艺流程中,可循环利用的物质是_______ (填化学式)。
(2)工业上还可用碳还原法制备高纯 。将天青石精矿和煤粉按照一定质量比在回转窑中煅烧,生成
。将天青石精矿和煤粉按照一定质量比在回转窑中煅烧,生成 ,再处理得高纯
,再处理得高纯 。
。

①煅烧温度对 转化率的影响如上图甲所示,最佳煅烧温度为
转化率的影响如上图甲所示,最佳煅烧温度为_______ 。
②天青石精矿和煤粉质量比对 转化率的影响如上图乙所示,天青石精矿和煤粉质量比增大至
转化率的影响如上图乙所示,天青石精矿和煤粉质量比增大至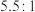 后,
后, 转化率下降的可能原因是
转化率下降的可能原因是_______ 。
 可用于陶瓷工业,
可用于陶瓷工业,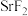 可作防蛀牙膏的添加剂。
可作防蛀牙膏的添加剂。(1)以天青石精矿(主要含
 )为原料制备高纯
)为原料制备高纯 的部分工艺流程如图所示:
的部分工艺流程如图所示:
①“转化”中用
 和过量氨水的混合溶液浸取天青石精矿,可制得
和过量氨水的混合溶液浸取天青石精矿,可制得 沉淀。写出该过程的离子方程式:
沉淀。写出该过程的离子方程式:②“转化”中维持反应温度70℃且控制氨水过量,氨水过量的主要原因是
③该工艺流程中,可循环利用的物质是
(2)工业上还可用碳还原法制备高纯
 。将天青石精矿和煤粉按照一定质量比在回转窑中煅烧,生成
。将天青石精矿和煤粉按照一定质量比在回转窑中煅烧,生成 ,再处理得高纯
,再处理得高纯 。
。
①煅烧温度对
 转化率的影响如上图甲所示,最佳煅烧温度为
转化率的影响如上图甲所示,最佳煅烧温度为②天青石精矿和煤粉质量比对
 转化率的影响如上图乙所示,天青石精矿和煤粉质量比增大至
转化率的影响如上图乙所示,天青石精矿和煤粉质量比增大至 后,
后, 转化率下降的可能原因是
转化率下降的可能原因是
您最近半年使用:0次
名校
8 . 近年来,利用SRB(硫酸盐还原菌)治理废水中的有机物、 及重金属污染取得了新的进展。
及重金属污染取得了新的进展。
(1)图1表示 和
和 在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样
在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样 ,在SRB的作用下,废水中的有机物(主要为
,在SRB的作用下,废水中的有机物(主要为 )将
)将 还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化:
还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化:____________ 。 还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。
还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。______ 。
②负极附近的 的变化:
的变化:______ (“减小”或“增大”)。
(3)SRB可用于处理废水中含重金属锑(Sb)的离子。
①通过两步反应将 转化为
转化为 除去,转化过程中有单质生成。完成第一步反应的离子方程式。
除去,转化过程中有单质生成。完成第一步反应的离子方程式。
第一步________
______ ______
______ _______+______↓+______
_______+______↓+______
第二步:
 及重金属污染取得了新的进展。
及重金属污染取得了新的进展。(1)图1表示
 和
和 在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样
在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样 ,在SRB的作用下,废水中的有机物(主要为
,在SRB的作用下,废水中的有机物(主要为 )将
)将 还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化:
还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化: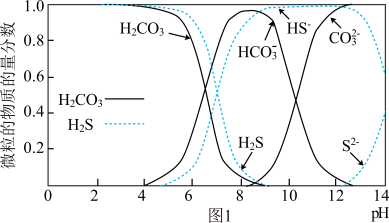
 还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。
还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。
②负极附近的
 的变化:
的变化:(3)SRB可用于处理废水中含重金属锑(Sb)的离子。
①通过两步反应将
 转化为
转化为 除去,转化过程中有单质生成。完成第一步反应的离子方程式。
除去,转化过程中有单质生成。完成第一步反应的离子方程式。第一步
______
 ______
______ _______+______↓+______
_______+______↓+______
第二步:

您最近半年使用:0次
名校
9 . 氯及其化合物应用广泛。氯的单质 可由
可由 与浓盐酸反应制得。氯的氧化物
与浓盐酸反应制得。氯的氧化物 可用于自来水消毒,
可用于自来水消毒, 是一种黄绿色气体,易溶于水,与碱反应会生成
是一种黄绿色气体,易溶于水,与碱反应会生成 与
与 ,在稀硫酸和
,在稀硫酸和 的混合溶液中通入
的混合溶液中通入 气体可制得
气体可制得 。新制氯水可将
。新制氯水可将 氧化为
氧化为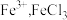 溶液可用于刻蚀覆铜板。下列反应的离子方程式表示不正确的是
溶液可用于刻蚀覆铜板。下列反应的离子方程式表示不正确的是
 可由
可由 与浓盐酸反应制得。氯的氧化物
与浓盐酸反应制得。氯的氧化物 可用于自来水消毒,
可用于自来水消毒, 是一种黄绿色气体,易溶于水,与碱反应会生成
是一种黄绿色气体,易溶于水,与碱反应会生成 与
与 ,在稀硫酸和
,在稀硫酸和 的混合溶液中通入
的混合溶液中通入 气体可制得
气体可制得 。新制氯水可将
。新制氯水可将 氧化为
氧化为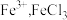 溶液可用于刻蚀覆铜板。下列反应的离子方程式表示不正确的是
溶液可用于刻蚀覆铜板。下列反应的离子方程式表示不正确的是A.用 制 制 |
B. 与碱反应: 与碱反应: |
C.制取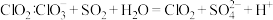 |
D.新制氯水氧化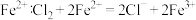 |
您最近半年使用:0次
名校
解题方法
10 . 如图是无机物 在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体,
在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体, 都含有相同的元素。
都含有相同的元素。
(1)写出反应①的化学方程式:_______ 。
(2)在①②③④中属于氮的固定的是_______ (填序号)。
(3)下列说法正确的是_______(填字母)。
(4) 易溶于水。已知某温度压强下
易溶于水。已知某温度压强下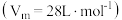 ,将体积为
,将体积为 的试管充满
的试管充满 后倒扣在水中。
后倒扣在水中。
①最终试管中所得 的物质的量浓度为(不考虑
的物质的量浓度为(不考虑 的扩散)
的扩散)_______  。
。
②若 按物质的量之比
按物质的量之比 被
被 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是_______ 。为提高吸收速率与效率,最好选用_______ 装置(填字母)。 制取
制取 ,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗
,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗 的
的 制取
制取 ,在该过程中至少消耗的
,在该过程中至少消耗的 的物质的量为
的物质的量为_______  。
。
(6)实验室里检验 中阳离子的方法是
中阳离子的方法是_______ 。
 在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体,
在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体, 都含有相同的元素。
都含有相同的元素。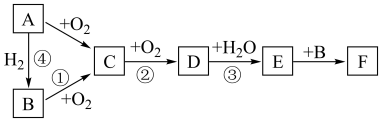
(1)写出反应①的化学方程式:
(2)在①②③④中属于氮的固定的是
(3)下列说法正确的是_______(填字母)。
A.通过水可以除去 中含有的少量D 中含有的少量D |
B.物质 均可以用向上排空气法收集 均可以用向上排空气法收集 |
C. 的浓溶液的存放方法是保存在无色细口玻璃瓶 的浓溶液的存放方法是保存在无色细口玻璃瓶 |
D.物质 中只含离子键 中只含离子键 |
(4)
 易溶于水。已知某温度压强下
易溶于水。已知某温度压强下 ,将体积为
,将体积为 的试管充满
的试管充满 后倒扣在水中。
后倒扣在水中。①最终试管中所得
 的物质的量浓度为(不考虑
的物质的量浓度为(不考虑 的扩散)
的扩散) 。
。②若
 按物质的量之比
按物质的量之比 被
被 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是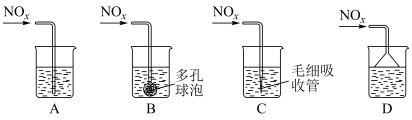
 制取
制取 ,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗
,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗 的
的 制取
制取 ,在该过程中至少消耗的
,在该过程中至少消耗的 的物质的量为
的物质的量为 。
。(6)实验室里检验
 中阳离子的方法是
中阳离子的方法是
您最近半年使用:0次



