I. 溶液可用于多种气体的处理。
溶液可用于多种气体的处理。
(1) 是温室气体,可用
是温室气体,可用 溶液吸收得到
溶液吸收得到 或
或 。
。
① 俗称纯碱,已知25℃时,
俗称纯碱,已知25℃时, 第一步水解的平衡常数
第一步水解的平衡常数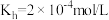 ,当溶液中
,当溶液中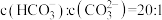 时,溶液的
时,溶液的
_______ 。
②泡沫灭火器中通常装有 溶液和
溶液和 溶液,请写出这两种溶液混合反应时的离子方程式
溶液,请写出这两种溶液混合反应时的离子方程式_______ 。
(2)金属与浓硝酸反应产生的 可用
可用 溶液吸收,反应方程式为:
溶液吸收,反应方程式为: ,含
,含 的水溶液与
的水溶液与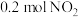 恰好完全反应得
恰好完全反应得 溶液A,溶液B为
溶液A,溶液B为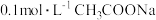 溶液,则两份溶液中
溶液,则两份溶液中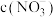 、
、 和
和 由大到小的顺序为
由大到小的顺序为_______ 。(已知 的电离常数
的电离常数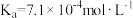 ,
, 的电离常数
的电离常数 )。
)。
(3)直接排放含 的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的
的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的 。吸收液吸收
。吸收液吸收 的过程中,
的过程中, 随
随 变化关系如下表所示:
变化关系如下表所示:
 溶液中溶液离子浓度关系正确的是(选填字母)
溶液中溶液离子浓度关系正确的是(选填字母)_______ 。
a.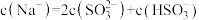
b.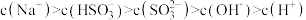
c.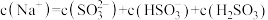
d.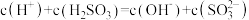
Ⅱ.滴定是一种重要的定量实验方法:某实验小组为测定碱式碳酸铜的纯度,取制得的碱式碳酸铜产品5.0g,加适量硫酸,再加 水,加热溶解,冷却后配成
水,加热溶解,冷却后配成 溶液,量取配成的
溶液,量取配成的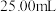 溶液于碘量瓶中,加入适量缓冲溶液控制溶液的
溶液于碘量瓶中,加入适量缓冲溶液控制溶液的 在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用
在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用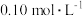 的
的 溶液进行滴定,至临近滴定终点时再加入
溶液进行滴定,至临近滴定终点时再加入 淀粉溶液做指示剂,继续滴入
淀粉溶液做指示剂,继续滴入 溶液至滴定终点。平行测定3次,实验数据如下表所示。
溶液至滴定终点。平行测定3次,实验数据如下表所示。
已知: ,
, 。
。
(4)判断滴定到达终 溶液点的现象是
溶液点的现象是_______ 。
(5)经数据处理可得该实验中滴定所用标准溶液的体积为_______  。
。
(6)下列操作会导致测定结果偏高的是_______ 。
a.装Na2S2O3溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失
b.锥形瓶未用待测液润洗
c.读 溶液体积时,若滴定前仰视,滴定后俯视
溶液体积时,若滴定前仰视,滴定后俯视
d.滴定过程中使用的碱式滴定管未润洗就装标准液滴定
 溶液可用于多种气体的处理。
溶液可用于多种气体的处理。(1)
 是温室气体,可用
是温室气体,可用 溶液吸收得到
溶液吸收得到 或
或 。
。①
 俗称纯碱,已知25℃时,
俗称纯碱,已知25℃时, 第一步水解的平衡常数
第一步水解的平衡常数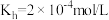 ,当溶液中
,当溶液中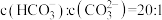 时,溶液的
时,溶液的
②泡沫灭火器中通常装有
 溶液和
溶液和 溶液,请写出这两种溶液混合反应时的离子方程式
溶液,请写出这两种溶液混合反应时的离子方程式(2)金属与浓硝酸反应产生的
 可用
可用 溶液吸收,反应方程式为:
溶液吸收,反应方程式为: ,含
,含 的水溶液与
的水溶液与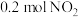 恰好完全反应得
恰好完全反应得 溶液A,溶液B为
溶液A,溶液B为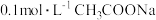 溶液,则两份溶液中
溶液,则两份溶液中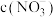 、
、 和
和 由大到小的顺序为
由大到小的顺序为 的电离常数
的电离常数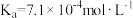 ,
, 的电离常数
的电离常数 )。
)。(3)直接排放含
 的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的
的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的 。吸收液吸收
。吸收液吸收 的过程中,
的过程中, 随
随 变化关系如下表所示:
变化关系如下表所示: | 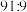 |  |  |
 | 8.2 | 7.2 | 6.2 |
 溶液中溶液离子浓度关系正确的是(选填字母)
溶液中溶液离子浓度关系正确的是(选填字母)a.
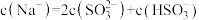
b.
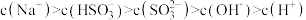
c.
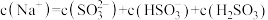
d.
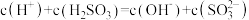
Ⅱ.滴定是一种重要的定量实验方法:某实验小组为测定碱式碳酸铜的纯度,取制得的碱式碳酸铜产品5.0g,加适量硫酸,再加
 水,加热溶解,冷却后配成
水,加热溶解,冷却后配成 溶液,量取配成的
溶液,量取配成的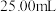 溶液于碘量瓶中,加入适量缓冲溶液控制溶液的
溶液于碘量瓶中,加入适量缓冲溶液控制溶液的 在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用
在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用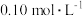 的
的 溶液进行滴定,至临近滴定终点时再加入
溶液进行滴定,至临近滴定终点时再加入 淀粉溶液做指示剂,继续滴入
淀粉溶液做指示剂,继续滴入 溶液至滴定终点。平行测定3次,实验数据如下表所示。
溶液至滴定终点。平行测定3次,实验数据如下表所示。已知:
 ,
, 。
。| 实验编号 | 滴定前 溶液的体积读数/ 溶液的体积读数/ | 滴定后 溶液的体积读数/ 溶液的体积读数/ |
| 1 | 0.10 | 20.12 |
| 2 | 1.20 | 23.21 |
| 3 | 1.50 | 21.48 |
 溶液点的现象是
溶液点的现象是(5)经数据处理可得该实验中滴定所用标准溶液的体积为
 。
。(6)下列操作会导致测定结果偏高的是
a.装Na2S2O3溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失
b.锥形瓶未用待测液润洗
c.读
 溶液体积时,若滴定前仰视,滴定后俯视
溶液体积时,若滴定前仰视,滴定后俯视d.滴定过程中使用的碱式滴定管未润洗就装标准液滴定
更新时间:2024-04-27 12:57:01
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】磷是重要的元素,能形成多种含氧酸和含氧酸盐。回答下列问题:
(1)次磷酸(H3PO2)是一种精细化工产品,向10mL H3PO2溶液中加入30mL等物质的量浓度的NaOH溶液后,所得的溶液中只有 、OH-两种阴离子。则NaH2PO2属于
、OH-两种阴离子。则NaH2PO2属于_______ (填“正盐”或“酸式盐”)。
(2)亚磷酸(H3PO3)溶液存在电离平衡:H3PO3⇌H++ ,
, ⇌H++
⇌H++
①已知25C时,1mol•L-1的H3PO3溶液中,H3PO3的电离度为α,H3PO3的一级电离平衡常数Ka1=_______ (用含α的计算式表示,H3PO3第二步电离忽略不计,忽略水的电离)。
②常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示 的是曲线
的是曲线_______ (填“I”或“II”),亚磷酸(H3PO3)的Ka2=_______ 。
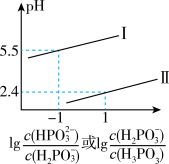
③请结合相关平衡常数判断NaH2PO3溶液显_______ 性(填“酸”、“中”或“碱”),其溶液中离子浓度大到小的顺序是_______ ,c(H+)- c(OH-)_______ c( )- c(H3PO3) (填“>”、“=”或“<”)。
)- c(H3PO3) (填“>”、“=”或“<”)。
(3)25℃时,HF 的电离常数为K=3.6×10-4;H3PO4的电离常数为K1=7.5×10 -3,K2=6.2×10 -8,K3=4.4×10 -13。足量 NaF溶液和 H3PO4溶液反应的离子方程式为:_______ 。
(1)次磷酸(H3PO2)是一种精细化工产品,向10mL H3PO2溶液中加入30mL等物质的量浓度的NaOH溶液后,所得的溶液中只有
 、OH-两种阴离子。则NaH2PO2属于
、OH-两种阴离子。则NaH2PO2属于(2)亚磷酸(H3PO3)溶液存在电离平衡:H3PO3⇌H++
 ,
, ⇌H++
⇌H++
①已知25C时,1mol•L-1的H3PO3溶液中,H3PO3的电离度为α,H3PO3的一级电离平衡常数Ka1=
②常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示
 的是曲线
的是曲线
③请结合相关平衡常数判断NaH2PO3溶液显
 )- c(H3PO3) (填“>”、“=”或“<”)。
)- c(H3PO3) (填“>”、“=”或“<”)。(3)25℃时,HF 的电离常数为K=3.6×10-4;H3PO4的电离常数为K1=7.5×10 -3,K2=6.2×10 -8,K3=4.4×10 -13。足量 NaF溶液和 H3PO4溶液反应的离子方程式为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】为抑制新冠病毒传播,含氯消毒剂被广泛使用。常见的含氯消毒剂有次氯酸盐、ClO2、有机氯化物等。用NaCl电解法生成ClO2的工艺原理示意图如图,发生器内电解生成ClO2。
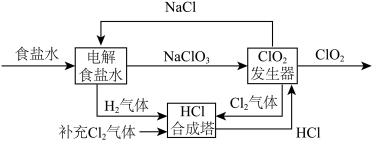
完成下列填空:
(1)Cl原子的最外层电子层上具有_____ 种不同能量的电子;HClO的电子式是_________ ;
(2)Cl2性质活泼,易形成多种化合物。请说明NaCl的熔沸点比HCl高的原因:_________________________
(3)根据示意图,补充并配平ClO2发生器中发生的化学反应方程式:_____ 。
_____NaClO3+_____HCl =_____+_____H2O
若反应中有2mol电子发生转移,则生成ClO2_____ mol。
(4)某兴趣小组通过实验测定不同pH环境中,相同浓度NaClO溶液的细菌杀灭率(%),实验结果如下表。
①NaClO溶液呈碱性的原因是_________________________ (用离子方程式表示)。
②调节NaClO溶液pH时不能选用盐酸的原因为________________ 。
③由表中数据可推断,该实验得到的结论是_____________________
④家用消毒常用84消毒液而不采用次氯酸,说明其理由。_______________

完成下列填空:
(1)Cl原子的最外层电子层上具有
(2)Cl2性质活泼,易形成多种化合物。请说明NaCl的熔沸点比HCl高的原因:
(3)根据示意图,补充并配平ClO2发生器中发生的化学反应方程式:
_____NaClO3+_____HCl =_____+_____H2O
若反应中有2mol电子发生转移,则生成ClO2
(4)某兴趣小组通过实验测定不同pH环境中,相同浓度NaClO溶液的细菌杀灭率(%),实验结果如下表。
NaClO溶液浓度/ (mg·L-1) | 不同pH下的细菌杀灭率/% | ||
pH=4.0 | pH=6.5 | pH=9.0 | |
250 | 98.90 | 77.90 | 53.90 |
①NaClO溶液呈碱性的原因是
②调节NaClO溶液pH时不能选用盐酸的原因为
③由表中数据可推断,该实验得到的结论是
④家用消毒常用84消毒液而不采用次氯酸,说明其理由。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题。
(1)在某温度下,向含有AgCl固体的AgCl饱和溶液中通入少量HCl,则AgCl的溶解度___________ (填“增大”“减小”或“不变”,下同),Ksp___________ ,c(Ag+)___________ 。
(2)在25℃时对氨水进行如下操作,若向氨水中加入稀硫酸,使氨水恰好被中和,所得溶液的pH___________ 7(“大于”、“小于”或“等于”);若向氨水中加入稀硫酸至溶液的pH=7,此时溶液中 =amol/L,则
=amol/L,则 =
=___________ 。
(3)若要在铁制品表面镀镍,电镀液用硫酸镍溶液,则镍应与电源的___________ 极相连,铁制品应与电源的___________ 极相连。电镀过程中硫酸镍溶液中溶质的浓度会___________ (填“增大”“减小”或“不变”)。
(1)在某温度下,向含有AgCl固体的AgCl饱和溶液中通入少量HCl,则AgCl的溶解度
(2)在25℃时对氨水进行如下操作,若向氨水中加入稀硫酸,使氨水恰好被中和,所得溶液的pH
 =amol/L,则
=amol/L,则 =
=(3)若要在铁制品表面镀镍,电镀液用硫酸镍溶液,则镍应与电源的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】一种将废水(含Ca2+、Mg2+、CN-及悬浮物)通过净化、杀菌消毒生产自来水的流程示意图如下:
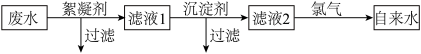
(1)絮凝剂除去悬浮物质时发生物理变化和化学变化,下列既发生物理变化又发生化学变化的是(填标号)______。
(2)绿矾是常用的絮凝剂,它在水中最终生成(填化学式)沉淀____ ,下列物质中也可以作为絮凝剂的有(填标号)______ 。
A.NH4Cl B.食盐 C.明矾 D.CH3COONa
若用FeCl3作絮凝剂,实践中发现废水中的c(HCO )越大,净水效果越好,原因是
)越大,净水效果越好,原因是___ 。
(3)加沉淀剂是为了除去Ca2+、Mg2+,若加入生石灰和纯碱作沉淀剂,试剂添加时先加_后加__ ,理由是_____ 。此时Ca2+、Mg2+离子分别形成______ 、______ (填化学式)而沉淀下来。
(4)向滤液2中通入Cl2的作用有两种:一是利用生成的(填名称)______ 、______ 具有强氧化性能杀死水中的病菌;二是将CN-氧化成CO2和N2,从而消除CN-的毒性,若参加反应的C12与CN-的物质的量之比为5: 2,则该反应的离子方程式是______ 。

(1)絮凝剂除去悬浮物质时发生物理变化和化学变化,下列既发生物理变化又发生化学变化的是(填标号)______。
| A.蒸馏 | B.煤干馏 | C.风化 | D.分馏 |
A.NH4Cl B.食盐 C.明矾 D.CH3COONa
若用FeCl3作絮凝剂,实践中发现废水中的c(HCO
 )越大,净水效果越好,原因是
)越大,净水效果越好,原因是(3)加沉淀剂是为了除去Ca2+、Mg2+,若加入生石灰和纯碱作沉淀剂,试剂添加时先加_后加
(4)向滤液2中通入Cl2的作用有两种:一是利用生成的(填名称)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看做化学平衡。请根据所学的知识回答:
(1)A为0.1mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为__ 。
(2)B为0.1mol·L-1NaHCO3溶液,请分析NaHCO3溶液显碱性的原因:__ 。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时常加入__ 以抑制其水解,若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为_ 。
(4)D为含有足量AgCl固体的饱和溶液,AgCl在水中存在沉淀溶解平衡:AgCl(s)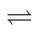 Ag+(aq)+Cl-(aq),在25℃时,Ksp(AgCl)=1.8×10-10。现将足量氯化银分别放入:
Ag+(aq)+Cl-(aq),在25℃时,Ksp(AgCl)=1.8×10-10。现将足量氯化银分别放入:
①100mL蒸馏水中;②100mL0.2mol·L-1AgNO3溶液中;③100mL0.1mol·L-1氯化铝溶液中;④100mL0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是__ (填序号);向②中加入足量氯化银后,氯离子的浓度为__ mol·L-1。
(1)A为0.1mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为
(2)B为0.1mol·L-1NaHCO3溶液,请分析NaHCO3溶液显碱性的原因:
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时常加入
(4)D为含有足量AgCl固体的饱和溶液,AgCl在水中存在沉淀溶解平衡:AgCl(s)
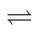 Ag+(aq)+Cl-(aq),在25℃时,Ksp(AgCl)=1.8×10-10。现将足量氯化银分别放入:
Ag+(aq)+Cl-(aq),在25℃时,Ksp(AgCl)=1.8×10-10。现将足量氯化银分别放入:①100mL蒸馏水中;②100mL0.2mol·L-1AgNO3溶液中;③100mL0.1mol·L-1氯化铝溶液中;④100mL0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】Ⅰ.(1) 硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请用文字简要说明原因___________________ , 用热水配制出澄清的较浓的 CuSO4 溶液时应再加入少量____________________ 。
(2) 稀 Na2S 溶液有一种腐卵气味,加入 AlCl3 溶液后,腐卵气味加剧,用离子方程式表 示气味加剧过程所发生的化学反应__________________ 。
(3) 下列物质水溶液经加热浓缩、蒸干灼烧后能得到原溶质物质的是_____
①NH4 HCO3;②CaCl2;③AlCl3;④Cu(NO3)2;⑤FeCl2;⑥K2SO3;⑦KMnO4;⑧ KAl(SO4)2
(Ⅱ)依据氧化还原反应:MnO4- + 5Fe2+ + 8H+ = Mn2+ + 5Fe3+ + 4H2O,欲采用滴定的方法测定 FeSO4 的质量分数,实验步骤如下:
① 称量绿矾样品,配成 100 mL 待测溶液,② 取一定体积待测液置于锥形瓶中,并加入一定量的硫酸,③ 将标准浓度的 KMnO4 溶液装入滴定管中,调节液面至 a mL 处,④ 滴定待测液至滴定终点时,滴定管的液面读数 b mL,⑤重复滴定 2~3 次。
(1) 如何确定滴定到达终点?现象是_____________
(2) 下列操作会导致测定结果偏低的是_____
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(3)下列每种量器的数量不限,在上述实验中,必须 使用的有_____
A.托盘天平 B.量筒 C.碱式滴定管 D.酸式滴定管
(2) 稀 Na2S 溶液有一种腐卵气味,加入 AlCl3 溶液后,腐卵气味加剧,用离子方程式表 示气味加剧过程所发生的化学反应
(3) 下列物质水溶液经加热浓缩、蒸干灼烧后能得到原溶质物质的是
①NH4 HCO3;②CaCl2;③AlCl3;④Cu(NO3)2;⑤FeCl2;⑥K2SO3;⑦KMnO4;⑧ KAl(SO4)2
(Ⅱ)依据氧化还原反应:MnO4- + 5Fe2+ + 8H+ = Mn2+ + 5Fe3+ + 4H2O,欲采用滴定的方法测定 FeSO4 的质量分数,实验步骤如下:
① 称量绿矾样品,配成 100 mL 待测溶液,② 取一定体积待测液置于锥形瓶中,并加入一定量的硫酸,③ 将标准浓度的 KMnO4 溶液装入滴定管中,调节液面至 a mL 处,④ 滴定待测液至滴定终点时,滴定管的液面读数 b mL,⑤重复滴定 2~3 次。
(1) 如何确定滴定到达终点?现象是
(2) 下列操作会导致测定结果偏低的是
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(3)下列每种量器的数量不限,在上述实验中,
A.托盘天平 B.量筒 C.碱式滴定管 D.酸式滴定管
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
(1)连二次硝酸中氮元素的化合价为____________ 。
(2)常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。

①写出H2N2O2在水溶液中的电离方程式:______________ 。
②常温下H2N2O2的Ka1约为______________
③b点时溶液中c(H2N2O2)_____ (填“>”、“<”或“=”,下同)c(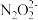 )。
)。
④a点时溶液中c(Na+)________ c(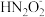 )+c(
)+c(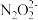 )。
)。
⑤a、b、c三点,水的电离程度最大的是__________ 。
(3)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中 =
=______ 。[已知Ksp(Ag2N2O2)=4.2×10-9,Ksp(Ag2SO4)=1.4×10-5]
(1)连二次硝酸中氮元素的化合价为
(2)常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。

①写出H2N2O2在水溶液中的电离方程式:
②常温下H2N2O2的Ka1约为
③b点时溶液中c(H2N2O2)
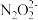 )。
)。④a点时溶液中c(Na+)
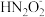 )+c(
)+c(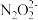 )。
)。⑤a、b、c三点,水的电离程度最大的是
(3)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中
 =
=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】水溶液广泛存在于生命体及其赖以生存的环境中,研究水溶液的性质及反应有重要意义,室温下,相关酸的电离平衡常数如下表所示:
回答下列问题。
(1) 电离方程式是
电离方程式是_________ 。
(2)物质的量浓度相同的 和
和 ,pH大小:
,pH大小:
_________  (填“<”“=”或“>”)。
(填“<”“=”或“>”)。
(3)物质的量浓度相同的 、
、 、
、 三种溶液,pH由大到小的顺序是
三种溶液,pH由大到小的顺序是_________ 。
(4)室温下,向未知浓度的 溶液中加入
溶液中加入 溶液。
溶液。
①溶液中的
_________ (填“增大”“减小”“不变”或“无法判断”)。
②当滴加 溶液至溶液中的
溶液至溶液中的 ,此时溶液中的pH
,此时溶液中的pH_________ 7(填“<”“=”或“>”),判断的依据_________ 。
(5)为测定某 溶液的浓度,取20.00
溶液的浓度,取20.00 待测溶液于锥形瓶中,滴加2滴酚酞溶液,用浓度为0.1000
待测溶液于锥形瓶中,滴加2滴酚酞溶液,用浓度为0.1000 的
的 标准溶液滴定。
标准溶液滴定。
①达到滴定终点的现象是_________ 。
②在滴定实验过程中,下列仪器中有蒸馏水,对实验结果没有影响的是_________ (填“滴定管”或“锥形瓶”)。
③经3次平行实验,达到滴定终点时,消耗 标准溶液体积的平均值为19.98
标准溶液体积的平均值为19.98 ,则此
,则此 溶液的浓度是
溶液的浓度是_________ 。
| 酸 |  | CH3COOH |  | HCl |
| 电离平衡常数 |  |  |  | —— |
(1)
 电离方程式是
电离方程式是(2)物质的量浓度相同的
 和
和 ,pH大小:
,pH大小:
 (填“<”“=”或“>”)。
(填“<”“=”或“>”)。(3)物质的量浓度相同的
 、
、 、
、 三种溶液,pH由大到小的顺序是
三种溶液,pH由大到小的顺序是(4)室温下,向未知浓度的
 溶液中加入
溶液中加入 溶液。
溶液。①溶液中的

②当滴加
 溶液至溶液中的
溶液至溶液中的 ,此时溶液中的pH
,此时溶液中的pH(5)为测定某
 溶液的浓度,取20.00
溶液的浓度,取20.00 待测溶液于锥形瓶中,滴加2滴酚酞溶液,用浓度为0.1000
待测溶液于锥形瓶中,滴加2滴酚酞溶液,用浓度为0.1000 的
的 标准溶液滴定。
标准溶液滴定。①达到滴定终点的现象是
②在滴定实验过程中,下列仪器中有蒸馏水,对实验结果没有影响的是
③经3次平行实验,达到滴定终点时,消耗
 标准溶液体积的平均值为19.98
标准溶液体积的平均值为19.98 ,则此
,则此 溶液的浓度是
溶液的浓度是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】碲及其化合物具有许多优良性能,被广泛用于冶金、化工、医药卫生等工业领域。工业上用铜阳极泥(主要成分除含Cu、Te外,还有少量Ag和Au)经如下工艺流程得到粗碲。
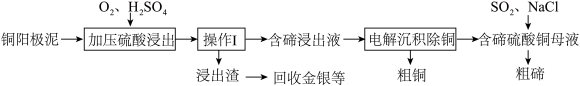
已知TeOSO4为正盐。
(1)已知此工艺中“加压硫酸浸出”过程中会发生以下化学反应:Cu2Te+2O2=2CuO+TeO2;
TeO2+H2SO4=TeOSO4+H2O。“含碲浸出液”的溶质成分除了TeOSO4外,主要是_____ (填化学式)。
(2)操作I的分离方法是___________
(3)“电解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电解初级阶段阴极的主要电极反应式是____________________________ 。
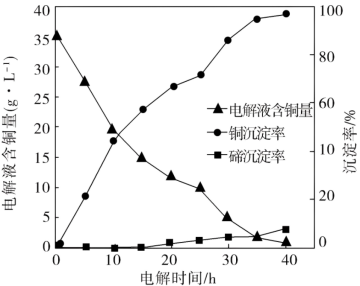
(4)通过图象分析,你认为工业上该过程持续的时段最好是________ 。
A.20h B.30h C.35h. D.40h
(5)向“含碲硫酸铜母液”通入SO2并加入NaCl反应一段时间后,Te(IV)浓度从6.72gL-1下降到0.10gL-1,该过程生成粗碲的离子方程式:_____________________
(6)25°C时,亚碲酸(H2TeO3)的Ka1=1×10-3,Ka2=2×10-8。
①0.1mol∙L-1H2TeO3电离度α约为_________ 。(α= ×100%)
×100%)
②0.lmol∙L-1的NaHTeO3溶液中,下列粒子的物质的量浓度关系正确的是______ 。
A.c(Na+)>c( )>c(OH-)>c(H2TeO3)>c(H+)
)>c(OH-)>c(H2TeO3)>c(H+)
B.c(Na+)+c(H+)=c( )+c(
)+c(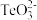 )+c(OH-)
)+c(OH-)
C.c(Na+)=c(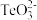 )+c(
)+c( )+c(H2TeO3)
)+c(H2TeO3)
D.c(H+)+c(H2TeO3)=c(OH-)+c(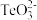 )
)

已知TeOSO4为正盐。
(1)已知此工艺中“加压硫酸浸出”过程中会发生以下化学反应:Cu2Te+2O2=2CuO+TeO2;
TeO2+H2SO4=TeOSO4+H2O。“含碲浸出液”的溶质成分除了TeOSO4外,主要是
(2)操作I的分离方法是
(3)“电解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电解初级阶段阴极的主要电极反应式是

(4)通过图象分析,你认为工业上该过程持续的时段最好是
A.20h B.30h C.35h. D.40h
(5)向“含碲硫酸铜母液”通入SO2并加入NaCl反应一段时间后,Te(IV)浓度从6.72gL-1下降到0.10gL-1,该过程生成粗碲的离子方程式:
(6)25°C时,亚碲酸(H2TeO3)的Ka1=1×10-3,Ka2=2×10-8。
①0.1mol∙L-1H2TeO3电离度α约为
 ×100%)
×100%)②0.lmol∙L-1的NaHTeO3溶液中,下列粒子的物质的量浓度关系正确的是
A.c(Na+)>c(
 )>c(OH-)>c(H2TeO3)>c(H+)
)>c(OH-)>c(H2TeO3)>c(H+)B.c(Na+)+c(H+)=c(
 )+c(
)+c(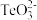 )+c(OH-)
)+c(OH-)C.c(Na+)=c(
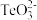 )+c(
)+c( )+c(H2TeO3)
)+c(H2TeO3)D.c(H+)+c(H2TeO3)=c(OH-)+c(
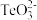 )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】焦亚硫酸钠(Na2S2O5)具有强还原性、漂白性,广泛用于食品、医药、印染等。工业上常以含硫废气为原料制得过饱和NaHSO3溶液,再将其结晶脱水制得Na2S2O5。实验室可用如图装置(略去部分夹持仪器)模拟该制备过程。 已知:常温下,
 5.6×10-11,Ka1 (H2SO3)=1.3×10-2、Ka2 (H2SO3)=6.2×10-8。回答下列问题:
5.6×10-11,Ka1 (H2SO3)=1.3×10-2、Ka2 (H2SO3)=6.2×10-8。回答下列问题:

(1)按图示组装仪器。
①A装置用于制备SO2,试剂X、Y的组合最好是_______________ (填字母)。
a.稀盐酸和 Na2SO3,固体 b.98%硫酸和铜
c.70%硫酸和K2SO3固体 d.稀硝酸和 NaHSO3固体
②D装置的作用是___________________
(2)检查装置的气密性后装入药品,先向C 中烧瓶滴加饱和Na2CO3溶液,再向 A 中烧瓶滴加 X,反应一段时间,待 C 中溶液的pH 为4.1 时,停止通SO2,写出SO2和饱和 Na2CO3溶液反应的化学方程式:__________________________________ 。
(3)将恒压分液漏斗更换为固体加料漏斗,先向三颈烧瓶中加入Na2CO3粉末至pH为7~8,再继续通入SO2至 pH=4.1,该步骤的目的是_________________________ 。将C 中溶液结晶脱水析出太量白色固体,经过滤、乙醇洗涤、真空干燥,得到产品 Na2S2O5。
(4)称取1.000g产品于碘量瓶中,加入50.00 mL 0.2000 mol·L-1过量标准碘溶液(杂质不参与反应),在暗处放置5分钟充分反应:______________________________ (填离子方程式)。再用 标准溶液滴定剩余碘,发生反应:
标准溶液滴定剩余碘,发生反应: , 加入淀粉指示剂,滴定至溶液蓝色刚好褪去。上述过程重复三次,消耗Na2S2O3溶液的体积分别是19.60 mL、20.22 mL、20.18 mL,产品中Na2S2O5的纯度为
, 加入淀粉指示剂,滴定至溶液蓝色刚好褪去。上述过程重复三次,消耗Na2S2O3溶液的体积分别是19.60 mL、20.22 mL、20.18 mL,产品中Na2S2O5的纯度为__________________________________ (结果保留四位有效数字)。
(5)产品中可能混有的杂质为_____________________________ ,为提高纯度,在不改变原有装置的基础上对(2)中的操作进行改进,改进后的操作是_________________________________ 。

 5.6×10-11,Ka1 (H2SO3)=1.3×10-2、Ka2 (H2SO3)=6.2×10-8。回答下列问题:
5.6×10-11,Ka1 (H2SO3)=1.3×10-2、Ka2 (H2SO3)=6.2×10-8。回答下列问题:
(1)按图示组装仪器。
①A装置用于制备SO2,试剂X、Y的组合最好是
a.稀盐酸和 Na2SO3,固体 b.98%硫酸和铜
c.70%硫酸和K2SO3固体 d.稀硝酸和 NaHSO3固体
②D装置的作用是
(2)检查装置的气密性后装入药品,先向C 中烧瓶滴加饱和Na2CO3溶液,再向 A 中烧瓶滴加 X,反应一段时间,待 C 中溶液的pH 为4.1 时,停止通SO2,写出SO2和饱和 Na2CO3溶液反应的化学方程式:
(3)将恒压分液漏斗更换为固体加料漏斗,先向三颈烧瓶中加入Na2CO3粉末至pH为7~8,再继续通入SO2至 pH=4.1,该步骤的目的是
(4)称取1.000g产品于碘量瓶中,加入50.00 mL 0.2000 mol·L-1过量标准碘溶液(杂质不参与反应),在暗处放置5分钟充分反应:
 标准溶液滴定剩余碘,发生反应:
标准溶液滴定剩余碘,发生反应: , 加入淀粉指示剂,滴定至溶液蓝色刚好褪去。上述过程重复三次,消耗Na2S2O3溶液的体积分别是19.60 mL、20.22 mL、20.18 mL,产品中Na2S2O5的纯度为
, 加入淀粉指示剂,滴定至溶液蓝色刚好褪去。上述过程重复三次,消耗Na2S2O3溶液的体积分别是19.60 mL、20.22 mL、20.18 mL,产品中Na2S2O5的纯度为(5)产品中可能混有的杂质为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氧化还原是学习化学的重要工具。根据所学知识,按要求填空。
(1)四大发明在人类发展史上发挥了重要的作用,其中黑火药的爆炸原理为2KNO3+S+2C K2S+N2↑+3CO2↑。
K2S+N2↑+3CO2↑。
①上述反应中被还原的元素为_____ (填元素符号),氧化产物为_____ (填化学式)。
②若上述反应中转移的电子的物质的量为2.4mol,生成N2的体积(标准状况下)为____ L,被S氧化的C的物质的量为_____ mol。
(2)已知Fe(NH4)2Fe(CN)6是难溶于酸的白色沉淀,将其与H2SO4和NaClO3的混合溶液加热,经过滤洗涤干燥可制得铵铁蓝Fe(NH4)Fe(CN)6,发生反应的离子方程式为_____ 。
(3)测定产品中Ca(IO3)2的质量分数:准确称取产品0.2500g,加酸溶解后,再加入足量KI发生反应IO +5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液作为指示剂,用0.1000mol•L-1Na2S2O3溶液滴定(I2+2S2O
+5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液作为指示剂,用0.1000mol•L-1Na2S2O3溶液滴定(I2+2S2O =2I-+ S4O
=2I-+ S4O 至终点,消耗Na2S2O3溶液30.00mL,产品中Ca(IO3)2的质量分数为
至终点,消耗Na2S2O3溶液30.00mL,产品中Ca(IO3)2的质量分数为____ %。若达到终点后俯视读数,则造成的误差是____ 。(偏高、偏低或无影响)[已知Ca(IO3)2的摩尔质量:390g•mol-1]。
(1)四大发明在人类发展史上发挥了重要的作用,其中黑火药的爆炸原理为2KNO3+S+2C
 K2S+N2↑+3CO2↑。
K2S+N2↑+3CO2↑。①上述反应中被还原的元素为
②若上述反应中转移的电子的物质的量为2.4mol,生成N2的体积(标准状况下)为
(2)已知Fe(NH4)2Fe(CN)6是难溶于酸的白色沉淀,将其与H2SO4和NaClO3的混合溶液加热,经过滤洗涤干燥可制得铵铁蓝Fe(NH4)Fe(CN)6,发生反应的离子方程式为
(3)测定产品中Ca(IO3)2的质量分数:准确称取产品0.2500g,加酸溶解后,再加入足量KI发生反应IO
 +5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液作为指示剂,用0.1000mol•L-1Na2S2O3溶液滴定(I2+2S2O
+5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液作为指示剂,用0.1000mol•L-1Na2S2O3溶液滴定(I2+2S2O =2I-+ S4O
=2I-+ S4O 至终点,消耗Na2S2O3溶液30.00mL,产品中Ca(IO3)2的质量分数为
至终点,消耗Na2S2O3溶液30.00mL,产品中Ca(IO3)2的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
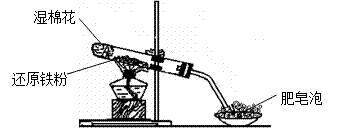
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为____________________________ ;
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是______ ,若溶液未变红色则说明硬质试管中固体物质的成分是___________________________ ;
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:__________ (用离子方程式表示);
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按如图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式:_____________________ , _______________________ ;

(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+ 具有_______ 性;由此可知,实验室中FeSO4溶液要临时配制并加少量铁粉的原因是___________________ 。

请回答下列问题:
(1)硬质试管中发生反应的化学方程式为
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按如图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式:

(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+ 具有
您最近一年使用:0次



