解题方法
1 . 氯化镍(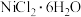 )常用于电镀、陶瓷等工业,某实验室以单质Ni为原料制取氯化镍的实验步骤如下:
)常用于电镀、陶瓷等工业,某实验室以单质Ni为原料制取氯化镍的实验步骤如下: 完全沉淀pH为3.2;
完全沉淀pH为3.2; 开始沉淀pH为7.2,完全沉淀pH为9.2。
开始沉淀pH为7.2,完全沉淀pH为9.2。
② 易水解,从溶液中获取
易水解,从溶液中获取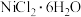 须控制pH<2。
须控制pH<2。
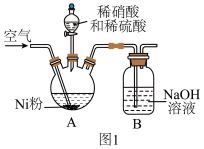
(1)在三颈烧瓶中(装置见图1)加入一定量Ni粉和水,通入空气,滴入稀硝酸和稀硫酸的混酸,至反应结束,过滤,制得 溶液。
溶液。
①向A装置中通入空气的作用除搅拌外还有___________ 。
②若镍粉过量,判断反应完成的现象是___________ 。 溶液与
溶液与 溶液混合反应得到
溶液混合反应得到 沉淀,过滤,洗涤。
沉淀,过滤,洗涤。
①沉淀反应的离子方程式为___________ 。
②检验 沉淀已经洗涤完全的方法是
沉淀已经洗涤完全的方法是___________ 。
(3)所得 固体中混有少量
固体中混有少量 。
。
请补充完整由 固体制备
固体制备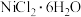 的实验方案:
的实验方案:
向 固体中加入盐酸,搅拌,
固体中加入盐酸,搅拌,___________ 。
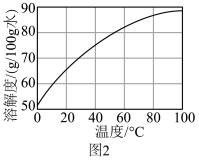
[ 溶解度曲线如图2所示。实验中
溶解度曲线如图2所示。实验中须 选用的仪器和试剂:pH计、盐酸、冰水、 ]
]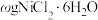 晶体产品于锥形瓶中,加入足量的蒸馏水溶解配成250mL溶液,取25.00mL所配溶液于锥形瓶中,用
晶体产品于锥形瓶中,加入足量的蒸馏水溶解配成250mL溶液,取25.00mL所配溶液于锥形瓶中,用 的标准溶液EDTA(
的标准溶液EDTA( )滴定至终点(发生反应
)滴定至终点(发生反应 ),四次实验消耗标准液的体积分别为20.02mL、19.98mL、19.60mL,20.00mL则
),四次实验消耗标准液的体积分别为20.02mL、19.98mL、19.60mL,20.00mL则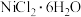 的纯度为
的纯度为___________ %(只列计算式,不考虑杂质反应)。
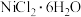 )常用于电镀、陶瓷等工业,某实验室以单质Ni为原料制取氯化镍的实验步骤如下:
)常用于电镀、陶瓷等工业,某实验室以单质Ni为原料制取氯化镍的实验步骤如下:
 完全沉淀pH为3.2;
完全沉淀pH为3.2; 开始沉淀pH为7.2,完全沉淀pH为9.2。
开始沉淀pH为7.2,完全沉淀pH为9.2。②
 易水解,从溶液中获取
易水解,从溶液中获取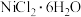 须控制pH<2。
须控制pH<2。(1)在三颈烧瓶中(装置见图1)加入一定量Ni粉和水,通入空气,滴入稀硝酸和稀硫酸的混酸,至反应结束,过滤,制得
 溶液。
溶液。①向A装置中通入空气的作用除搅拌外还有
②若镍粉过量,判断反应完成的现象是
 溶液与
溶液与 溶液混合反应得到
溶液混合反应得到 沉淀,过滤,洗涤。
沉淀,过滤,洗涤。①沉淀反应的离子方程式为
②检验
 沉淀已经洗涤完全的方法是
沉淀已经洗涤完全的方法是(3)所得
 固体中混有少量
固体中混有少量 。
。请补充完整由
 固体制备
固体制备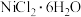 的实验方案:
的实验方案:向
 固体中加入盐酸,搅拌,
固体中加入盐酸,搅拌,[
 溶解度曲线如图2所示。实验中
溶解度曲线如图2所示。实验中 ]
]
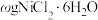 晶体产品于锥形瓶中,加入足量的蒸馏水溶解配成250mL溶液,取25.00mL所配溶液于锥形瓶中,用
晶体产品于锥形瓶中,加入足量的蒸馏水溶解配成250mL溶液,取25.00mL所配溶液于锥形瓶中,用 的标准溶液EDTA(
的标准溶液EDTA( )滴定至终点(发生反应
)滴定至终点(发生反应 ),四次实验消耗标准液的体积分别为20.02mL、19.98mL、19.60mL,20.00mL则
),四次实验消耗标准液的体积分别为20.02mL、19.98mL、19.60mL,20.00mL则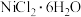 的纯度为
的纯度为
您最近半年使用:0次
名校
2 .  盐酸与
盐酸与 碳酸钠溶液相互滴定,下图为反应过程中
碳酸钠溶液相互滴定,下图为反应过程中 、
、 、
、 微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
 盐酸与
盐酸与 碳酸钠溶液相互滴定,下图为反应过程中
碳酸钠溶液相互滴定,下图为反应过程中 、
、 、
、 微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是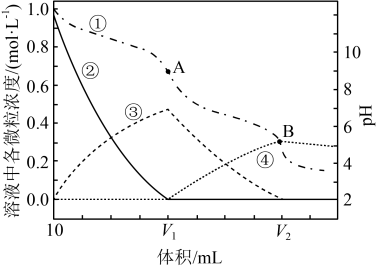
| A.上图是盐酸滴定碳酸钠溶液的曲线变化图 |
B.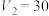 |
C.碳酸的电离平衡常数 数量级是 数量级是 |
D.已知草酸酸性大于碳酸,若用同浓度 溶液代替 溶液代替 溶液,其它实验条件不变,则A点下移 溶液,其它实验条件不变,则A点下移 |
您最近半年使用:0次
解题方法
3 . 设 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A. 硝基 硝基 与 与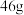 二氧化氮 二氧化氮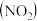 所含的电子数均为 所含的电子数均为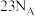 |
B.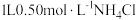 溶液与 溶液与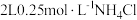 溶液中 溶液中 的物质的量均为 的物质的量均为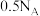 |
C. 过氧化钠分别与足量 过氧化钠分别与足量 、 、 反应,转移的电子数均为 反应,转移的电子数均为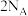 |
D.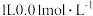 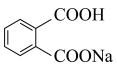 溶液中, 溶液中,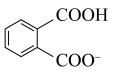 和 和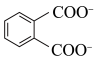 数目之和为 数目之和为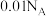 |
您最近半年使用:0次
4 . 常温下,向20 mL 0.1 mol⋅L HCOOH溶液中滴加V mL 0.1 mol⋅L
HCOOH溶液中滴加V mL 0.1 mol⋅L NaOH溶液,混合溶液的pH与
NaOH溶液,混合溶液的pH与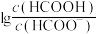 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是
 HCOOH溶液中滴加V mL 0.1 mol⋅L
HCOOH溶液中滴加V mL 0.1 mol⋅L NaOH溶液,混合溶液的pH与
NaOH溶液,混合溶液的pH与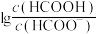 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是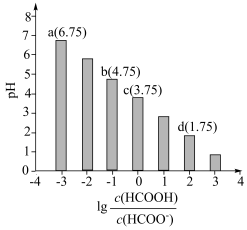
A.当 时,随着 时,随着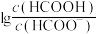 减小,水的电离程度减小 减小,水的电离程度减小 |
B.当 时达到图像c点 时达到图像c点 |
C.当 时,该溶液呈碱性 时,该溶液呈碱性 |
D.常温下,HCOOH的电离常数 的数量级为 的数量级为 |
您最近半年使用:0次
名校
5 . 某学习小组在实验宣中利用下图装置央持装置略去)测定某铁硫化物FexSy)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
步骤I:按图连接装置,检查装置气密性,装入药品;
步骤II:打开分液漏斗旋塞,缓缓滴入水,并点燃酒精喷灯;
步骤III:当硬质玻璃管中固体质量不再改变时,停止加热,继续通入一段时间的O2;
步骤IV:实验结束后,将D中所得溶液加水配制成250mL溶液;
……
1.步骤III中,停止加热后还需继续向烧瓶中滴水一段时问,其目的为_____ 。
2.步骤IV中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有_____ 。
3.取25.00mL步骤IV中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.660g。则FexSy的化学式为_____。
4.有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。你认为此方案是否合理?_____ (填“是”或“否”),原因为_____ 。
5.某同学探究溶液的酸碱性对FeCl3水解平衡的影响,实验方案如下:配制50mL0.001mol·L−lFeCl3溶液、50mL对照组溶液X,向两种溶液中分别滴加1滴1mol·L−lHCl溶液、1滴1mol·L−lNaOH溶液,测得溶液pH随时间变化的曲线如图所示。
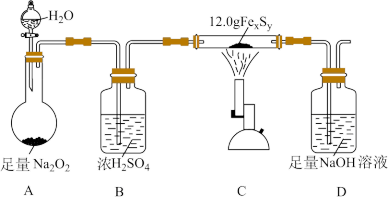
步骤I:按图连接装置,检查装置气密性,装入药品;
步骤II:打开分液漏斗旋塞,缓缓滴入水,并点燃酒精喷灯;
步骤III:当硬质玻璃管中固体质量不再改变时,停止加热,继续通入一段时间的O2;
步骤IV:实验结束后,将D中所得溶液加水配制成250mL溶液;
……
1.步骤III中,停止加热后还需继续向烧瓶中滴水一段时问,其目的为
2.步骤IV中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有
3.取25.00mL步骤IV中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.660g。则FexSy的化学式为_____。
| A.Fe2S | B.FeS | C.Fe2S3 | D.FeS2 |
5.某同学探究溶液的酸碱性对FeCl3水解平衡的影响,实验方案如下:配制50mL0.001mol·L−lFeCl3溶液、50mL对照组溶液X,向两种溶液中分别滴加1滴1mol·L−lHCl溶液、1滴1mol·L−lNaOH溶液,测得溶液pH随时间变化的曲线如图所示。
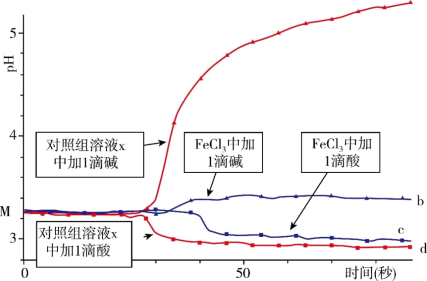
| A.依据M点对应的pH,说明Fe3+发生了水解反应 |
| B.对照组溶液X的组成可能是0.003mol·L−lKCl溶液 |
| C.依据曲线c和d说明Fe3+水解平衡发生了移动 |
| D.通过仪器检测体系浑浊度的变化,可表征水解平衡移动的方向 |
您最近半年使用:0次
6 . 下列实验操作、现象和所得结论均正确的是
| 实验操作 | 现象 | 结论 | |
| A | 在灼热木炭中加入浓硫酸,将生成的气体依次通过品红溶液、饱和NaHCO3溶液、澄清石灰水 | 品红溶液褪色,澄清石灰水变浑浊 | 浓硫酸和木炭反应产生SO2和CO2气体 |
| B | 惰性电极电解CuCl2溶液,并用湿润的淀粉KI试纸检验阳极产生的气体 | 试纸先变蓝后褪色 | 阳极有氯气产生且氯气具有漂白性 |
| C | 取少量Na2SO3样品溶于蒸馏水,滴加足量稀盐酸,再加入足量BaCl2溶液 | 有白色沉淀生成 | 样品已经变质 |
| D | 用pH试纸测定浓度均为0.1mol·L-1的CH3COONa溶液和NaClO溶液的pH比较溶液pH大小 | 最终CH3COONa溶液对应的pH试纸蓝色较浅 | 酸性:CH3COOH>HClO |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
7 . 请按要求回答以下问题:
(1)基态F原子的核外电子轨道表达式为___________ 。
(2)25Mn原子核外电子排布式为___________ 。
(3)菱锌矿ZnCO3中基态30Zn原子价电子排布式___________ ,基态C原子的核外电子占据的最高能级电子云轮廓为___________ ,基态O原子有___________ 种运动状态不同的电子。
(4)常温下,0.1mol·L-1NaHCO3溶液中,c( )<c(H2CO3),则溶液显
)<c(H2CO3),则溶液显___________ 性。
(1)基态F原子的核外电子轨道表达式为
(2)25Mn原子核外电子排布式为
(3)菱锌矿ZnCO3中基态30Zn原子价电子排布式
(4)常温下,0.1mol·L-1NaHCO3溶液中,c(
 )<c(H2CO3),则溶液显
)<c(H2CO3),则溶液显
您最近半年使用:0次
解题方法
8 . 下列实验操作不能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 实验室配制FeCl3水溶液 | 将FeCl3溶于少量浓盐酸中,再加水稀释 |
| B | 除去MgCl2酸性溶液中的Fe3+ | 加入过量MgO充分搅拌,过滤 |
| C | 证明Cu(OH)2的Ksp比Mg(OH)2的小 | 将0.1mol·L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol·L-1CuSO4溶液 |
| D | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液加热蒸干 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 设NA为阿伏加德罗常数的值,下列说法错误的是
| A.1L0.1mol·L-1CH3COONa溶液中,CH3COO-的数目小于0.1NA |
| B.常温下,1LpH=1的H2SO4溶液中,H+的数目为0.1NA |
| C.32gSO2与过量O2反应生成的SO3分子数为0.5NA |
| D.电解饱和食盐水收集到标准状况下2.24L氯气,转移电子数为0.2NA |
您最近半年使用:0次
名校
10 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.0.1mol 固体与足量的 固体与足量的 充分反应,转移 充分反应,转移 个电子 个电子 |
B.1mol 中含有 中含有 键的数目约为 键的数目约为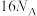 |
C.1L0.1mol/L 酸性溶液中所含 酸性溶液中所含 的数目为 的数目为 |
D.0.05mol/L的 溶液中含有 溶液中含有 的数目为 的数目为 |
您最近半年使用:0次



