名校
1 . 向 溶液中滴加
溶液中滴加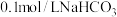 溶液,测得溶液电导率的变化如图。下列说法不正确的是
溶液,测得溶液电导率的变化如图。下列说法不正确的是
 溶液中滴加
溶液中滴加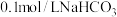 溶液,测得溶液电导率的变化如图。下列说法不正确的是
溶液,测得溶液电导率的变化如图。下列说法不正确的是
A. 是泡沫灭火器的成分之一 是泡沫灭火器的成分之一 |
B. 电导率下降的主要原因是发生了反应: 电导率下降的主要原因是发生了反应: |
C. 过程中,溶液中的 过程中,溶液中的 减小 减小 |
D.A、B、C三点水的电离程度: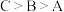 |
您最近一年使用:0次
2 . 向 的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中正确的是
的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中正确的是
 的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中正确的是
的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中正确的是
A.醋酸的电离平衡常数: |
| B.b点溶液呈中性 |
C.水的电离程度: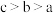 |
D.c点溶液中: |
您最近一年使用:0次
名校
解题方法
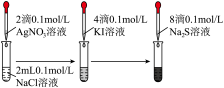
3 . 下列实验装置或操作能达到实验目的的是
|
|
A.蒸干 溶液制备 溶液制备 | B.验证沉淀转化 |
|
|
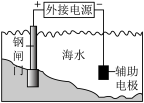
| C.检验乙炔 | D.钢闸门电化学防腐 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 制备 (S呈+2价)的化学方程式为
(S呈+2价)的化学方程式为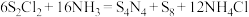 。下列说法正确的是
。下列说法正确的是
 (S呈+2价)的化学方程式为
(S呈+2价)的化学方程式为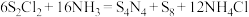 。下列说法正确的是
。下列说法正确的是A.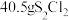 参与反应,转移电子的数目为 参与反应,转移电子的数目为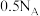 |
B.25℃、101kPa条件下,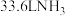 的分子数为 的分子数为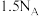 |
C.由 ( ( )与 )与 ( ( )组成的混合物中所含共价键的数目为 )组成的混合物中所含共价键的数目为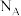 |
D.常温下,1LpH为5的 溶液中,由水电离出的 溶液中,由水电离出的 数目为 数目为 |
您最近一年使用:0次
5 . 下列实验方案能达到探究目的的是
| 选项 | 探究目的 | 实验方案 |
| A | CO还原 实验中, 实验中, 是否全部被还原 是否全部被还原 | 向CO还原 所得到的产物中加入稀盐酸,再滴加KSCN溶液,观察颜色变化 所得到的产物中加入稀盐酸,再滴加KSCN溶液,观察颜色变化 |
| B | 比较 和 和 结合 结合 的能力大小 的能力大小 | 室温下,用pH计分别测定等物质的量浓度的 溶液和NaClO溶液的pH 溶液和NaClO溶液的pH |
| C | 验证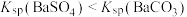 | 将 粉末和 粉末和 饱和溶液混合,充分。振荡,静置,取少量上层清液,滴加盐酸和 饱和溶液混合,充分。振荡,静置,取少量上层清液,滴加盐酸和 溶液,观察是否有沉淀产生 溶液,观察是否有沉淀产生 |
| D | 蔗糖水解产物是否具有还原性 | 向蔗糖溶液中加入少量稀硫酸,加热煮沸,冷却后加入银氨溶液,水浴加热,观察现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 下列关于酸、碱、盐在生产和生活中的应用,说法不合理的是
| A.KNO3是一种复合肥料 | B.高温煅烧石灰石可制得生石灰 |
| C.小苏打可用于治疗胃酸过多 | D.将氯化铵和草木灰混合使用 |
您最近一年使用:0次
名校
7 .  盐酸与
盐酸与 碳酸钠溶液相互滴定,下图为反应过程中
碳酸钠溶液相互滴定,下图为反应过程中 、
、 、
、 微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
 盐酸与
盐酸与 碳酸钠溶液相互滴定,下图为反应过程中
碳酸钠溶液相互滴定,下图为反应过程中 、
、 、
、 微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是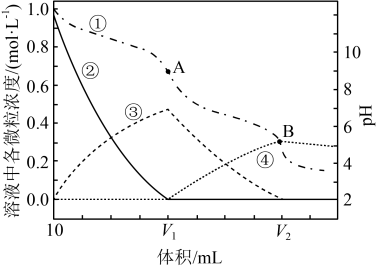
| A.上图是盐酸滴定碳酸钠溶液的曲线变化图 |
B.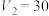 |
C.碳酸的电离平衡常数 数量级是 数量级是 |
D.已知草酸酸性大于碳酸,若用同浓度 溶液代替 溶液代替 溶液,其它实验条件不变,则A点下移 溶液,其它实验条件不变,则A点下移 |
您最近一年使用:0次
解题方法
8 . 下列说法正确的是
A.pH=11的氨水和pH=3的盐酸混合后的溶液,若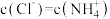 ,则溶液呈中性 ,则溶液呈中性 |
| B.在100℃时,pH约为6的纯水呈酸性 |
| C.25℃时,将pH=8的NaOH溶液加水稀释100倍,所得溶液的pH=6 |
D.0.1  溶液的pH小于7不能说明 溶液的pH小于7不能说明 为弱电解质 为弱电解质 |
您最近一年使用:0次
解题方法
9 . 下列实验方案不能达到实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A. | 将乙醇与浓硫酸的混合物加热至170℃,并将产生的气体干燥后通入少量溴的四氯化碳溶液中,观察溴的四氯化碳溶液颜色的变化 | 验证乙醇发生了消去反应 |
| B. | 向 溶液中加入少许铁粉,静置一段时间,观察是否有蓝色沉淀生成 溶液中加入少许铁粉,静置一段时间,观察是否有蓝色沉淀生成 | 验证 具有氧化性 具有氧化性 |
| C. | 分别测定相同浓度的CH3COONH4溶液和NaHCO3溶液的pH | 比较CH3COOH溶液和H2CO3的酸性 |
| D. | 向 溶液中滴加NaHCO3溶液,观察是否有白色沉淀生成 溶液中滴加NaHCO3溶液,观察是否有白色沉淀生成 | 验证结合H+的能力: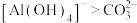 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 探究钠及其化合物的性质,下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 分别测定NaHCO3和Na2CO3溶液的pH | 两者都大于7,且Na2CO3溶液的pH大 | CO 的水解能力强于HCO 的水解能力强于HCO |
| B | 将25℃0.1mol·L-1CH3COONa溶液加热到40℃,用传感器监测溶液 变化 变化 | 溶液的 逐渐减小 逐渐减小 | 随温度升高,KW逐渐增大,CH3COONa溶液中c(H+)增大,c(OH-)减小 |
| C | 向NaHCO3溶液中加入等体积等浓度的NaAlO2溶液 | 有白色沉淀生成 | AlO 结合H+的能力强于CO 结合H+的能力强于CO |
| D | 测定中和热时,将稀 溶液缓慢倒入到盛有稀 溶液缓慢倒入到盛有稀 的内筒,搅拌使其充分混合,再盖上杯盖 的内筒,搅拌使其充分混合,再盖上杯盖 | 温度差为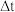 | 中和反应放热,将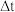 代入公式算得中和热( 代入公式算得中和热( ) ) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次