1 . 硫酸亚铁铵[(NH4)2Fe(SO4)2•6H2O]又名摩尔盐,是浅绿色晶体,易溶于水,是分析化学中的重要试剂。某化学兴趣小组对摩尔盐的一些性质进行探究。回答下列问题:
(1)在试管中加入少量摩尔盐晶体,加水溶解,测得水溶液呈酸性。由此可知_______ 。
(2)摩尔盐在500℃时隔绝空气加热完全分解,气体产物可能有NH3、SO2、SO3、H2O等。兴趣小组利用下图装置证明摩尔盐分解的气体产物中有SO2和SO3。
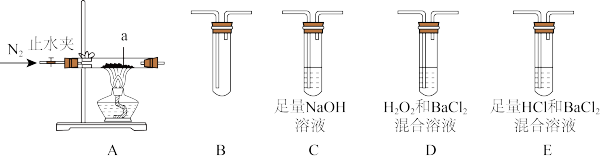
①a的名称是_______ 。装置B的作用_______ 。
②装置连接顺序为A→_______ →_______ →_______ →_______ (填字母序号)。
③能证明分解产物中有SO2的实验现象是_______ ,反应的离子方程式是_______ 。
④若装置连接顺序不变,能否将装置E中溶液换为BaCl2溶液?理由是_______ 。
(3)为判断摩尔盐是否变质,可以测定样品中Fe2+的含量。取w g样品溶于水,配制成250 mL溶液。每次取25.00 mL溶液,用c mol/L的酸性KMnO4溶液滴定,滴定三次,平均消耗KMnO4溶液体积 v mL。
①滴定时,用_______ (填“酸式”或“碱式”)滴定管盛装KMnO4溶液。
②样品中Fe2+的质量分数为_______ (用含w、c、v的式子表示)。
(1)在试管中加入少量摩尔盐晶体,加水溶解,测得水溶液呈酸性。由此可知
(2)摩尔盐在500℃时隔绝空气加热完全分解,气体产物可能有NH3、SO2、SO3、H2O等。兴趣小组利用下图装置证明摩尔盐分解的气体产物中有SO2和SO3。

①a的名称是
②装置连接顺序为A→
③能证明分解产物中有SO2的实验现象是
④若装置连接顺序不变,能否将装置E中溶液换为BaCl2溶液?理由是
(3)为判断摩尔盐是否变质,可以测定样品中Fe2+的含量。取w g样品溶于水,配制成250 mL溶液。每次取25.00 mL溶液,用c mol/L的酸性KMnO4溶液滴定,滴定三次,平均消耗KMnO4溶液体积 v mL。
①滴定时,用
②样品中Fe2+的质量分数为
您最近一年使用:0次
名校
解题方法
2 . 下列实验方案、现象和结论都正确的是
选项 | 实验方案 | 现象 | 结论 |
A | 往 | 产生白色沉淀 |
|
B | 用精密pH试纸分别测定相同浓度NaClO和 |
| 酸性强弱: |
C | 将稀硫酸酸化的 | 溶液出现黄色 |
|
D | 向少量蒸馏水中逐渐加入苯酚晶体并振荡至浑浊,静置片刻后,将试管放在热水浴中,片刻后取出,冷却静置 | 加热后可得到澄清溶液,冷却后溶液变浑浊 | 较高温度,苯酚能与水混溶;温度降低,苯酚溶解度降低 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 下列方案设计或现象和结论均完全正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 比较CH3COONa与NaClO酸性 | 室温下,用pH试纸分别测定室温下,用pH试纸分别测定 | NaClO溶液pH较大,则酸性:CH3COOH>HClO |
| B | 探究侯氏制碱法 | 向饱和食盐水中先通入二氧化碳至饱和后,再通入过量氨气 | 溶液变浑浊,析出NaHCO3 |
| C | 比较AgCl、AgI的Ksp大小 | 向5mL0.1mol/LAgNO3溶液中先加入4滴0.1mol/LNaCl溶液,再加入4滴0.1mol/LKI溶液 | 若先产生白色沉淀,后变为黄色沉淀,则AgI的Ksp较小 |
| D | 探究Na2SO3是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入BaCl2溶液 | 若有白色沉淀产生,则样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列实验操作能达到实验目的的是
| 操作 | 目的 | |
| A | 常温下,用 试纸测 试纸测 溶液 溶液  溶液 溶液 | 判断 和 和 酸性强弱 酸性强弱 |
 | 向含有酚酞的 溶液中滴入 溶液中滴入 溶液,观察溶液颜色的变化 溶液,观察溶液颜色的变化 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
 | 相同温度下,测得饱和 溶液的 溶液的 小于饱和 小于饱和 溶液的 溶液的 | 证明 酸性强于 酸性强于 |
 | 将 样品溶于稀 样品溶于稀 后,滴加 后,滴加 溶液,观察溶液是否变红 溶液,观察溶液是否变红 | 检验 样品是否变质 样品是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 探究氮、硫及其化合物的性质,下列实验方案、现象和结论都正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 将 样品溶于稀硫酸后,滴加 样品溶于稀硫酸后,滴加 溶液 溶液 | 溶液变红 |  已被氧化变质 已被氧化变质 |
| B | 向 溶液和盐酸反应后的溶液中加入紫色石蕊试液 溶液和盐酸反应后的溶液中加入紫色石蕊试液 | 溶液变红 | 说明盐酸已经过量 |
| C | 向两个同规格的烧瓶中分别充入同比例的 和 和 的混合气体,并分别浸泡于热水和冷水中 的混合气体,并分别浸泡于热水和冷水中 | 一段时间后,两个烧瓶内的颜色深浅不同 | 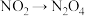 的转化存在限度 的转化存在限度 |
| D | 常温下,分别测定浓度均为 的 的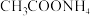 和 和 溶液的 溶液的 | 前者 小于后者 小于后者 | 说明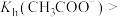 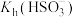 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 下列实验操作、现象和所得结论均正确的是
| 实验操作 | 现象 | 结论 | |
| A | 在灼热木炭中加入浓硫酸,将生成的气体依次通过品红溶液、饱和NaHCO3溶液、澄清石灰水 | 品红溶液褪色,澄清石灰水变浑浊 | 浓硫酸和木炭反应产生SO2和CO2气体 |
| B | 惰性电极电解CuCl2溶液,并用湿润的淀粉KI试纸检验阳极产生的气体 | 试纸先变蓝后褪色 | 阳极有氯气产生且氯气具有漂白性 |
| C | 取少量Na2SO3样品溶于蒸馏水,滴加足量稀盐酸,再加入足量BaCl2溶液 | 有白色沉淀生成 | 样品已经变质 |
| D | 用pH试纸测定浓度均为0.1mol·L-1的CH3COONa溶液和NaClO溶液的pH比较溶液pH大小 | 最终CH3COONa溶液对应的pH试纸蓝色较浅 | 酸性:CH3COOH>HClO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 下列实验方案、现象和结论均正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 取两份新制氯水,分别滴加AgNO3溶液和淀粉KI溶液 | 前者有白色沉淀,后者溶液变蓝 | 氯气与水反应存在限度 |
| B | 向稀硫酸中加入铜粉,再加入少量KNO3固体 | 开始无明显现象,加入KNO3后,溶液变蓝 | KNO3起催化作用 |
| C | 取少量Na2SO3样品溶于蒸馏水,滴加足量稀盐酸,再加入足量BaCl2溶液 | 有白色沉淀生成 | 样品已经变质 |
| D | 向浓度均为0.1mol·L-1的NaCl和Na2CO3溶液中分别滴加酚酞 | 前者不变色,后者变红 | 非金属性:C<Cl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 根据实验目的设计实验方案并进行实验,观察到相关现象,其中方案设计或结论正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 探究脱氧剂(主要成分是Fe粉)是否变质 | 取少量样品溶于盐酸,滴加KSCN溶液 | 无明显现象 | 脱氧剂没有变质 |
| B | 探究反应物浓度对反应: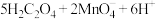 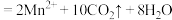 速率的影响 速率的影响 | 向A、B两支各盛有2 mL 0.2 mol/L H2C2O4溶液的试管中同时4 mL 0.01 mol/L KMnO4溶液、4 mL 0.02 mol/L KMnO4溶液,测定颜色褪去所需时间分别为 和 和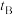 | 褪色时间: | 浓度增大,该反应速率加快 |
| C | 探究温度对水解平衡的影响 | 缓加热0.5 mol/L CH3COONa溶液到60℃,并用传感器测定溶液的pH,溶液的pH逐渐减小 | 溶液的pH逐渐减小 | 温度升高,水解平衡逆向移动 |
| D | 探究亚硫酸和次氯酸的酸性 | 向次氯酸钙的溶液中通入少量SO2 | 出现白色沉淀 | 酸性:H2SO3>HClO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 下列实验操作、现象与结论相匹配的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向 溶液中加入 溶液中加入 溶液 溶液 | 有白色沉淀生成 |  结合 结合 的能力比 的能力比 弱 弱 |
| B | 将 溶液和 溶液和 溶液分别加入 溶液分别加入 溶液中 溶液中 | 均出现白色沉淀 |  溶液和 溶液和 溶液均可使 溶液均可使 的水解平衡正向移动 的水解平衡正向移动 |
| C | 常温下,将 苯与 苯与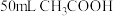 混合 混合 | 所得混合溶液的体积为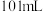 | 混合过程中削弱了 分子间的氢键,且苯与 分子间的氢键,且苯与 分子间的作用弱于氢键 分子间的作用弱于氢键 |
| D | 将 样品溶于稀 样品溶于稀 后,滴加 后,滴加 溶液 溶液 | 溶液显红色 |  晶体已氧化变质 晶体已氧化变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 下列方案设计、现象和结论有不正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 相同温度下,等质量的大理石与等体积等浓度的盐酸反应 | 粉状大理石产生气泡更快 | 反应速率:粉状大理石>块状大理石 |
| B | Na2SO3固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量BaCl2溶液 | 若有白色沉淀产生,则样品已经变质 |
| C | 比较CH3COOH和HClO的Ka大小 | 用pH试纸分别0.1mol•L-1CH3COONa溶液和NaClO溶液的pH | 若pH(NaClO)>pH(CH3COONa)则说明Ka(CH3COOH)>Ka(HClO) |
| D | 检验蛋白质性质 | 向鸡蛋清溶液中滴加醋酸铅溶液 | 溶液变浑浊,再加水浑浊不消失说明鸡蛋清溶液发生了变性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

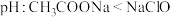
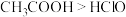
 加入
加入 强
强

