下列实验操作、现象与结论相匹配的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向 溶液中加入 溶液中加入 溶液 溶液 | 有白色沉淀生成 |  结合 结合 的能力比 的能力比 弱 弱 |
| B | 将 溶液和 溶液和 溶液分别加入 溶液分别加入 溶液中 溶液中 | 均出现白色沉淀 |  溶液和 溶液和 溶液均可使 溶液均可使 的水解平衡正向移动 的水解平衡正向移动 |
| C | 常温下,将 苯与 苯与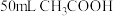 混合 混合 | 所得混合溶液的体积为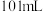 | 混合过程中削弱了 分子间的氢键,且苯与 分子间的氢键,且苯与 分子间的作用弱于氢键 分子间的作用弱于氢键 |
| D | 将 样品溶于稀 样品溶于稀 后,滴加 后,滴加 溶液 溶液 | 溶液显红色 |  晶体已氧化变质 晶体已氧化变质 |
| A.A | B.B | C.C | D.D |
更新时间:2024-04-08 09:28:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验方案设计、现象和结论都正确的是
| 选项 | 方案设计 | 现象 | 结论 |
| A | 向盛有少量蒸馏水的试管里滴加2滴 溶液,然后再滴加2滴KSCN溶液 溶液,然后再滴加2滴KSCN溶液 | 溶液颜色不变 |  比 比 稳定 稳定 |
| B | 取两份新制氯水,分别滴加AgNO3溶液和淀粉KI溶液 | 前者有白色沉淀,后者溶液变蓝色 | 氯气与水的反应存在限度 |
| C | 取少量样品苯于试管中,滴加适量的浓溴水 | 未观察到有白色沉淀产生 | 苯中不含有苯酚 |
| D | 向 和KSCN的混合溶液中滴入酸化的AgNO3溶液 和KSCN的混合溶液中滴入酸化的AgNO3溶液 | 溶液变红 | 氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】为测定某补铁剂中铁元素的价态,进行如下实验:
下列说法错误的是
步骤 | 实验操作 | 实验现象 |
1 | 取补铁剂水溶液,滴加KSCN溶液 | 无明显现象 |
2 | 取补铁剂水溶液,滴加NaOH溶液 | 无明显现象 |
3 | 取补铁剂酸(HCl)溶液,滴加KSCN溶液 | 溶液变为血红色 |
4 | 取补铁剂酸(HCl)溶液,滴加过量NaOH溶液 | 颜色加深,放入离心机离心后,溶液观察到少量红褐色沉淀 |
| A.该补铁剂在水中能溶解,但是难电离 |
B.步骤3说明补铁剂酸(HCl)溶液中一定有 |
C.步骤4说明补铁剂酸(HCl)溶液中一定没有 |
| D.该补铁剂与维生素C同时服用,有助于人体吸收铁元素 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列根据实验操作和实验现象所得出的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将FeCl2样品溶于盐酸后,滴加KSCN溶液 | 溶液变成红色 | 原FeCl2样品已变质 |
| B | 将Na2SO3样品溶于水,滴加入稀盐酸酸化的Ba(NO3)2溶液 | 产生白色沉淀 | 原Na2SO3样品已变质 |
| C | 向淀粉KI溶液中滴入3滴稀硫酸,再加入10%的H2O2溶液 | 滴入稀硫酸未见溶液变蓝;加入H2O2溶液后,溶液立即变蓝 | 酸性条件下,H2O2氧化性强于I2 |
| D | 向5mL0.5mol/LNaHCO3溶液中滴入2mL1mol/LBaCl2溶液 | 产生白色沉淀,且有无色气体生成 | 反应的化学方程式为2NaHCO3+BaCl2=BaCO3↓+2NaCl+CO2↑+H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:常温下浓度为0.1mol/L的下列溶液的pH如表:下列有关说法正确的是
溶质 | NaF | Na2CO3 | NaClO | NaHCO3 |
pH | 7.5 | 11.6 | 9.7 | 8.3 |
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF |
B.若将CO2通入0.1mol/LNa2CO3溶液至溶液呈中性,则溶液中:2c( )+c( )+c( )=0.1mol/L )=0.1mol/L |
| C.向Na2CO3溶液中通入足量的HF气体,化学反应方程式为:Na2CO3+2HF=CO2↑+H2O+2NaF |
| D.等体积等物质的量浓度的NaClO溶液与NaF溶液中离子总数大小:N(NaClO)>N(NaF) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
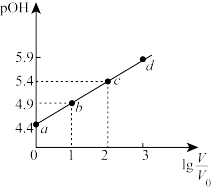
【推荐2】已知H3PO3与足量的NaOH溶液反应生成Na2HPO3。室温下向1 mol∙L−1Na2HPO3溶液中加水稀释,溶液的pOH与溶液稀释倍数关系如图。已知pOH=−lgc(OH-);lg4=0.60,  是开始溶液体积,V是加水后溶液体积。下列说法错误的是
是开始溶液体积,V是加水后溶液体积。下列说法错误的是
 是开始溶液体积,V是加水后溶液体积。下列说法错误的是
是开始溶液体积,V是加水后溶液体积。下列说法错误的是
| A.Na2HPO3的第一步水解常数约是10−8.8 |
| B.稀释100倍时溶液的pH=8.6 |
C.b点溶液中c(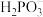 )+c( )+c( )+c(H3PO3)=1 mol∙L−1 )+c(H3PO3)=1 mol∙L−1 |
| D.H3PO3的第二步电离常数是6.4×10−6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列溶液中各微粒的浓度关系或说法正确的是
| A.0.1 mol•L-1 pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
B.等物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O;c(NH ) 由大到小的顺序是: ①>②>③>④ ) 由大到小的顺序是: ①>②>③>④ |
| C.a mol·L-1HCN溶液与b mol·L-1NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b |
| D.0.1mol·L-1的醋酸的pH=a,0.01mol·L-1的醋酸的pH=b,则a+1=b |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于物质结构与性质的说法,不正确的是
| A.Na、Mg、Al原子的电负性依次增大 |
| B.HCl和HI化学键的类型和分子的极性都相同 |
C.氨分子间存在氢键, 分子间没有氢键,故 分子间没有氢键,故 的熔沸点及稳定性均大于 的熔沸点及稳定性均大于 |
| D.基态钾原子核外电子共有19种运动状态,且其3s与4s轨道形状相同,能量不相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】硼酸(H3BO3)是一种片层状结构的白色晶体(如图),有油腻感,可做润滑剂。已知含氧酸的通式一般可以表示为(HO)mROn,酸的强度与酸中的非羟基氧原子数n有关,n越大,酸性越强。下列有关叙述正确的是


| A.H4SiO4酸性大于H3BO3酸性 |
| B.硼酸晶体类型与石墨相同 |
| C.1 mol H3BO3晶体中含有6mol氢键 |
| D.硼酸在加热时溶解度增大的原因是加热时氢键被破坏,有利于硼酸溶解 |
您最近一年使用:0次



