16. CH
3COOH为常见的弱酸,在工业生产和生活中有广泛的应用。
I.(1)常温下中和100 mL pH=3的CH
3COOH溶液和1 L pH=4的CH
3COOH溶液,需要等物质的量浓度的NaOH溶液的体积分别为V
1和V
2,则V
1_______V
2(填“>”、“=”或“<”) ;
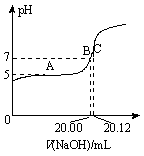
(2)常温下,用0.1000 mol/L的NaOH溶液滴定20.00 mL某未知浓度的CH
3COOH溶液,滴定曲线如图所示。其中A点所示溶液中c(CH
3COO
-)=2c(CH
3COOH),C点所示溶液中存在c(CH
3COO
-)+c(CH
3COOH)=c(Na
+)。则常温下CH
3COOH的电离常数K
a=
_________,CH
3COOH溶液的实际浓度为
____________;
Ⅱ.1100℃时,体积为2 L的恒容容器中发生如下反应:
Na
2SO
4(s)+4H
2(g)

Na
2S(s)+4H
2O(g)。
(1)下列能判断反应达到平衡状态的是
________;
A.容器中压强不变
B.混合气体密度不变
C.1 mol H-H键断裂同时形成2 mol H-O
D.H
2的体积分数不变
(2)若2 min时反应达平衡,此时气体质量增加8 g,则用H
2表示该反应的反应速率为
___________;
(3)某温度下该反应达平衡状态,测得混合气体的平均相对分子质量为14,则该温度下的平衡常数K为
_____________;
(4)若降低温度,K值减小,则反应的ΔH
______0(填“>”或“<”) ;
(5)若反应达平衡后,加入少量的H
2,再次平衡后,H
2O的体积分数
___________(填“增大”、“减小”或“不变”)。