名校
1 . 室温下,现有相同体积、 的氨水和
的氨水和 两种溶液:
两种溶液:
(1)溶液中水的电离程度:氨水_______  溶液。(填“
溶液。(填“ ”、“
”、“ ”或“
”或“ ”)
”)
(2)两种溶液分别加水稀释时的 变化曲线如图所示:
变化曲线如图所示: 点所在曲线对应的是
点所在曲线对应的是_______ (填溶液名称)
② 三点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积由大到小排序
三点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积由大到小排序_______ 。
 的氨水和
的氨水和 两种溶液:
两种溶液:(1)溶液中水的电离程度:氨水
 溶液。(填“
溶液。(填“ ”、“
”、“ ”或“
”或“ ”)
”)(2)两种溶液分别加水稀释时的
 变化曲线如图所示:
变化曲线如图所示: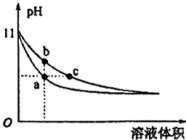
 点所在曲线对应的是
点所在曲线对应的是②
 三点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积由大到小排序
三点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积由大到小排序
您最近半年使用:0次
2 .  ,相同
,相同  的两种一元弱酸
的两种一元弱酸  与
与  溶液分别加水稀释,溶液
溶液分别加水稀释,溶液 随溶液体积变化的曲线如图所示。下列说法正确的是
随溶液体积变化的曲线如图所示。下列说法正确的是
 ,相同
,相同  的两种一元弱酸
的两种一元弱酸  与
与  溶液分别加水稀释,溶液
溶液分别加水稀释,溶液 随溶液体积变化的曲线如图所示。下列说法正确的是
随溶液体积变化的曲线如图所示。下列说法正确的是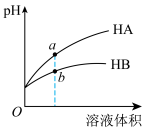
A.同浓度的 与 与  溶液中, 溶液中,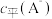 大于 大于 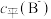 |
B.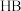 的酸性强于 的酸性强于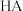 |
C. 点溶液的导电性大于 点溶液的导电性大于 点溶液 点溶液 |
D. 点的 点的 大于 大于 点的 点的  |
您最近半年使用:0次
3 . 25℃时,几种酸的电离平衡常数如下表所示:
| 酸 | CH3COOH | HCN | H2CO3 | HNO2 |
 | 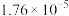 |  | 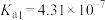  |  |
A.反应 能够发生 能够发生 |
| B.等物质的量的CH3COOH和CH3COONa的混合溶液呈碱性 |
C.CO2通入NaCN溶液中,反应的离子方程式为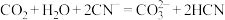 |
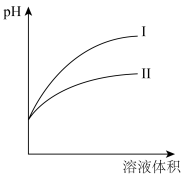
| D.常温下,等pH的醋酸和盐酸分别加等体积水稀释(如上图),I表示盐酸的稀释过程 |
您最近半年使用:0次
解题方法
4 . 常温下,分别取未知浓度的MOH和HA溶液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如图所示。下列叙述正确的是
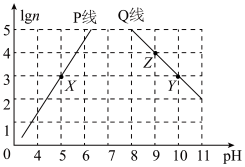
| A.P线代表HA的稀释图像且HA为强酸 |
| B.水的电离程度:Z>Y=X |
C.将X点溶液与Y点溶液混合至中性时, |
D.将X点溶液与Z点溶液等体积混合,所得溶液中一定有: |
您最近半年使用:0次
5 . 常温下,分别取未知浓度的 和
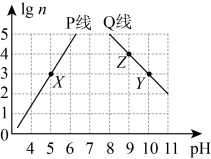
和 溶液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如图所示。下列叙述不正确的是
溶液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如图所示。下列叙述不正确的是
 和
和 溶液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如图所示。下列叙述不正确的是
溶液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如图所示。下列叙述不正确的是
A.P线代表 的稀释图像 的稀释图像 |
B.Z点溶液稀释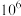 倍,所得溶液 倍,所得溶液 |
C.X、Y、Z点水的电离程度: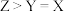 |
D.将 溶液和 溶液和 溶液等体积混合,所得溶液呈碱性 溶液等体积混合,所得溶液呈碱性 |
您最近半年使用:0次
解题方法
6 . 某温度下,pH=11的氨水和NaOH溶液分别加水稀释至原体积的100倍,溶液的pH随溶液体积变化的曲线如图所示。下列说法错误的是

| A.a值一定大于9 |
| B.Ⅰ为NaOH溶液稀释时溶液的pH变化曲线 |
| C.完全中和稀释相同倍数后的两溶液,消耗相同浓度的稀H2SO4的体积:NaOH溶液<氨水 |
| D.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大 |
您最近半年使用:0次
2024-03-17更新
|
71次组卷
|
2卷引用:黑龙江省海林市朝鲜族中学2023-2024学年高二上学期第二次月考化学试题
7 . 室温下,体积均为10mL、pH均为11的氨水和NaOH溶液分别加水稀释至原体积的100倍,溶液的pH随溶液体积变化的曲线如图所示。下列说法正确的是
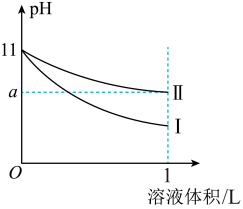

A. |
| B.Ⅱ为NaOH溶液稀释时溶液的pH变化曲线 |
| C.完全中和1L两溶液,消耗相同浓度的稀盐酸溶液的体积:NaOH溶液<氨水 |
| D.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大 |
您最近半年使用:0次
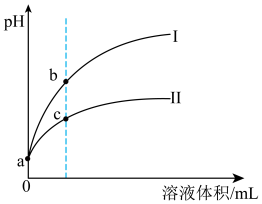
8 . 已知常温时HClO的 ,HF的
,HF的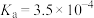 ,现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是
,现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是
 ,HF的
,HF的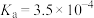 ,现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是
,现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是
| A.曲线Ⅰ为次氯酸稀释时pH变化曲线 |
| B.取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗次氯酸的体积较小 |
| C.a点时,若都加入相同大小的锌粒,此时与氢氟酸反应的速率大 |
| D.溶液中水的电离程度:a>b>c |
您最近半年使用:0次
9 . 已知25℃时,部分弱电解质的电离平衡常数数据如下表:
回答下列问题:
(1)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的 由小到大的顺序为
由小到大的顺序为___________ (填字母序号)。
(2)常温下,0.1mol/L醋酸溶液加水稀释过程中,下列表达式的数据减小的是___________(填字母序号)。
(3)25℃时,将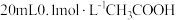 溶液和
溶液和 溶液分别与
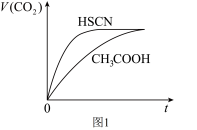
溶液分别与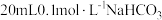 溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生
溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是___________ 反应结束后所得两溶液中,c(SCN-)_________ c(CH3COO-)(填“>”“<”或“=”)。
(4)体积均为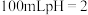 的
的 与一元酸
与一元酸 ,加水稀释过程中
,加水稀释过程中 与溶液体积的关系如图2所示,则
与溶液体积的关系如图2所示,则 的电离平衡常数
的电离平衡常数___________ (填“大于”、“小于”或“等于”) 的电离平衡常数。
的电离平衡常数。

(5)25℃时,在 与
与 的混合溶液中,若测得
的混合溶液中,若测得 ,则溶液中
,则溶液中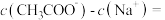
________ mol/L(填精确值),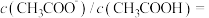
___________ 。
| 弱酸化学式 |  |  |  |  |
| 电离平衡常数 | 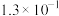 |  |  | 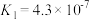 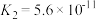 |
(1)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的
 由小到大的顺序为
由小到大的顺序为(2)常温下,0.1mol/L醋酸溶液加水稀释过程中,下列表达式的数据减小的是___________(填字母序号)。
A. | B. |
C.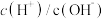 | D. |
(3)25℃时,将
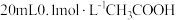 溶液和
溶液和 溶液分别与
溶液分别与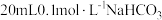 溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生
溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是
(4)体积均为
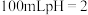 的
的 与一元酸
与一元酸 ,加水稀释过程中
,加水稀释过程中 与溶液体积的关系如图2所示,则
与溶液体积的关系如图2所示,则 的电离平衡常数
的电离平衡常数 的电离平衡常数。
的电离平衡常数。
(5)25℃时,在
 与
与 的混合溶液中,若测得
的混合溶液中,若测得 ,则溶液中
,则溶液中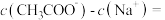
您最近半年使用:0次
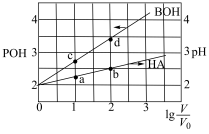
10 . 常温下,将体积均为 的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随
的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随 的变化如图所示。已知
的变化如图所示。已知 ,下列说法正确的是
,下列说法正确的是
 的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随
的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随 的变化如图所示。已知
的变化如图所示。已知 ,下列说法正确的是
,下列说法正确的是
A.电离常数: |
| B.水的电离程度:b>d |
C.升温,a点溶液中 增大 增大 |
| D.等浓度HA和BOH溶液等体积混合,溶液的pH<7 |
您最近半年使用:0次



