名校
解题方法
1 . 常温下将NaOH溶液滴加到 溶液中,混合溶液的pH与离子浓度变化的关系如图所示[纵坐标为
溶液中,混合溶液的pH与离子浓度变化的关系如图所示[纵坐标为 或
或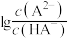 ]。下列叙述正确的是
]。下列叙述正确的是
 溶液中,混合溶液的pH与离子浓度变化的关系如图所示[纵坐标为
溶液中,混合溶液的pH与离子浓度变化的关系如图所示[纵坐标为 或
或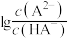 ]。下列叙述正确的是
]。下列叙述正确的是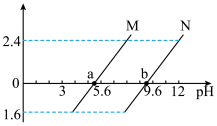
A.曲线N表示pH与 的关系 的关系 |
B.图中a点对应溶液中: |
C.NaHA溶液中: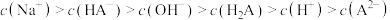 |
| D.溶液pH从5.6到9.6的过程中,水的电离程度先增大后减小 |
您最近半年使用:0次
今日更新
|
450次组卷
|
6卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题江西省部分地区2023-2024学年高三下学期3月月考化学试题甘肃省酒泉市九师联盟2023-2024学年高三下学期3月月考化学试题(已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)河南省九师联盟2023-2024学年高三下学期3月质量检测理科综合化学试题湖北省九师联盟2024届高三下学期3月质量检测(W-G)化学试卷
名校
解题方法
2 . 25℃时,用0.1
 溶液滴定同浓度的
溶液滴定同浓度的 溶液,
溶液, 被滴定分数
被滴定分数 与
与 值、微粒分布分数
值、微粒分布分数 ,X表示
,X表示 、
、 或
或 ]的关系如图所示,下列说法正确的是
]的关系如图所示,下列说法正确的是

 溶液滴定同浓度的
溶液滴定同浓度的 溶液,
溶液, 被滴定分数
被滴定分数 与
与 值、微粒分布分数
值、微粒分布分数 ,X表示
,X表示 、
、 或
或 ]的关系如图所示,下列说法正确的是
]的关系如图所示,下列说法正确的是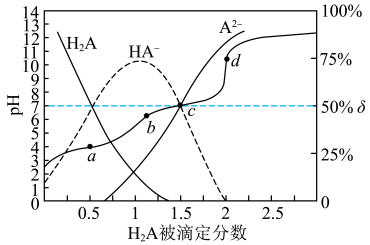
A.用 溶液滴定0.1 溶液滴定0.1 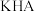 溶液可以用酚酞作指示剂 溶液可以用酚酞作指示剂 |
B.25℃时, 第二步电离平衡常数 第二步电离平衡常数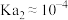 |
C.c点溶液中: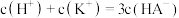 |
D.a、b、c、d四点溶液中水的电离程度: |
您最近半年使用:0次
今日更新
|
261次组卷
|
3卷引用:云南省大理白族自治州2024届高三第二次复习统一检测理综-化学试卷
3 . 25℃时,向100mL 0.1
 溶液中滴加0.1
溶液中滴加0.1 KOH溶液,溶液pH与KOH溶液体积的关系曲线如图所示,对图中四个点a、b、c,d的分析中,不正确的是
KOH溶液,溶液pH与KOH溶液体积的关系曲线如图所示,对图中四个点a、b、c,d的分析中,不正确的是

 溶液中滴加0.1
溶液中滴加0.1 KOH溶液,溶液pH与KOH溶液体积的关系曲线如图所示,对图中四个点a、b、c,d的分析中,不正确的是
KOH溶液,溶液pH与KOH溶液体积的关系曲线如图所示,对图中四个点a、b、c,d的分析中,不正确的是
A.a点存在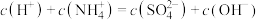 |
B.b点存在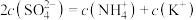 |
C.d点水的电离程度最大,且存在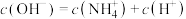 |
D.c点存在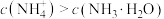 |
您最近半年使用:0次
4 . 将 溶液与氨水等体积混合,测得
溶液与氨水等体积混合,测得 和铜氨各级配离子的物质的量分数
和铜氨各级配离子的物质的量分数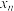 与平衡体系中
与平衡体系中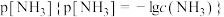 的关系如下图所示。下列说法中错误的是
的关系如下图所示。下列说法中错误的是
 溶液与氨水等体积混合,测得
溶液与氨水等体积混合,测得 和铜氨各级配离子的物质的量分数
和铜氨各级配离子的物质的量分数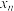 与平衡体系中
与平衡体系中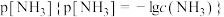 的关系如下图所示。下列说法中错误的是
的关系如下图所示。下列说法中错误的是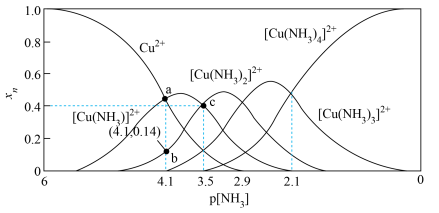
| A.a点的纵坐标约为0.43 |
B.平衡体系中 越大越有利于配位数大的铜氨配合物的形成 越大越有利于配位数大的铜氨配合物的形成 |
C.反应 的平衡常数为 的平衡常数为 |
D.p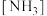 在 在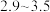 时,混合溶液中含铜微粒浓度最大的是 时,混合溶液中含铜微粒浓度最大的是 |
您最近半年使用:0次
5 . Al3+与F-具有很强的亲和性,AlF在NaF溶液中存在分步电离: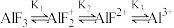 。常温下实验测定
。常温下实验测定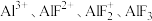 的百分含量随
的百分含量随 变化如图所示,下列说法错误的是
变化如图所示,下列说法错误的是
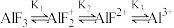 。常温下实验测定
。常温下实验测定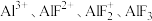 的百分含量随
的百分含量随 变化如图所示,下列说法错误的是
变化如图所示,下列说法错误的是
A.曲线b表示 |
B.N点时, |
C.M点溶液中 |
D.常温下, 化学平衡常数的数量级为1015 化学平衡常数的数量级为1015 |
您最近半年使用:0次
名校
解题方法
6 . 某学习小组进行如下实验:向均为 某浓度的
某浓度的 和
和 溶液中分别滴加
溶液中分别滴加 的盐酸,溶液
的盐酸,溶液 随滴加
随滴加 溶液体积
溶液体积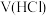 的变化如下图。下列说法正确的是加入
的变化如下图。下列说法正确的是加入
 某浓度的
某浓度的 和
和 溶液中分别滴加
溶液中分别滴加 的盐酸,溶液
的盐酸,溶液 随滴加
随滴加 溶液体积
溶液体积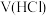 的变化如下图。下列说法正确的是加入
的变化如下图。下列说法正确的是加入
A.曲线I是 溶液的滴定曲线 溶液的滴定曲线 |
B. 三点,水的电离程度为 三点,水的电离程度为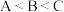 |
C.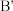 点存在 点存在 |
D.II曲线上任意一点存在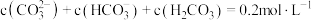 |
您最近半年使用:0次
7 . 含硫化合物在能源、材料及环境等工业领域均有广泛的应用。
Ⅰ.工业废气 分解可制取
分解可制取 。
。
(1)已知热化学方程式:
ⅰ.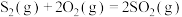

ⅱ.

ⅲ.

 热分解反应
热分解反应 的
的
___________ (用含 、
、 、
、 的式子表示)。
的式子表示)。
(2)一定温度下,2mol 在体积为VL的恒容密闭容器中发生上述分解反应,ts时
在体积为VL的恒容密闭容器中发生上述分解反应,ts时 的产率为40%,则0~ts内
的产率为40%,则0~ts内 的平均分解速率为
的平均分解速率为___________  ;
; 充分分解达到平衡时,容器中
充分分解达到平衡时,容器中 和
和 的分压相等,则该温度下的平衡常数
的分压相等,则该温度下的平衡常数
___________ 。
Ⅱ.KSCN可用于镀铬工业。常温下,用KSCN配制电镀液,溶液中 与
与 发生第一、二步络合的反应如下:
发生第一、二步络合的反应如下:
ⅳ.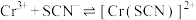
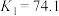
ⅴ.

(3)根据以上络合反应,下列说法正确的有___________(填字母)。
(4)常温下,某研究小组配制了起始浓度 、
、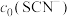 不同的系列溶液,测得平衡时
不同的系列溶液,测得平衡时 、
、 、
、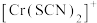 的浓度
的浓度 (含铬微粒)随
(含铬微粒)随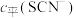 的变化曲线如图所示,平衡后其他含铬微粒
的变化曲线如图所示,平衡后其他含铬微粒 (3≤x≤6,图中未画出)总浓度为amol/L。
(3≤x≤6,图中未画出)总浓度为amol/L。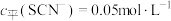 时,图中含铬微粒按浓度由大到小的顺序为
时,图中含铬微粒按浓度由大到小的顺序为___________ ;A点时,溶液中 的平衡浓度为
的平衡浓度为___________ (列出计算式即可)。
②在某电镀工艺中, 的浓度需要在
的浓度需要在 以上,结合计算判断C点所对应的溶液能否用于该电镀工艺
以上,结合计算判断C点所对应的溶液能否用于该电镀工艺________ (写出计算过程)。
Ⅰ.工业废气
 分解可制取
分解可制取 。
。(1)已知热化学方程式:
ⅰ.
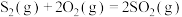

ⅱ.


ⅲ.


 热分解反应
热分解反应 的
的
 、
、 、
、 的式子表示)。
的式子表示)。(2)一定温度下,2mol
 在体积为VL的恒容密闭容器中发生上述分解反应,ts时
在体积为VL的恒容密闭容器中发生上述分解反应,ts时 的产率为40%,则0~ts内
的产率为40%,则0~ts内 的平均分解速率为
的平均分解速率为 ;
; 充分分解达到平衡时,容器中
充分分解达到平衡时,容器中 和
和 的分压相等,则该温度下的平衡常数
的分压相等,则该温度下的平衡常数
Ⅱ.KSCN可用于镀铬工业。常温下,用KSCN配制电镀液,溶液中
 与
与 发生第一、二步络合的反应如下:
发生第一、二步络合的反应如下:ⅳ.
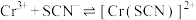
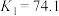
ⅴ.


(3)根据以上络合反应,下列说法正确的有___________(填字母)。
| A.加水稀释后,溶液中离子的总数减少 |
B.加入少量 固体,溶液中含铬微粒总数不变 固体,溶液中含铬微粒总数不变 |
C.反应 的平衡常数 的平衡常数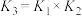 |
D.溶液中 减小, 减小, 与 与 浓度的比值减小 浓度的比值减小 |
(4)常温下,某研究小组配制了起始浓度
 、
、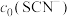 不同的系列溶液,测得平衡时
不同的系列溶液,测得平衡时 、
、 、
、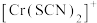 的浓度
的浓度 (含铬微粒)随
(含铬微粒)随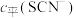 的变化曲线如图所示,平衡后其他含铬微粒
的变化曲线如图所示,平衡后其他含铬微粒 (3≤x≤6,图中未画出)总浓度为amol/L。
(3≤x≤6,图中未画出)总浓度为amol/L。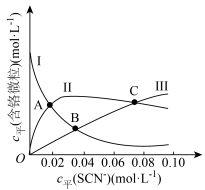
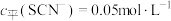 时,图中含铬微粒按浓度由大到小的顺序为
时,图中含铬微粒按浓度由大到小的顺序为 的平衡浓度为
的平衡浓度为②在某电镀工艺中,
 的浓度需要在
的浓度需要在 以上,结合计算判断C点所对应的溶液能否用于该电镀工艺
以上,结合计算判断C点所对应的溶液能否用于该电镀工艺
您最近半年使用:0次
名校
解题方法
8 . 常温下,亚砷酸 及其钠盐水溶液中的
及其钠盐水溶液中的 种
种 四种含砷微粒的分布系数(分布系数
四种含砷微粒的分布系数(分布系数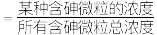 )与
)与 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 及其钠盐水溶液中的
及其钠盐水溶液中的 种
种 四种含砷微粒的分布系数(分布系数
四种含砷微粒的分布系数(分布系数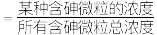 )与
)与 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是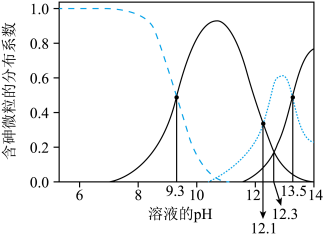
A.当 时,主要含砷微粒为 时,主要含砷微粒为 |
B.在水中 的 的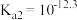 |
C. 的 的 与 与 的 的 等体积混合后,得到的溶液呈碱性 等体积混合后,得到的溶液呈碱性 |
D. 与 与 反应至 反应至 时, 时,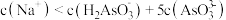 |
您最近半年使用:0次
名校
9 . 某温度下, 与不同pH的
与不同pH的 体系反应可生成不同的沉淀。下面图1表示
体系反应可生成不同的沉淀。下面图1表示 体系中各含碳粒子的物质的量分数与pH的关系。图2表示
体系中各含碳粒子的物质的量分数与pH的关系。图2表示 与不同pH的
与不同pH的 体系反应生成沉淀的情况,其中曲线Ⅰ的离子浓度关系符合
体系反应生成沉淀的情况,其中曲线Ⅰ的离子浓度关系符合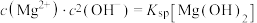 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合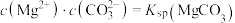 [注:起始
[注:起始 mol⋅L
mol⋅L ,不同pH下
,不同pH下 由图1得到]。
由图1得到]。
 与不同pH的
与不同pH的 体系反应可生成不同的沉淀。下面图1表示
体系反应可生成不同的沉淀。下面图1表示 体系中各含碳粒子的物质的量分数与pH的关系。图2表示
体系中各含碳粒子的物质的量分数与pH的关系。图2表示 与不同pH的
与不同pH的 体系反应生成沉淀的情况,其中曲线Ⅰ的离子浓度关系符合
体系反应生成沉淀的情况,其中曲线Ⅰ的离子浓度关系符合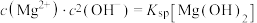 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合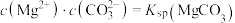 [注:起始
[注:起始 mol⋅L
mol⋅L ,不同pH下
,不同pH下 由图1得到]。
由图1得到]。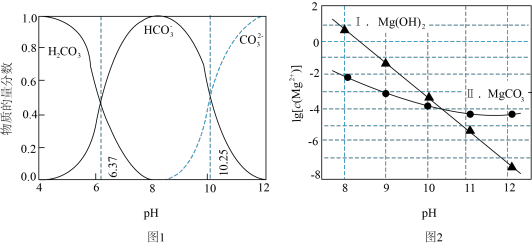
A.上述 体系呈中性时, 体系呈中性时,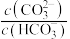 一定是 一定是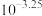 |
B.符合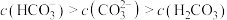 的pH范围: 的pH范围: |
C. , ,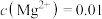 mol⋅L mol⋅L 时,溶液中存在 时,溶液中存在 和 和 两种沉淀 两种沉淀 |
D. , ,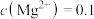 mol⋅L mol⋅L 时可发生反应: 时可发生反应: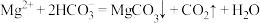 |
您最近半年使用:0次
10 . 常温下,水溶液中H2A、HA-、A2-、HB、B-的分布系数 [如
[如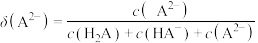 ]随POH变化曲线如图1所示,溶液中
]随POH变化曲线如图1所示,溶液中 与
与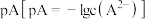 关系如图2所示。用0.1mol·L-1H2A溶液滴定20.00mL0.1mol·L-1BaB2溶液,若混合后溶液体积变化忽略不计,下列说法错误的是
关系如图2所示。用0.1mol·L-1H2A溶液滴定20.00mL0.1mol·L-1BaB2溶液,若混合后溶液体积变化忽略不计,下列说法错误的是
 [如
[如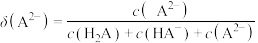 ]随POH变化曲线如图1所示,溶液中
]随POH变化曲线如图1所示,溶液中 与
与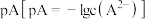 关系如图2所示。用0.1mol·L-1H2A溶液滴定20.00mL0.1mol·L-1BaB2溶液,若混合后溶液体积变化忽略不计,下列说法错误的是
关系如图2所示。用0.1mol·L-1H2A溶液滴定20.00mL0.1mol·L-1BaB2溶液,若混合后溶液体积变化忽略不计,下列说法错误的是
A.常温下,H2A的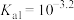 |
B.当滴入5.00mLH2A溶液时,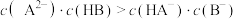 |
| C.当滴入20.00mLH2A溶液时,此时溶液的pH约为5.1 |
D.当溶液的pOH=7时, |
您最近半年使用:0次
7日内更新
|
575次组卷
|
2卷引用:山东省济南市2023-2024学年高三下学期3月模拟(一模)考试化学试题



