18.

是一种易溶于热水,微溶于冷水,难溶于乙醇的紫红色晶体,可利用下图装置制备。
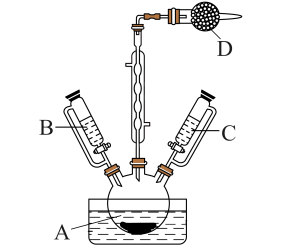
已知:①Co
2+在溶液中较稳定,

具有较强还原性;
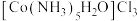
为深红色晶体;
②

,
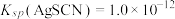
。
具体实验步骤如下:
I.在锥形瓶中,将12.5gNH
4Cl溶于50mL水中,加热至沸,加入25.0g研细的CoCl
2·6H
2O晶体,溶解得到混合溶液;
Ⅱ.将上述混合液倒入仪器A中,用冰水浴冷却,利用仪器B分批次加入75mL试剂X,并充分搅拌,无沉淀析出;
Ⅲ.再利用仪器C逐滴加入20mL试剂Y,水浴加热至50~60℃,不断搅拌溶液,直到气泡终止放出,溶液变为深红色;
Ⅳ.再换另一个仪器C慢慢注入75mL浓盐酸,50~60℃水浴加热20min,再用冰水浴冷却至室温,便有大量紫红色晶体析出,最后转移至布氏漏斗中减压过滤;
Ⅴ.依次用不同试剂洗涤晶体,再将晶体转移至烘箱中干燥1小时,最终得到mg产品。
回答下列问题:
(1)研细CoCl
2·6H
2O晶体的仪器名称为
___________,仪器D中的试剂为
___________。
(2)步骤Ⅱ、步骤Ⅲ中使用试剂X和试剂Y分别为
___________、
___________(填标号),步骤Ⅱ中75mL试剂X需分批次滴加的目的是
___________。
①浓氨水
②NaOH溶液
③KMnO
4溶液
④30%双氧水
(3)写出步骤Ⅲ中发生反应的离子方程式
___________。
(4)步骤Ⅴ中使用的洗涤试剂有冰水、乙醇、冷的盐酸,洗涤剂使用的先后顺序是冰水、
___________。
(5)最终获得产品会含少量杂质
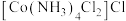
或

,产品组成可表示为

,通过测定z值可进一步测定产品纯度,进行如下实验:
实验Ⅰ:称取一定质量的产品溶解后,加入几滴K
2CrO
4溶液作指示剂,用cmol·L
-1AgNO
3标准溶液滴定达终点时,消耗

。
实验Ⅱ:另取相同质量的产品,加入

稍过量cmol·L
-1AgNO
3标准溶液,加热至沸使钴配合物分解,加入硝基苯静置、分层,将白色沉淀完全包裹,再加入几滴

溶液作指示剂,用cmol·L
-1KSCN标准溶液滴定剩余的AgNO
3,达终点时消耗
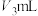
。
计算
 ___________
___________(用

、

和

表示);若实验Ⅱ中加入硝基苯的量太少,会导致y值
___________(填“偏大”、“偏小”或“不变”)。