名校
1 . 按要求填空:
(1)用系统命名法命名: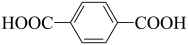 的苯环上的碳原子的杂化方式为
的苯环上的碳原子的杂化方式为___________ ,羧基上碳原子的杂化方式为___________ ,最多有___________ 个原子共平面。
(3)正硝酸钠( )为白色晶体,是一种重要的化工原料。
)为白色晶体,是一种重要的化工原料。
① 阴离子的空间构型为
阴离子的空间构型为___________ ,其中心原子杂化方式为___________ 。
②写出一种与 的阴离子互为等电子体的阴离子或分子
的阴离子互为等电子体的阴离子或分子___________ (填化学式)。
(4) 的电子式为
的电子式为___________ ; 中H-N-H键角比
中H-N-H键角比 中H-N-H键角
中H-N-H键角_________ (填“大”或“小”),理由是_____________ 。
(5)若硝酸的结构表示为 ,已知硝酸与水分子可形成一水合二硝酸结晶水合物(
,已知硝酸与水分子可形成一水合二硝酸结晶水合物(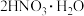 ),水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式
),水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式______ (氢键用“…”表示)。
(6)已知NaCl和MgO的晶体结构相似,熔点较高的是____________________ (填化学式),原因是______________________ 。
(1)用系统命名法命名:
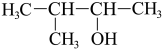

 的苯环上的碳原子的杂化方式为
的苯环上的碳原子的杂化方式为(3)正硝酸钠(
 )为白色晶体,是一种重要的化工原料。
)为白色晶体,是一种重要的化工原料。①
 阴离子的空间构型为
阴离子的空间构型为②写出一种与
 的阴离子互为等电子体的阴离子或分子
的阴离子互为等电子体的阴离子或分子(4)
 的电子式为
的电子式为 中H-N-H键角比
中H-N-H键角比 中H-N-H键角
中H-N-H键角(5)若硝酸的结构表示为
 ,已知硝酸与水分子可形成一水合二硝酸结晶水合物(
,已知硝酸与水分子可形成一水合二硝酸结晶水合物(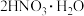 ),水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式
),水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式(6)已知NaCl和MgO的晶体结构相似,熔点较高的是
您最近半年使用:0次
解题方法
2 . 含氮物质在工业上应用非常广泛。将单质钡(Ba)、铼(Re)以一定比例混合,于特制容器中加热,依次通入N2、O2可制得某黑色晶体,该晶体晶胞如图所示,含有多个由Ba(+2)、Re(+4)、O(-2)和N(-3)组成的八面体与平面三角形,括号中为其化合价。
(1)基态Ba原子的简化电子排布式为___________ ,N、O、Ba简单氢化物的沸点由高到低的顺序为___________ (填化学式)。
(2)NO 中N原子的杂化方式为
中N原子的杂化方式为___________ ,下列离子或分子与 互为等电子体的是
互为等电子体的是___________ (填标号)。
a.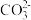 b.
b. c.SO3 d.
c.SO3 d.
(3)苯胺(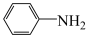 )中N原子与苯环形成p-π共轭,
)中N原子与苯环形成p-π共轭, 、
、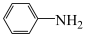 、
、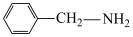 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是___________ 。
(4)该晶体中含有的八面体和平面三角形的个数比为___________ ,晶体的化学式为___________ 。
(5)晶胞参数为apm、apm、cpm, ,
,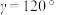 ,该晶体的密度为
,该晶体的密度为___________ g·cm-1(写出表达式)。

(1)基态Ba原子的简化电子排布式为
(2)NO
 中N原子的杂化方式为
中N原子的杂化方式为 互为等电子体的是
互为等电子体的是a.
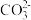 b.
b. c.SO3 d.
c.SO3 d.
(3)苯胺(
 )中N原子与苯环形成p-π共轭,
)中N原子与苯环形成p-π共轭, 、
、 、
、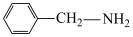 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是(4)该晶体中含有的八面体和平面三角形的个数比为
(5)晶胞参数为apm、apm、cpm,
 ,
,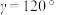 ,该晶体的密度为
,该晶体的密度为
您最近半年使用:0次
解题方法
3 . CaCN2可以作为固态氮肥,并改善土壤酸性,通过 反应制备。下列说法错误的是
反应制备。下列说法错误的是
 反应制备。下列说法错误的是
反应制备。下列说法错误的是| A.该反应为熵增过程 |
| B.该反应实现了氮的固定 |
| C.该反应需在无水条件下进行 |
D. 的电子式为 的电子式为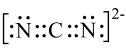 |
您最近半年使用:0次
解题方法
4 . 一种叠氮化合物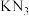 的晶胞结构如下图。下列说法错误的是
的晶胞结构如下图。下列说法错误的是
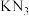 的晶胞结构如下图。下列说法错误的是
的晶胞结构如下图。下列说法错误的是
A. 空间构型为直线形 空间构型为直线形 |
B.该晶体中每个K+周围距离最近且相等的 共有6个 共有6个 |
C.该晶体的密度为 |
| D.可用X射线衍射法测定该晶体结构 |
您最近半年使用:0次
名校
解题方法
5 . 类推的思维方法在化学学习中应用广泛,但类推出的结论需经过实践的检验才能确定其正确与否。下列几种类推结论错误的是
| A.H2O是“V形分子”,则H2S是“V形分子” | B.SO2是极性分子,则O3是极性分子 |
| C.键角H2O>H2S,则键角NH3>PH3 | D.电负性P<S,则第一电离能P<S |
您最近半年使用:0次
名校
解题方法
6 . 根据原子结构,分子结构与性质的相关知识,回答下列问题:
(1)基态铜元素的价层电子轨道表示式为___________ ,核外有___________ 种不同运动状态的电子。
(2) 分子的VSEPR模型为
分子的VSEPR模型为___________ ; 分子的立体构型为
分子的立体构型为___________ 。
(3)熔点比较:
___________  填“>”、“<”或“=”,下同);沸点比较:
填“>”、“<”或“=”,下同);沸点比较:
___________  ,原因是
,原因是___________ 。
(4) 的大
的大 键表示为
键表示为___________ ,与其互为等电子体的微粒有___________ (任写一种)。
(1)基态铜元素的价层电子轨道表示式为
(2)
 分子的VSEPR模型为
分子的VSEPR模型为 分子的立体构型为
分子的立体构型为(3)熔点比较:

 填“>”、“<”或“=”,下同);沸点比较:
填“>”、“<”或“=”,下同);沸点比较:
 ,原因是
,原因是(4)
 的大
的大 键表示为
键表示为
您最近半年使用:0次
名校
解题方法
7 . 科学家研究发现:等电子体的空间结构相同,则下列有关说法中正确的是
A.BF3和CO 是等电子体,均为平面正三角形结构 是等电子体,均为平面正三角形结构 |
| B.B3N3H6和苯(C6H6)是等电子体,B3N3H6分子中不存在“肩并肩”式重叠的轨道 |
| C.NH3和PCl3是等电子体,均为三角锥形结构 |
D.CH4和NH 是等电子体,键角均为60° 是等电子体,键角均为60° |
您最近半年使用:0次
名校
解题方法
8 . 价层电子对互斥理论可以预测某些微粒的空间结构。下列说法错误的是
| A.BF3和NF3均为非极性分子 | B.PCl3、NCl3的空间构型都是三角锥形 |
| C.SO2和SO3的VSEPR模型均为平面三角形 | D.CO2与N 的键角相等 的键角相等 |
您最近半年使用:0次
9 . 回答下列问题。
(1)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸常被用作碳包覆的碳源,其易溶于水的原因是___________ 。1mol抗坏血酸中手性碳原子的数目为___________ 。 分子的空间结构是平面四边形。它有两种空间异构体——俗称顺铂和反铂。其结构简式如图,在水中的溶解性大小为顺铂
分子的空间结构是平面四边形。它有两种空间异构体——俗称顺铂和反铂。其结构简式如图,在水中的溶解性大小为顺铂___________ (填“>”或“<”)反铂。 分子
分子___________ (填“具有”“不具有”)手性。
(3)根据等电子原理,写出两个与 具有相同空间结构的分子或离子
具有相同空间结构的分子或离子___________ 。
(4)已知苯酚(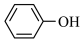 )具有弱酸性,其
)具有弱酸性,其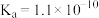 ;水杨酸离子(
;水杨酸离子( )能形成分子内氢键,据此判断相同温度下酸性强弱比较:水杨酸离子
)能形成分子内氢键,据此判断相同温度下酸性强弱比较:水杨酸离子___________ (填“>”或“<”)苯酚,其原因是___________ 。
(5)B、Al,Ga为同主族元素, ,
, 在一定条件下均易形成双聚分子,而
在一定条件下均易形成双聚分子,而 却很难形成双聚分子,其主要原因是
却很难形成双聚分子,其主要原因是 分子内形成了大
分子内形成了大 键,该大
键,该大 键可表示为
键可表示为___________ 。(分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数)
键的电子数)
(1)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸常被用作碳包覆的碳源,其易溶于水的原因是

 分子的空间结构是平面四边形。它有两种空间异构体——俗称顺铂和反铂。其结构简式如图,在水中的溶解性大小为顺铂
分子的空间结构是平面四边形。它有两种空间异构体——俗称顺铂和反铂。其结构简式如图,在水中的溶解性大小为顺铂 分子
分子(3)根据等电子原理,写出两个与
 具有相同空间结构的分子或离子
具有相同空间结构的分子或离子(4)已知苯酚(
 )具有弱酸性,其
)具有弱酸性,其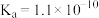 ;水杨酸离子(
;水杨酸离子( )能形成分子内氢键,据此判断相同温度下酸性强弱比较:水杨酸离子
)能形成分子内氢键,据此判断相同温度下酸性强弱比较:水杨酸离子(5)B、Al,Ga为同主族元素,
 ,
, 在一定条件下均易形成双聚分子,而
在一定条件下均易形成双聚分子,而 却很难形成双聚分子,其主要原因是
却很难形成双聚分子,其主要原因是 分子内形成了大
分子内形成了大 键,该大
键,该大 键可表示为
键可表示为 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数)
键的电子数)
您最近半年使用:0次
名校
10 . 石灰氮(CaCN2)是一种氮素肥效长的固态肥料,同时也是一种低毒、无残留的农药。工业上合成方法之一为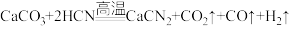 。回答下列问题:
。回答下列问题:
(1)已知Sn和C同主族,Sn的原子序数为50,基态Sn原子的价层电子排布图为_____ ;与Ca同周期未成对电子数最多的元素是_____ (填元素符号)。
(2)N原子核外不同运动状态的电子有_____ 种;下列属于氮原子激发态的电子排布式有_____ 。(填字母序号)
A. [He]2s22p3 B. [He]2s22p23s1 C. [He]2s12p33s1 D. [He]2s22p2
(3)上述制备反应中生成物CO2分子中σ键的类型为_____ 。(填序号)
①s-pσ键②p-pσ键③sp-pσ键④sp2-pσ键
(4)已知等电子原理是指原子总数相同、价电子总数相同的分子或离子具有相同的结构特征,其性质相近。这样的粒子互称为等电子体,例如CO和N2互为等电子体,请写出CO的电子式:_____ 。
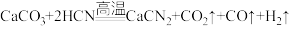 。回答下列问题:
。回答下列问题:(1)已知Sn和C同主族,Sn的原子序数为50,基态Sn原子的价层电子排布图为
(2)N原子核外不同运动状态的电子有
A. [He]2s22p3 B. [He]2s22p23s1 C. [He]2s12p33s1 D. [He]2s22p2
(3)上述制备反应中生成物CO2分子中σ键的类型为
①s-pσ键②p-pσ键③sp-pσ键④sp2-pσ键
(4)已知等电子原理是指原子总数相同、价电子总数相同的分子或离子具有相同的结构特征,其性质相近。这样的粒子互称为等电子体,例如CO和N2互为等电子体,请写出CO的电子式:
您最近半年使用:0次



