解题方法
1 . 常温下,用0.20mol·L-1盐酸滴定25.00mL0.20mol·L-1NH3·H2O溶液,所得溶液的pH、NH4+和NH3·H2O的物质的量分数(x)与滴加盐酸体积的关系如图所示。下列说法不正确 的是
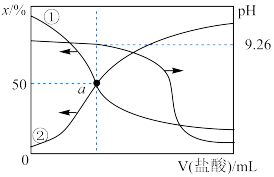
| A.曲线①代表x(NH3·H2O) |
| B.当溶液显中性时,滴入盐酸的体积小于25.00mL |
| C.NH3·H2O的电离常数约为1×10-9.26 |
D.a点的溶液中存在c(NH )=c(NH3·H2O)>c(Cl-) )=c(NH3·H2O)>c(Cl-) |
您最近半年使用:0次
2 . 25℃时,向10mL0.10mol/L的一元弱酸HA(Ka=1.0×10-3)中逐滴加入0.10mol/LNaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如图所示,理论上刚好反应点和滴定终点都在b点之前,下列说法不正确的是

| A.V=10mL时,c(OH-)=c(HA)+c(H+) |
| B.b点时,c(Na+)>c(A-)>c(OH-)>c(H+) |
| C.溶液在a点和b点时水的电离程度相同,b点水电离的氢离子都是自由的 |
D.a点时, |
您最近半年使用:0次
名校
3 .  盐酸与
盐酸与 碳酸钠溶液相互滴定,下图为反应过程中
碳酸钠溶液相互滴定,下图为反应过程中 、
、 、
、 微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
 盐酸与
盐酸与 碳酸钠溶液相互滴定,下图为反应过程中
碳酸钠溶液相互滴定,下图为反应过程中 、
、 、
、 微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是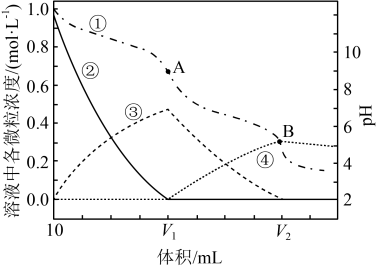
| A.上图是盐酸滴定碳酸钠溶液的曲线变化图 |
B.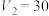 |
C.碳酸的电离平衡常数 数量级是 数量级是 |
D.已知草酸酸性大于碳酸,若用同浓度 溶液代替 溶液代替 溶液,其它实验条件不变,则A点下移 溶液,其它实验条件不变,则A点下移 |
您最近半年使用:0次
名校
4 . 下列反应对应的离子方程式正确的是
A.乙酰胺与盐酸混合共热: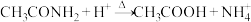 |
B.硫化钠溶液在空气中氧化变质: |
C.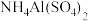 溶液与足量 溶液与足量 溶液反应: 溶液反应: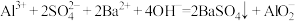 |
D.证明 、 、 、 、 三者的酸性强弱: 三者的酸性强弱: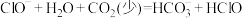 |
您最近半年使用:0次
解题方法
5 . 一定温度下,在冰醋酸中加水稀释时,溶液的导电能力的变化趋势如图所示,下列有关说法中错误的是
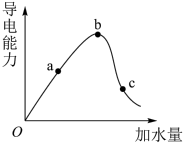
| A.稀释过程中,b点时的电离程度最大 |
| B.加水前,CH3COOH主要以分子形式存在 |
| C.a、b、c三点的pH大小关系:c>a>b |
| D.a、c点的溶液中分别加入足量的锌粉,产生H2的质量相同 |
您最近半年使用:0次
名校
6 . 常温下,向一定浓度邻苯二甲酸钠( 表示)溶液中通入
表示)溶液中通入 气体,保持溶液体积和温度不变,测得
气体,保持溶液体积和温度不变,测得 与
与 [
[ 为
为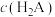 、
、 、
、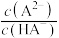 ;
; ]的变化关系如图所示,下列说法错误的是
]的变化关系如图所示,下列说法错误的是
 表示)溶液中通入
表示)溶液中通入 气体,保持溶液体积和温度不变,测得
气体,保持溶液体积和温度不变,测得 与
与 [
[ 为
为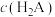 、
、 、
、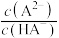 ;
; ]的变化关系如图所示,下列说法错误的是
]的变化关系如图所示,下列说法错误的是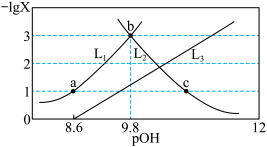
A.曲线 表示 表示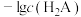 |
B. 点溶液中: 点溶液中: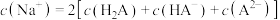 |
C. 的 的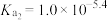 |
D.该溶液中通入和 等物质的量的 等物质的量的 时溶液显碱性 时溶液显碱性 |
您最近半年使用:0次
名校
7 . 水溶液存在离子平衡,回答下列问题:
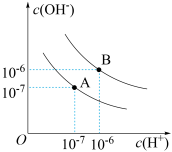
(1)水的电离平衡曲线如图所示。若以A点表示25°C时水在电离平衡时的离子浓度。当温度升到100°C时,水的电离平衡状态到B点,该温度时0.1mol/LNaOH溶液pH为___________ 。___________ (填“正”或“逆”)反应方向移动:水的电离程度将___________ (填“增大”、“减小”或“不变”)。
(3)常温下向20.00mL0.100mol/LHX(一元酸)溶液中滴加0.100mol/LNaOH的pH变化如图所示。___________ 。
②C点溶液中c(X-)___________ c(Na+)(填“>”、“<”或“=”)。
(1)水的电离平衡曲线如图所示。若以A点表示25°C时水在电离平衡时的离子浓度。当温度升到100°C时,水的电离平衡状态到B点,该温度时0.1mol/LNaOH溶液pH为
(3)常温下向20.00mL0.100mol/LHX(一元酸)溶液中滴加0.100mol/LNaOH的pH变化如图所示。

②C点溶液中c(X-)
您最近半年使用:0次
8 . 室温下,取一定量冰醋酸,进行如下实验:
①将冰醋酸配制成 醋酸溶液;
醋酸溶液;
②取 ①所配溶液,加入
①所配溶液,加入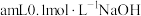 溶液,充分反应后,测得溶液
溶液,充分反应后,测得溶液 ;
;
③向②所得溶液中继续滴加稀盐酸,直至溶液中 。
。
下列说法正确的是
①将冰醋酸配制成
 醋酸溶液;
醋酸溶液;②取
 ①所配溶液,加入
①所配溶液,加入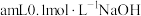 溶液,充分反应后,测得溶液
溶液,充分反应后,测得溶液 ;
;③向②所得溶液中继续滴加稀盐酸,直至溶液中
 。
。下列说法正确的是
A.①中:所得溶液的 |
B.②中: |
C.③中:所得溶液中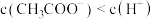 ,且 ,且 |
D.取等体积的①与③所得溶液,二者所含 分子数目相等 分子数目相等 |
您最近半年使用:0次
9 . 常温下,下列有关电解质溶液的说法正确的是
| A.pH=4的H2S溶液与pH=10的NaOH溶液等体积混合,所得混合溶液中:c(H+)<c(OH-) |
B.将CH3COONa溶液从20℃升温至30℃,溶液中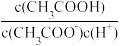 增大 增大 |
C.向0.1mol/LCH3COOH溶液中加入少量纯CH3COOH,溶液 减小 减小 |
| D.向醋酸钠溶液中加入适量醋酸后,混合溶液中离子浓度大小可能为:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
您最近半年使用:0次
10 . 下表是几种弱酸常温下的电离常数:
(1)写出 的电离方程式
的电离方程式___________ 。
(2) 四种酸的酸性由强到弱的顺序为
四种酸的酸性由强到弱的顺序为___________ 。
(3)写出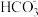 的水解方程式
的水解方程式___________ 。
(4)同浓度的 结合
结合 的能力由强到弱的顺序为
的能力由强到弱的顺序为___________ 。
 |  |  |  |
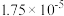 | 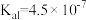 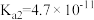 | 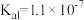 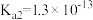 |  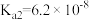 |
(1)写出
 的电离方程式
的电离方程式(2)
 四种酸的酸性由强到弱的顺序为
四种酸的酸性由强到弱的顺序为(3)写出
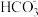 的水解方程式
的水解方程式(4)同浓度的
 结合
结合 的能力由强到弱的顺序为
的能力由强到弱的顺序为
您最近半年使用:0次



