19. 某实验小组探究SO
2与K
2FeO
4的反应,实验如下。
资料:i.K
2FeO
4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O
2,在碱性溶液中较稳定。
ii.Fe
3+可以与C
2O

形成[Fe(C
2O
4)
3]
3-;
| 装置 | 操作及现象 |
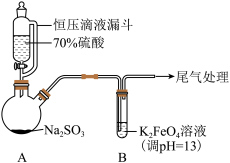
| 实验一:向B中通入SO2,产生暗红褐色沉淀X和溶液Y(略显红色);继续通入SO2一段时间后,溶液呈红色,继而变为橙色,最终沉淀消失,溶液几乎无色。 |
(1)A中产生SO
2的化学方程式为
___________。
(2)暗红褐色沉淀X可能含Fe
3+、OH
-、SO

、SO

,检验如下:
实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在
___________。另取少量溶液滴加BaCl
2溶液,产生白色沉淀,但不能确认含有SO

,原因是
___________。
实验三:向X中加入H
2C
2O
4溶液,沉淀溶解。继续滴加BaCl
2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO

。
实验三中用H
2C
2O
4溶液溶解沉淀的目的是:
___________。
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:
___________。
(3)查阅资料:a.Fe
3+、SO

、H
2O(或OH
﹣)会形成配合物HOFeOSO
2。
b. SO

和O
2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO

①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L
-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是
___________。
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:
___________。
总结:SO
2与K
2FeO
4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。