1 . 某温度下,PbCO3饱和溶液和PbI2饱和溶液中的阴、阳离子浓度满足如图所示的关系。
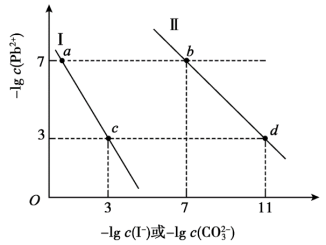
| A.曲线Ⅰ表示PbCO3的溶解平衡 |
| B.该温度下Ksp(PbI2):Ksp(PbCO3)=108 |
| C.曲线Ⅱ上的b点可通过改变温度移动至d点 |
| D.向PbI2的悬浊液中加入Na2CO3浓溶液,可以将其转化成PbCO3 |
您最近半年使用:0次
2 . T℃时, 和
和 的沉淀溶解平衡曲线如图所示,已知
的沉淀溶解平衡曲线如图所示,已知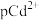 为
为 浓度的负对数,pN为阴离子浓度的负对数,下列说法正确的是
浓度的负对数,pN为阴离子浓度的负对数,下列说法正确的是
 和
和 的沉淀溶解平衡曲线如图所示,已知
的沉淀溶解平衡曲线如图所示,已知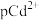 为
为 浓度的负对数,pN为阴离子浓度的负对数,下列说法正确的是
浓度的负对数,pN为阴离子浓度的负对数,下列说法正确的是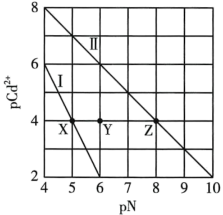
A.X点: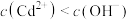 ,Z点: ,Z点: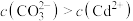 |
B.溶度积的负对数: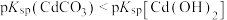 |
C.Y点对应的 溶液为不饱和溶液,可以继续溶解 溶液为不饱和溶液,可以继续溶解 |
D.T℃时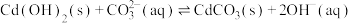 的平衡常数K为 的平衡常数K为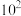 |
您最近半年使用:0次
3 . 室温下,向Mg(NO3)2溶液、HF溶液、CH3CH2COOH溶液中分别滴加NaOH溶液,测得溶液中pH与pX[pX=-lgX,X代表 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是
已知:
 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是已知:

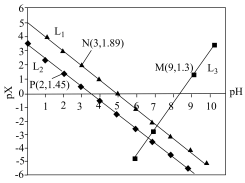
A. 代表的是pH与 代表的是pH与 的关系 的关系 |
B. 的 的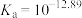 |
C.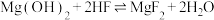 的 的 |
| D.含相同浓度NaF、HF的混合溶液的pH>7 |
您最近半年使用:0次
4 . 已知:常温下Ksp(CuS)<Ksp(PbS)。25℃时,饱和溶液中–lgc(S2-)与-lgc(X)的关系如图所示,其中,X代表Cu2+、Pb2+。下列叙述错误的是
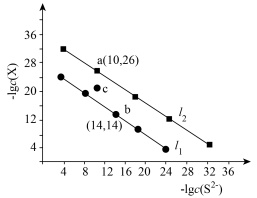
| A.l1直线代表–lgc(S2-)与-lgc(Pb2+)的关系 |
| B.该温度下Ksp(CuS)=1.0×10-36 |
| C.加热,可使溶液由c点变到a点 |
D.PbS(s)+Cu2+(aq) CuS(s)+Pb2+(aq)的平衡常数K=108 CuS(s)+Pb2+(aq)的平衡常数K=108 |
您最近半年使用:0次
5 . 难溶盐  可溶于盐酸。常温下,用
可溶于盐酸。常温下,用  调节
调节  浊液的
浊液的  ,测得体系中−lgc(F−)或−lgc(Ca2+)与
,测得体系中−lgc(F−)或−lgc(Ca2+)与 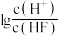 的关系如图所示,下列说法
的关系如图所示,下列说法错误 的是
 可溶于盐酸。常温下,用
可溶于盐酸。常温下,用  调节
调节  浊液的
浊液的  ,测得体系中−lgc(F−)或−lgc(Ca2+)与
,测得体系中−lgc(F−)或−lgc(Ca2+)与 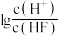 的关系如图所示,下列说法
的关系如图所示,下列说法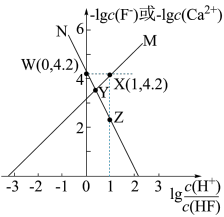
A.随着盐酸的加入, 不断溶解 不断溶解 |
B. 代表−lgc(F−)与 代表−lgc(F−)与 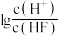 的变化曲线 的变化曲线 |
C.难溶盐  的溶度积常数Ksp(CaF2)=1.0×10−7.4 的溶度积常数Ksp(CaF2)=1.0×10−7.4 |
D. 点溶液中存在lgc(Ca2+)—2 点溶液中存在lgc(Ca2+)—2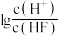 =—4.2 =—4.2 |
您最近半年使用:0次
6 . 室温下向含 和
和 的溶液中滴加
的溶液中滴加 溶液,混合液中
溶液,混合液中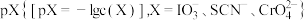 和
和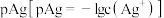 的关系如图所示,已知:
的关系如图所示,已知: ,下列叙述错误的是
,下列叙述错误的是
 和
和 的溶液中滴加
的溶液中滴加 溶液,混合液中
溶液,混合液中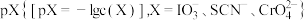 和
和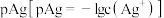 的关系如图所示,已知:
的关系如图所示,已知: ,下列叙述错误的是
,下列叙述错误的是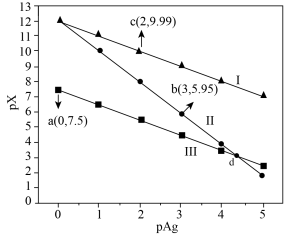
A.直线Ⅱ代表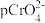 和 和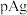 的关系 的关系 |
B.d点直线Ⅱ和直线Ⅲ对应的两种沉淀的 相同 相同 |
C.向等浓度的 和 和 混合溶液中逐滴滴加 混合溶液中逐滴滴加 溶液,先生成 溶液,先生成 沉淀 沉淀 |
D. 得平衡常数 得平衡常数 为 为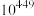 |
您最近半年使用:0次
7 . 室温下,某 溶液体系中满足
溶液体系中满足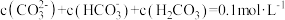 ,现利用平衡移动原理,研究
,现利用平衡移动原理,研究 在不同pH的
在不同pH的 体系中的可能产物。图1中曲线表示
体系中的可能产物。图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合
体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合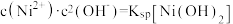 ,曲线Ⅱ的离子浓度关系符合
,曲线Ⅱ的离子浓度关系符合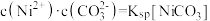 ,不同pH下
,不同pH下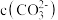 由图1得到。下列说法错误的是
由图1得到。下列说法错误的是
 溶液体系中满足
溶液体系中满足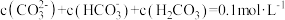 ,现利用平衡移动原理,研究
,现利用平衡移动原理,研究 在不同pH的
在不同pH的 体系中的可能产物。图1中曲线表示
体系中的可能产物。图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合
体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合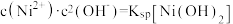 ,曲线Ⅱ的离子浓度关系符合
,曲线Ⅱ的离子浓度关系符合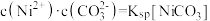 ,不同pH下
,不同pH下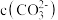 由图1得到。下列说法错误的是
由图1得到。下列说法错误的是
A.由图1, 的水解平衡常数的数量级是 的水解平衡常数的数量级是 |
B.图2中M点,溶液中存在 |
C.图2中P点,存在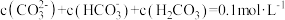 |
D.沉淀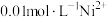 制备 制备 时,选用 时,选用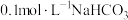 溶液比 溶液比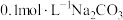 溶液效果好 溶液效果好 |
您最近半年使用:0次
8 . 已知: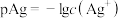 ,常温下向
,常温下向 溶液中滴加
溶液中滴加 溶液的滴定曲线Ⅰ如图所示。已知:
溶液的滴定曲线Ⅰ如图所示。已知: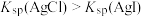 。下列说法正确的是
。下列说法正确的是
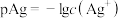 ,常温下向
,常温下向 溶液中滴加
溶液中滴加 溶液的滴定曲线Ⅰ如图所示。已知:
溶液的滴定曲线Ⅰ如图所示。已知: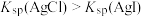 。下列说法正确的是
。下列说法正确的是
A.常温下, |
B.溶液中水的电离程度: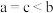 |
C.c点溶液中 |
| D.将NaCl溶液换为等浓度的NaI溶液,图像变为曲线Ⅱ |
您最近半年使用:0次
7日内更新
|
253次组卷
|
5卷引用:贵州省贵阳市2024届高三下学期适应性测试(一)化学试题
贵州省贵阳市2024届高三下学期适应性测试(一)化学试题贵州省贵阳市2024届高三下学期适应性测试(一)化学试题宁夏石嘴山市光明中学2024届高三第一次模拟考试理综化学试题(已下线)通关练10 盘点溶液中的“四大”平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)
9 . 某同学分别向0.1 mol/L、5 mol/L NaCl溶液中滴加2滴0.1 mol/L AgNO3溶液,均有白色沉淀,振荡后,前者沉淀不消失、后者沉淀消失。查阅水溶液中银氯配合物的分布曲线(以银的百分含量计),如下图所示,下列说法不正确 的是
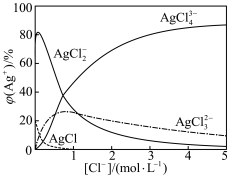
| A.AgCl在不同浓度的NaCl溶液中溶解度不同 |
| B.银氯配合物中Ag+是中心离子,Cl−是配体 |
C.上述实验中,白色沉淀消失的离子方程式是Ag++ 4Cl−=AgCl |
| D.推测浓盐酸中滴加2滴0.1 mol/L AgNO3溶液,产生白色沉淀,振荡后沉淀消失 |
您最近半年使用:0次
10 . 25℃时,用NaOH溶液分别滴定HX、 、
、 三种溶液,
三种溶液, [M表示
[M表示 、
、 、
、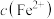 ]随pH变化关系如图所示,其中③的M代表
]随pH变化关系如图所示,其中③的M代表 。已知
。已知 ,下列有关分析不正确的是
,下列有关分析不正确的是
 、
、 三种溶液,
三种溶液, [M表示
[M表示 、
、 、
、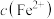 ]随pH变化关系如图所示,其中③的M代表
]随pH变化关系如图所示,其中③的M代表 。已知
。已知 ,下列有关分析不正确的是
,下列有关分析不正确的是
A.①代表滴定 溶液的变化关系 溶液的变化关系 |
B.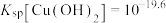 |
C.a点时,③中 与②中M的关系为 与②中M的关系为 |
D. 、 、 固体均易溶解于HX溶液 固体均易溶解于HX溶液 |
您最近半年使用:0次



