1 . 某温度下,PbCO3饱和溶液和PbI2饱和溶液中的阴、阳离子浓度满足如图所示的关系。
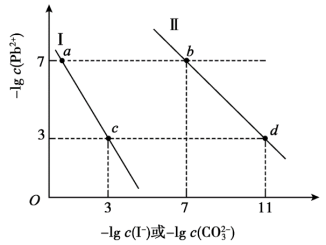
| A.曲线Ⅰ表示PbCO3的溶解平衡 |
| B.该温度下Ksp(PbI2):Ksp(PbCO3)=108 |
| C.曲线Ⅱ上的b点可通过改变温度移动至d点 |
| D.向PbI2的悬浊液中加入Na2CO3浓溶液,可以将其转化成PbCO3 |
您最近半年使用:0次
名校
解题方法
2 . 室温下,用饱和Na2CO3溶液浸泡BaSO4粉末,一段时间后过滤,向滤渣中加入过量盐酸产生气泡,滤渣未完全溶解,已知:室温下 ,
,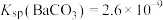 ,下列说法
,下列说法错误 的是
 ,
,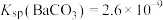 ,下列说法
,下列说法A.反应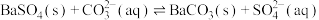 正向进行,需满足 正向进行,需满足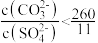 |
| B.室温下,BaSO4的溶解度小于BaCO3的溶解度 |
C.滤渣中加入盐酸反应的离子方程式: |
D.过滤后所得清液中存在: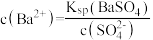 ,且 ,且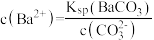 |
您最近半年使用:0次
3 . T℃时, 和
和 的沉淀溶解平衡曲线如图所示,已知
的沉淀溶解平衡曲线如图所示,已知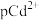 为
为 浓度的负对数,pN为阴离子浓度的负对数,下列说法正确的是
浓度的负对数,pN为阴离子浓度的负对数,下列说法正确的是
 和
和 的沉淀溶解平衡曲线如图所示,已知
的沉淀溶解平衡曲线如图所示,已知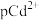 为
为 浓度的负对数,pN为阴离子浓度的负对数,下列说法正确的是
浓度的负对数,pN为阴离子浓度的负对数,下列说法正确的是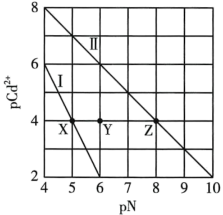
A.X点: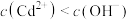 ,Z点: ,Z点: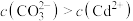 |
B.溶度积的负对数: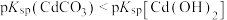 |
C.Y点对应的 溶液为不饱和溶液,可以继续溶解 溶液为不饱和溶液,可以继续溶解 |
D.T℃时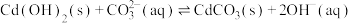 的平衡常数K为 的平衡常数K为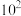 |
您最近半年使用:0次
解题方法
4 . 现有常温下浓度均为 的下列五种溶液:
的下列五种溶液:
① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液
(1)这5种溶液pH由大到小的顺序是__________ (填序号)。
(2)②中各离子浓度由大到小的顺序是__________ 。
(3)向③中通入少量氨气,此时 的值
的值__________ (填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积__________ ④的体积(填“大于”“小于”或“等于”)。
(5)常温下,向 溶液中加入
溶液中加入 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为__________ ,若将所得悬浊液的pH值调整为4,则溶液中 的浓度为
的浓度为__________  (已知常温下
(已知常温下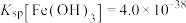 。
。
 的下列五种溶液:
的下列五种溶液:①
 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液(1)这5种溶液pH由大到小的顺序是
(2)②中各离子浓度由大到小的顺序是
(3)向③中通入少量氨气,此时
 的值
的值(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积
(5)常温下,向
 溶液中加入
溶液中加入 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为 的浓度为
的浓度为 (已知常温下
(已知常温下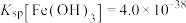 。
。
您最近半年使用:0次
5 . 已知:常温下Ksp(CuS)<Ksp(PbS)。25℃时,饱和溶液中–lgc(S2-)与-lgc(X)的关系如图所示,其中,X代表Cu2+、Pb2+。下列叙述错误的是
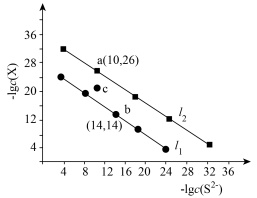
| A.l1直线代表–lgc(S2-)与-lgc(Pb2+)的关系 |
| B.该温度下Ksp(CuS)=1.0×10-36 |
| C.加热,可使溶液由c点变到a点 |
D.PbS(s)+Cu2+(aq) CuS(s)+Pb2+(aq)的平衡常数K=108 CuS(s)+Pb2+(aq)的平衡常数K=108 |
您最近半年使用:0次
6 . 钯催化剂(主要成分为Pd、α-Al2O3,还含少量铁、铜等)是石油化工中催化加氢和催化氧化等反应的重要催化剂。一种从废钯催化剂中回收海绵钯的工艺流程如下:
②常温下,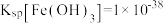 ,
, 。
。
回答下列问题:
(1)“还原Ⅰ”过程中加入甲酸的主要目的是还原___________ (填化学式)。
(2)“酸浸”过程中Pd转化的离子方程式为___________ 。
(3)“酸浸”过程中温度、固液比对浸取率的影响如图,则“酸浸”最佳条件为___________ 。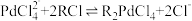 ,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是
,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是___________ 。
(5)“沉钯”过程钯元素主要发生如下转化:H2PdCl4 (稀溶液) [Pd(NH3)4]Cl4 (稀溶液)
[Pd(NH3)4]Cl4 (稀溶液) [Pd(NH3)4]Cl2(沉淀)。则滤液中溶质的主要成分为
[Pd(NH3)4]Cl2(沉淀)。则滤液中溶质的主要成分为___________ (填化学式)。
(6)N2H4的电子式为___________ 。
(7)“还原Ⅱ”过程中产生无毒无害气体。由[Pd(NH3)4]Cl2生成海绵钯的化学方程式为___________ 。

②常温下,
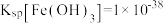 ,
, 。
。回答下列问题:
(1)“还原Ⅰ”过程中加入甲酸的主要目的是还原
(2)“酸浸”过程中Pd转化的离子方程式为
(3)“酸浸”过程中温度、固液比对浸取率的影响如图,则“酸浸”最佳条件为

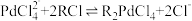 ,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是
,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是(5)“沉钯”过程钯元素主要发生如下转化:H2PdCl4 (稀溶液)
 [Pd(NH3)4]Cl4 (稀溶液)
[Pd(NH3)4]Cl4 (稀溶液) [Pd(NH3)4]Cl2(沉淀)。则滤液中溶质的主要成分为
[Pd(NH3)4]Cl2(沉淀)。则滤液中溶质的主要成分为(6)N2H4的电子式为
(7)“还原Ⅱ”过程中产生无毒无害气体。由[Pd(NH3)4]Cl2生成海绵钯的化学方程式为
您最近半年使用:0次
7 . 按要求回答下列问题。
(1)铁盐可用作净水剂,用离子方程式表示其原理:___________ 。配制 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的___________ 中,然后再加水稀释到所需的浓度。将 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是___________ (填化学式)。
(2)某 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的___________ ,充分反应后过滤,即可除去 。
。
(3)在 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成?___________ (填“是”或“否”)。向溶液中加入 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为___________ 。(已知 时
时 、
、 、
、 的
的 分别为
分别为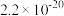 、
、 、
、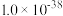 )
)
(1)铁盐可用作净水剂,用离子方程式表示其原理:
 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是(2)某
 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的 。
。(3)在
 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成? 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为 时
时 、
、 、
、 的
的 分别为
分别为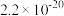 、
、 、
、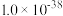 )
)
您最近半年使用:0次
8 . 化工生产中常用MnS作为沉淀剂除去工业废水中的Cu2+: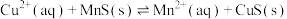 ,下列说法正确的是
,下列说法正确的是
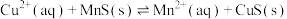 ,下列说法正确的是
,下列说法正确的是A.相同温度时,MnS的 比CuS的 比CuS的 小 小 |
B.该反应达到平衡时 |
C.设该反应的平衡常数为K,则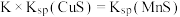 |
D.向平衡体系中加入少量 固体后, 固体后, 减小, 减小, 增大 增大 |
您最近半年使用:0次
9 . 已知: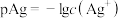 ,常温下向
,常温下向 溶液中滴加
溶液中滴加 溶液的滴定曲线Ⅰ如图所示。已知:
溶液的滴定曲线Ⅰ如图所示。已知: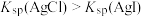 。下列说法正确的是
。下列说法正确的是
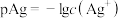 ,常温下向
,常温下向 溶液中滴加
溶液中滴加 溶液的滴定曲线Ⅰ如图所示。已知:
溶液的滴定曲线Ⅰ如图所示。已知: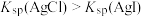 。下列说法正确的是
。下列说法正确的是
A.常温下, |
B.溶液中水的电离程度: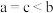 |
C.c点溶液中 |
| D.将NaCl溶液换为等浓度的NaI溶液,图像变为曲线Ⅱ |
您最近半年使用:0次
7日内更新
|
226次组卷
|
5卷引用:贵州省贵阳市2024届高三下学期适应性测试(一)化学试题
贵州省贵阳市2024届高三下学期适应性测试(一)化学试题贵州省贵阳市2024届高三下学期适应性测试(一)化学试题宁夏石嘴山市光明中学2024届高三第一次模拟考试理综化学试题(已下线)通关练10 盘点溶液中的“四大”平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)
名校
10 . 向0.1mol∙L-1FeSO4溶液中持续通入H2S至饱和,有微量黑色的FeS沉淀生成,该溶液中[H2S]=0.1mol∙L-1。(忽略FeSO4浓度的变化和溶液体积的变化)。已知常温下,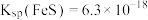 ,H2S的电离常数分别为:
,H2S的电离常数分别为: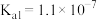 、
、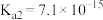 。
。
(1)写出生成黑色沉淀的离子方程式___________ 。
(2)溶液中[S2-]=___________ mol∙L-1;溶液中[H+]=___________ mol∙L-1。
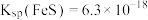 ,H2S的电离常数分别为:
,H2S的电离常数分别为: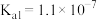 、
、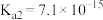 。
。(1)写出生成黑色沉淀的离子方程式
(2)溶液中[S2-]=
您最近半年使用:0次



