名校
解题方法
1 . 常温下,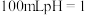 的
的 ,要使溶液的
,要使溶液的
①需要加入水___________  。
。
②需要加入 的盐酸
的盐酸___________  。需要加入
。需要加入 的
的
___________  。
。
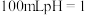 的
的 ,要使溶液的
,要使溶液的
①需要加入水
 。
。②需要加入
 的盐酸
的盐酸 。需要加入
。需要加入 的
的
 。
。
您最近半年使用:0次
2 . 常温下,分别取未知浓度的 和
和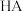 溶液,加水稀释至原体积的
溶液,加水稀释至原体积的 倍,稀释过程中,两溶液
倍,稀释过程中,两溶液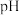 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是

 和
和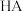 溶液,加水稀释至原体积的
溶液,加水稀释至原体积的 倍,稀释过程中,两溶液
倍,稀释过程中,两溶液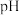 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
A. 为弱碱, 为弱碱,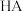 为强酸 为强酸 |
| B.将X点溶液与Z点溶液等体积混合,所得溶液呈碱性 |
C.若升高温度,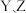 点对应溶液的 点对应溶液的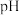 均不变 均不变 |
D.水的电离程度: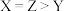 |
您最近半年使用:0次
3 . 常温下,下列关于 的
的 溶液说法正确的是
溶液说法正确的是
 的
的 溶液说法正确的是
溶液说法正确的是A.将 的 的 溶液稀释10倍,溶液的 溶液稀释10倍,溶液的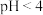 |
B.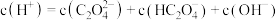 |
C.与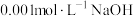 溶液等体积混合后,溶液呈碱性 溶液等体积混合后,溶液呈碱性 |
D.加水稀释时,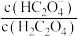 逐渐减小 逐渐减小 |
您最近半年使用:0次
名校
解题方法
4 . 已知水在100℃时,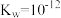 。
。
(1)在100℃,某溶液中由水电离产生的 mol/L,则该溶液的
mol/L,则该溶液的
___________ 。
(2)100℃时,若100体积 的某强酸溶液与1体积
的某强酸溶液与1体积 的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是___________ 。
(3)100℃时,将 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为___________ 。
(4)常温下,将 的
的 溶液与等物质的量浓度的
溶液与等物质的量浓度的 溶液等体积混合,所得混合液的
溶液等体积混合,所得混合液的
___________ 。
(5)已知HA的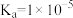 ,常温下,取
,常温下,取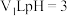 的
的 溶液与
溶液与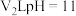 的
的 溶液混合,若混合后溶液
溶液混合,若混合后溶液 ,则大小关系:V1
,则大小关系:V1___________ V2(填“大于”“小于”或“等于”)。
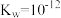 。
。(1)在100℃,某溶液中由水电离产生的
 mol/L,则该溶液的
mol/L,则该溶液的
(2)100℃时,若100体积
 的某强酸溶液与1体积
的某强酸溶液与1体积 的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是(3)100℃时,将
 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为(4)常温下,将
 的
的 溶液与等物质的量浓度的
溶液与等物质的量浓度的 溶液等体积混合,所得混合液的
溶液等体积混合,所得混合液的
(5)已知HA的
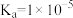 ,常温下,取
,常温下,取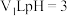 的
的 溶液与
溶液与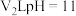 的
的 溶液混合,若混合后溶液
溶液混合,若混合后溶液 ,则大小关系:V1
,则大小关系:V1
您最近半年使用:0次
5 . 下列说法中正确的是
| A.在100℃时,pH约为6的纯水呈酸性 |
B.将1mL 盐酸稀释至1000mL,所得溶液的pH为9 盐酸稀释至1000mL,所得溶液的pH为9 |
C.在常温下,当水电离出的 为 为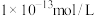 时,此溶液的pH可能为1或13 时,此溶液的pH可能为1或13 |
| D.将pH=2的盐酸和醋酸各1mL分别稀释至100mL,所得醋酸的pH略大 |
您最近半年使用:0次
名校
解题方法
6 . 向碘水、淀粉的混合液中加入 溶液,蓝色褪去。为探究褪色原因,实验如图:
溶液,蓝色褪去。为探究褪色原因,实验如图:不正确 的是
 溶液,蓝色褪去。为探究褪色原因,实验如图:
溶液,蓝色褪去。为探究褪色原因,实验如图:
A.过程①中蓝色褪去的原因可能是 氧化了 氧化了 | B.过程①后溶液 可能明显变小 可能明显变小 |
C.过程③中加入 溶液的目的是除去 溶液的目的是除去 | D.过程④说明过程①生成含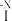 的粒子 的粒子 |
您最近半年使用:0次
名校
解题方法
7 . 有4种混合溶液,分别由等体积 的两种溶液混合而成:
的两种溶液混合而成:
① 与
与 (混合溶液呈中性)
(混合溶液呈中性)
② 与HCl
与HCl
③ 与NaCl
与NaCl
④ 与
与 (混合溶液呈碱性)
(混合溶液呈碱性)
下列各项排序正确的是
 的两种溶液混合而成:
的两种溶液混合而成:①
 与
与 (混合溶液呈中性)
(混合溶液呈中性)②
 与HCl
与HCl③
 与NaCl
与NaCl④
 与
与 (混合溶液呈碱性)
(混合溶液呈碱性)下列各项排序正确的是
| A.pH:②<①<③<④ |
B.溶液中 :①<③<②<④ :①<③<②<④ |
C. :①<③<②<④ :①<③<②<④ |
D. :①<③<④<② :①<③<④<② |
您最近半年使用:0次
名校
解题方法
8 . 常温下,下列关于电解质溶液的说法正确的是
| A.pH=12的氨水和氢氧化钠溶液按体积比1∶9混合后,pH值增大 |
B.等体积、等浓度的Na2CO3和NaHCO3溶液混合后,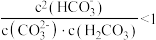 |
C.0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合后存在: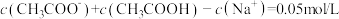 |
D.等浓度的氨水和硫酸按体积比3∶1混合后溶液显碱性,则混合溶液中存在: |
您最近半年使用:0次
解题方法
9 . 下列溶液一定呈中性的是
A. mol⋅L mol⋅L 的溶液 的溶液 |
B. 的溶液 的溶液 |
| C.使石蕊试液呈紫色的溶液 |
| D.酸与碱恰好完全反应生成正盐的溶液 |
您最近半年使用:0次
10 . 下列有关水的离子积常数 或
或 变化的判断,正确的是
变化的判断,正确的是
 或
或 变化的判断,正确的是
变化的判断,正确的是| A.随着温度的升高,水的离子积常数减小 |
B.完全中和 的 的 溶液 溶液 ,需要 ,需要 的 的 溶液 溶液 |
| C.由非电解质溶于水得到的溶液一定呈中性 |
D.氢氧化钠溶液久置于空气中, 减小 减小 |
您最近半年使用:0次



