解题方法
1 . 水溶液广泛存在于生命体及其赖以生存的环境中,电解质在水溶液中发生的离子反应以及电离平衡等,都与生命活动、日常生活、工农业生产和环境保护等息息相关。回答下列问题:
①图中黑球代表___________ 。(填微粒符号)
②写出Y电极的电极反应式:___________ 。
(2)A、B、C、D四种物质分别是NaOH、 、
、 、HCl中的一种。
、HCl中的一种。
① 的A溶液
的A溶液 ,则A是
,则A是___________ 。
②B溶液和D溶液显碱性,等浓度时两者的pH关系: ,则D溶液是
,则D溶液是___________ 。
(3)用水稀释 的氨水时,溶液中随着水量的增加而减小的是
的氨水时,溶液中随着水量的增加而减小的是___________ 。(填字母,下同)。
a. b.
b. c.
c. 与
与 的乘积 d.
的乘积 d. 的物质的量
的物质的量
(4)pH相同、等体积的盐酸和醋酸两份溶液,则下列说法正确的是___________ 。
a.
b.分别与过量的锌粉反应,醋酸产生的气体比较多
c.稀释相同倍数时,醋酸的pH比较小
d.恰好中和时消耗NaOH的物质的量相同
(5)碳酸钠的水溶液呈___________ 性,用离子方程式表示:___________ 。
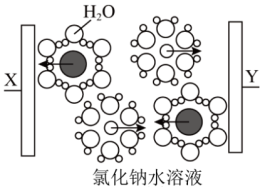
①图中黑球代表
②写出Y电极的电极反应式:
(2)A、B、C、D四种物质分别是NaOH、
 、
、 、HCl中的一种。
、HCl中的一种。①
 的A溶液
的A溶液 ,则A是
,则A是②B溶液和D溶液显碱性,等浓度时两者的pH关系:
 ,则D溶液是
,则D溶液是(3)用水稀释
 的氨水时,溶液中随着水量的增加而减小的是
的氨水时,溶液中随着水量的增加而减小的是a.
 b.
b. c.
c. 与
与 的乘积 d.
的乘积 d. 的物质的量
的物质的量(4)pH相同、等体积的盐酸和醋酸两份溶液,则下列说法正确的是
a.

b.分别与过量的锌粉反应,醋酸产生的气体比较多
c.稀释相同倍数时,醋酸的pH比较小
d.恰好中和时消耗NaOH的物质的量相同
(5)碳酸钠的水溶液呈
您最近半年使用:0次
2 . 请回答下列问题:
(1)现有常温下 的盐酸(甲)和
的盐酸(甲)和  的醋酸溶液(乙),请根据下列操作回答:
的醋酸溶液(乙),请根据下列操作回答:
①常温下 溶液加水稀释过程,下列表达式的数值一定变小的是
溶液加水稀释过程,下列表达式的数值一定变小的是___________ (填字母)。
A.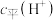 B.
B.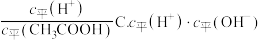 D.
D.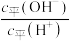
②取 的乙溶液,加入等体积的水,醋酸的电离平衡
的乙溶液,加入等体积的水,醋酸的电离平衡___________ (填“向左”“向右”或“不”)移动;另取10 的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中
的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中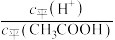 的值将
的值将___________ (填“增大”“减小”或“无法确定”)。
③相同条件下,取等体积的甲、乙两溶液,分别加水稀释100倍,所得溶液的 大小关系为
大小关系为  (甲)
(甲)___________  (乙)(填>、<”或“=”)。
(乙)(填>、<”或“=”)。
(2)联氨(又称肼, ,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,联氨是二元弱碱,在水中的电离方程式与氨相似,其一级电离方程式为
,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,联氨是二元弱碱,在水中的电离方程式与氨相似,其一级电离方程式为___________ ,其一级电离常数 
___________ 。
(已知: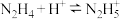 的
的 )
)
(3)已知 的
的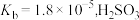 的
的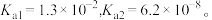 若氨水的浓度为
若氨水的浓度为 ,溶液中的c平(OH-)=
,溶液中的c平(OH-)=___________ mol/L。将  通入该氨水中,当
通入该氨水中,当  降至
降至  时,溶液中的
时,溶液中的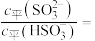
___________ 。
(1)现有常温下
 的盐酸(甲)和
的盐酸(甲)和  的醋酸溶液(乙),请根据下列操作回答:
的醋酸溶液(乙),请根据下列操作回答:①常温下
 溶液加水稀释过程,下列表达式的数值一定变小的是
溶液加水稀释过程,下列表达式的数值一定变小的是A.
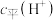 B.
B.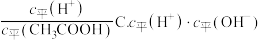 D.
D.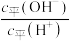
②取
 的乙溶液,加入等体积的水,醋酸的电离平衡
的乙溶液,加入等体积的水,醋酸的电离平衡 的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中
的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中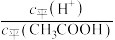 的值将
的值将③相同条件下,取等体积的甲、乙两溶液,分别加水稀释100倍,所得溶液的
 大小关系为
大小关系为  (甲)
(甲) (乙)(填>、<”或“=”)。
(乙)(填>、<”或“=”)。(2)联氨(又称肼,
 ,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,联氨是二元弱碱,在水中的电离方程式与氨相似,其一级电离方程式为
,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,联氨是二元弱碱,在水中的电离方程式与氨相似,其一级电离方程式为
(已知:
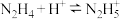 的
的 )
)(3)已知
 的
的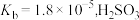 的
的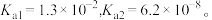 若氨水的浓度为
若氨水的浓度为 ,溶液中的c平(OH-)=
,溶液中的c平(OH-)= 通入该氨水中,当
通入该氨水中,当  降至
降至  时,溶液中的
时,溶液中的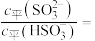
您最近半年使用:0次
3 . 常温下,分别取未知浓度的 和
和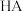 溶液,加水稀释至原体积的
溶液,加水稀释至原体积的 倍,稀释过程中,两溶液
倍,稀释过程中,两溶液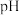 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是

 和
和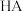 溶液,加水稀释至原体积的
溶液,加水稀释至原体积的 倍,稀释过程中,两溶液
倍,稀释过程中,两溶液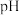 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
A. 为弱碱, 为弱碱,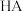 为强酸 为强酸 |
| B.将X点溶液与Z点溶液等体积混合,所得溶液呈碱性 |
C.若升高温度,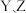 点对应溶液的 点对应溶液的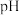 均不变 均不变 |
D.水的电离程度: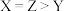 |
您最近半年使用:0次
4 . 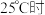 ,相同
,相同  的两种一元弱酸
的两种一元弱酸 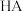 与
与  溶液分别加水稀释,溶液
溶液分别加水稀释,溶液 随溶液体积变化的曲线如图所示。下列说法正确的是
随溶液体积变化的曲线如图所示。下列说法正确的是
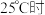 ,相同
,相同  的两种一元弱酸
的两种一元弱酸 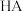 与
与  溶液分别加水稀释,溶液
溶液分别加水稀释,溶液 随溶液体积变化的曲线如图所示。下列说法正确的是
随溶液体积变化的曲线如图所示。下列说法正确的是
A.同浓度的 与 与  溶液中, 溶液中,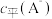 大于 大于 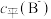 |
B.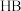 的酸性强于 的酸性强于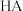 |
C. 点溶液的导电性大于 点溶液的导电性大于 点溶液 点溶液 |
D. 点的 点的 大于 大于 点的 点的  |
您最近半年使用:0次
5 . 下列事实能说明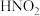 是弱电解质的有几种
是弱电解质的有几种
①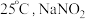 溶液的
溶液的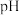 大于7 ②用
大于7 ②用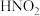 溶液做导电性实验,灯泡很暗 ③
溶液做导电性实验,灯泡很暗 ③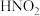 溶液不与
溶液不与 溶液反应 ④
溶液反应 ④ 时,
时,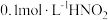 溶液的
溶液的 
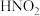 是弱电解质的有几种
是弱电解质的有几种①
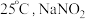 溶液的
溶液的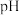 大于7 ②用
大于7 ②用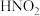 溶液做导电性实验,灯泡很暗 ③
溶液做导电性实验,灯泡很暗 ③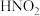 溶液不与
溶液不与 溶液反应 ④
溶液反应 ④ 时,
时,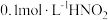 溶液的
溶液的 
| A.1 | B.2 | C.3 | D.4 |
您最近半年使用:0次
6 . 某温度下,将 和体积均相同的
和体积均相同的 和
和 溶液分别加水稀释,其
溶液分别加水稀释,其 随加水体积的变化如图所示。下列叙述正确的是
随加水体积的变化如图所示。下列叙述正确的是
 和体积均相同的
和体积均相同的 和
和 溶液分别加水稀释,其
溶液分别加水稀释,其 随加水体积的变化如图所示。下列叙述正确的是
随加水体积的变化如图所示。下列叙述正确的是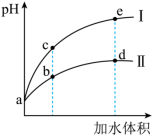
A.稀释前溶液的浓度: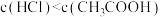 |
| B.曲线Ⅱ表示的是HCl稀释的过程 |
C.从b点到d点,溶液中 逐渐增大 逐渐增大 |
| D.溶液中水的电离程度:b点 > c点 |
您最近半年使用:0次
解题方法
7 . Ⅰ.25°C时,有关物质的电离平衡常数如下:
回答下列问题。
(1)常温下,醋酸钠的溶液呈___________ 性(填“酸”“中”或“碱”),原因是___________ (写离子方程式)。
(2)物质的量浓度为 的下列四种溶液,pH由大到小的顺序是___________(填编号)。
的下列四种溶液,pH由大到小的顺序是___________(填编号)。
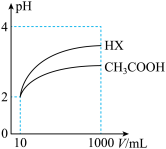
(3)体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。则HX的电离平衡常数___________ (填“大于”、“等于”或“小于”)醋酸的电离平衡常数:HX是___________ 酸(填“强”或“弱”),理由是___________ 。 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到
溶液进行电解,可循环再生NaOH,同时得到 ,原理如图所示(电极材料为石墨)。
,原理如图所示(电极材料为石墨)。___________ (填“正”或“负”)极,C口流出的物质是___________ 。
(5) 放电的电极反应式为
放电的电极反应式为___________ 。
| 化学式 |  |  |  |
| 电离平衡常数 | 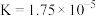 |   | 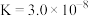 |
(1)常温下,醋酸钠的溶液呈
(2)物质的量浓度为
 的下列四种溶液,pH由大到小的顺序是___________(填编号)。
的下列四种溶液,pH由大到小的顺序是___________(填编号)。A. | B. | C. | D. |
(3)体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。则HX的电离平衡常数
 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到
溶液进行电解,可循环再生NaOH,同时得到 ,原理如图所示(电极材料为石墨)。
,原理如图所示(电极材料为石墨)。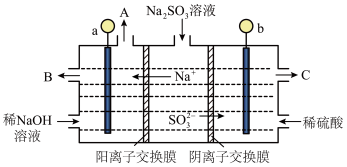
(5)
 放电的电极反应式为
放电的电极反应式为
您最近半年使用:0次
名校
8 . 下列实验能达到目的的是
| A.测定中和反应的反应热:用酸碱中和滴定法 |
| B.判断醋酸为弱电解质:测定并比较醋酸和盐酸的pH |
| C.用98%浓硫酸配制10%的稀硫酸:仪器为烧杯、玻璃棒 |
| D.测定镀锌铁皮的镀层厚度:将镀锌铁皮放入稀硫酸中,待产生氢气的速率突然减小,可以判断锌镀层已反应完全 |
您最近半年使用:0次
9 . 某温度下,等体积、相同 的盐酸和醋酸溶液分别加水稀释,溶液中的
的盐酸和醋酸溶液分别加水稀释,溶液中的 随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
 的盐酸和醋酸溶液分别加水稀释,溶液中的
的盐酸和醋酸溶液分别加水稀释,溶液中的 随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
| A.Ⅱ表示的是盐酸的变化曲线 |
B.b点溶液中水电离的 小于c点溶液 小于c点溶液 |
C.取等体积的a点、b点对应的溶液,消耗的 的量相同 的量相同 |
| D.b点酸的总浓度大于a点酸的总浓度 |
您最近半年使用:0次
名校
10 . 化学中常用pH表示水溶液的酸碱度,其定义为pH =-lg(H+)。下列有关叙述不正确的是
| A.向体积相同,pH均为3的盐酸和醋酸溶液中加入NaOH溶液至恰好中和,醋酸消耗NaOH的量更多 |
| B.向体积相同,pH均为3的的盐酸和醋酸溶液中分别加水稀释至pH=5,盐酸加水体积更多 |
| C.常温下,pH均为5的的醋酸溶液和NH4Cl溶液中由水电离的c(H+)之比为1:104 |
| D.向pH=3的醋酸溶液中加入等体积pH=3的盐酸溶液,醋酸的电离平衡不移动 |
您最近半年使用:0次



