某温度下,等体积、相同 的盐酸和醋酸溶液分别加水稀释,溶液中的
的盐酸和醋酸溶液分别加水稀释,溶液中的 随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
 的盐酸和醋酸溶液分别加水稀释,溶液中的
的盐酸和醋酸溶液分别加水稀释,溶液中的 随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
| A.Ⅱ表示的是盐酸的变化曲线 |
B.b点溶液中水电离的 小于c点溶液 小于c点溶液 |
C.取等体积的a点、b点对应的溶液,消耗的 的量相同 的量相同 |
| D.b点酸的总浓度大于a点酸的总浓度 |
更新时间:2024-04-24 09:13:19
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】25℃时,向20mL 0.10mol/L的一元弱酸HA(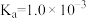 )中逐滴加入0.10mol/L NaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如下图所示,下列说法正确的是
)中逐滴加入0.10mol/L NaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如下图所示,下列说法正确的是
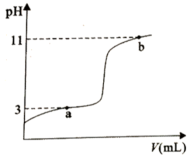
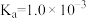 )中逐滴加入0.10mol/L NaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如下图所示,下列说法正确的是
)中逐滴加入0.10mol/L NaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如下图所示,下列说法正确的是
| A.溶液在a点和b点时水的电离程度相同 |
B. mL时, mL时,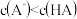 |
C.a点时,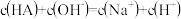 |
D.b点时,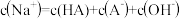 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】能促进水的电离,且水溶液呈碱性的是
| A.NaOH | B. | C. | D. |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 为阿伏加德罗常数的值。下列说法一定正确的是
为阿伏加德罗常数的值。下列说法一定正确的是
 为阿伏加德罗常数的值。下列说法一定正确的是
为阿伏加德罗常数的值。下列说法一定正确的是A.1LpH=1的H3PO4溶液中H+的数目为 |
B.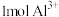 完全水解生成氢氧化铝胶体粒子的数目为 完全水解生成氢氧化铝胶体粒子的数目为 |
C. 的 的 溶液中 溶液中 的数目小于 的数目小于 |
D.25℃, 的 的 溶液中由水电离出的 溶液中由水电离出的 的数目为 的数目为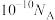 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,用一定浓度的盐酸溶液滴定某氨水溶液。滴定终点附近溶液pH和导电能力的变化分别如下图所示(利用溶液导电能力的变化可判断滴定终点,溶液总体积变化忽略不计)。下列说法错误的是
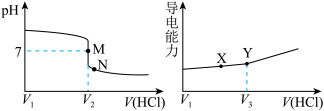

| A.M点对应溶液中c(NH4+)=c(Cl-) |
| B.X→Y溶液导电性增强的主要原因是c(H+)和c(Cl-)增大 |
| C.根据溶液pH和导电能力的变化可判断V2<V3 |
D.M→N过程中 不变 不变 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】相同温度下,关于浓度相同的HCl和CH3COOH两种溶液的比较,下列说法正确的是
| A.CH3COOH部分电离,n(CH3COOˉ)<n(Clˉ) |
| B.加入足量Mg,生成的氢气体积前者小于后者 |
| C.等体积的两种溶液分别与同浓度的NH3·H2O反应后呈中性,消耗的氨水体积相等 |
| D.分别与NaOH固体反应后呈中性的溶液中(忽略溶液体积变化):c(CH3COOˉ)<c(Clˉ) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,有关醋酸溶液的叙述中正确的是
A.用pH计测得 的 的 溶液的pH约2.9,说明 溶液的pH约2.9,说明 是弱酸 是弱酸 |
B.将 的醋酸稀释为 的醋酸稀释为 的过程中, 的过程中,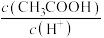 比值不变 比值不变 |
C.向 的 的 溶液中加入少量 溶液中加入少量 固体, 固体, 的电离程度增大 的电离程度增大 |
D. 的醋酸和盐酸分别与 的醋酸和盐酸分别与 的NaOH溶液完全中和,两者消耗NaOH溶液的体积相同 的NaOH溶液完全中和,两者消耗NaOH溶液的体积相同 |
您最近半年使用:0次

 溶液一定呈酸性的是
溶液一定呈酸性的是 是弱酸
是弱酸

 的电离常数大于
的电离常数大于