1 . 室温下,二元酸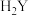 溶液中逐滴滴加NaOH溶液,混合溶液中粒子浓度与pH的关系如图所示。下列说法正确的是
溶液中逐滴滴加NaOH溶液,混合溶液中粒子浓度与pH的关系如图所示。下列说法正确的是
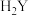 溶液中逐滴滴加NaOH溶液,混合溶液中粒子浓度与pH的关系如图所示。下列说法正确的是
溶液中逐滴滴加NaOH溶液,混合溶液中粒子浓度与pH的关系如图所示。下列说法正确的是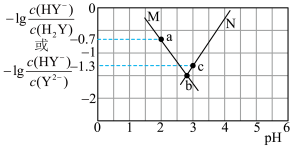
A.曲线M表示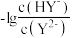 与pH的变化关系 与pH的变化关系 |
| B.a→c过程中,水的电离程度先增大后减小 |
C.b点溶液中: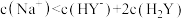 |
D.NaHY溶液中: |
您最近半年使用:0次
2 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.常温下,纯水中含有的离子数目约为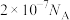 |
B.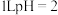 的稀硫酸中含有的 的稀硫酸中含有的 数目为 数目为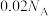 |
C.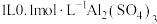 溶液中含有的阳离子数小于 溶液中含有的阳离子数小于 |
D. 硫化钠溶液中含有的 硫化钠溶液中含有的 的数目小于 的数目小于 |
您最近半年使用:0次
3 . 现有常温下的甲、乙两种溶液:甲为 溶液,乙为
溶液,乙为 溶液。下列说法错误的是
溶液。下列说法错误的是
 溶液,乙为
溶液,乙为 溶液。下列说法错误的是
溶液。下列说法错误的是A. 的电离程度:甲=乙 的电离程度:甲=乙 |
| B.均加水稀释到100mL后,pH的变化量:甲=乙 |
| C.均升温到40℃后,甲、乙的pH都变大 |
| D.将甲、乙混合充分反应后,混合溶液呈中性 |
您最近半年使用:0次
4 . 研究含氮化合物对消除环境污染,能源结构的改变,食品添加剂的研究等有重要意义。
(1)甘氨酸锌常用于食品的添加剂,也可代替甘油作烟丝的加香、防冻。一水合甘氨酸锌结构简式如图所示。___________ 。
②基态锌原子的核外电子排布式为___________ ,核外有___________ 种能量不同的电子,最高能层的符号为___________ 。
(2)“中国制造2025”是中国政府实施制造强国战略第一个十年行动领。氮化铬在现代工业中发挥了重要作用。
①基态N原子的价层电子的轨道表示式为___________ 。
②基态Cr原子的价层电子排布式为___________ 。
(3)NO在空气中存在如下反应:2NO(g)+O2(g) 2NO2(g),该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为:
2NO2(g),该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为:___________ 。 ②氨水③
②氨水③ ④
④ 。
。 由大到小顺序是
由大到小顺序是___________ (用序号表示)。
(5)若T℃时,pH=2的醋酸溶液中由水电离出的c(H+)=1×10-11,则该温度下水的离子积常数Kw=___________ 。
室温下VaLpH=1的HCl溶液与VbLpH=12的NaOH溶液混合后pH=3,则Va:Vb=___________ 。
(1)甘氨酸锌常用于食品的添加剂,也可代替甘油作烟丝的加香、防冻。一水合甘氨酸锌结构简式如图所示。

②基态锌原子的核外电子排布式为
(2)“中国制造2025”是中国政府实施制造强国战略第一个十年行动领。氮化铬在现代工业中发挥了重要作用。
①基态N原子的价层电子的轨道表示式为
②基态Cr原子的价层电子排布式为
(3)NO在空气中存在如下反应:2NO(g)+O2(g)
 2NO2(g),该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为:
2NO2(g),该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为: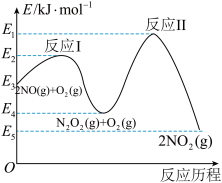
 ②氨水③
②氨水③ ④
④ 。
。 由大到小顺序是
由大到小顺序是(5)若T℃时,pH=2的醋酸溶液中由水电离出的c(H+)=1×10-11,则该温度下水的离子积常数Kw=
室温下VaLpH=1的HCl溶液与VbLpH=12的NaOH溶液混合后pH=3,则Va:Vb=
您最近半年使用:0次
5 . 常温下,用0.2mol/L盐酸滴定25.00mL0.2mol/L某弱碱ROH溶液,所得溶液pH、R+和ROH的物质的量分数与滴加盐酸体积的关系如图所示。下列叙述正确的是
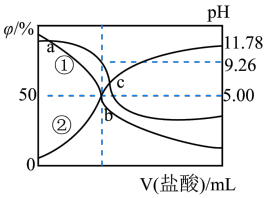

| A.曲线②代表ROH |
| B.若c点加入HCl溶液体积为25mL,则溶液中存在c(H+)>c(OH-)+c(ROH) |
| C.RCl的水解平衡常数为1.0×10-5 |
| D.a、b、c三点的溶液,水的电离程度:a<b<c |
您最近半年使用:0次
解题方法
6 . 常温下,下列各组离子在相应条件下可能大量共存的是
A.水电离出来的c(H+)<10-7mol/L的溶液中:Cl-、K+、 、S2- 、S2- |
B.遇甲基橙变红色的溶液中: 、Na+、Cl-、 、Na+、Cl-、 |
C.含Al3+的溶液中:K+、Na+、Cl-、 |
D.透明中性溶液中:Fe3+、 、 、 、Cl- 、Cl- |
您最近半年使用:0次
解题方法
7 . 根据下列图示所得出的结论不正确的是
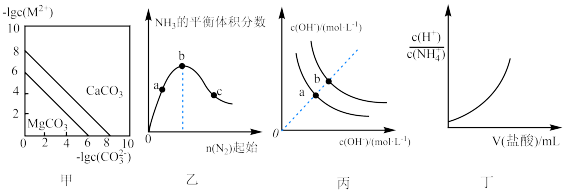
A.图甲表示一定温度下,MCO3(M:Mg2+、Ca2+)的沉淀溶解平衡曲线,则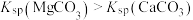 |
B.图乙是H2的起始量一定时恒温密闭容器中发生:N2(g)+3H2(g) 2NH3(g)反应,达到平衡时NH3的体积分数随N2的起始物质的量的变化曲线,则H2的转化率:b>c>a 2NH3(g)反应,达到平衡时NH3的体积分数随N2的起始物质的量的变化曲线,则H2的转化率:b>c>a |
| C.图丙表示不同温度下溶液中H+和OH-的浓度变化曲线,图中a点对应温度低于b点 |
D.图丁投示向0.lmol/L的NH4Cl溶液中滴加0.1mol/L的盐酸,溶液中 随盐酸的体积变化关系 随盐酸的体积变化关系 |
您最近半年使用:0次
8 . 下列溶液中的微粒浓度关系正确的是
A.Na2CO3溶液中离子浓度大小关系为 |
B.0.1mol/L NaHCO3溶液中  |
C.80℃时,0.1mol/L NaHSO4溶液中由水电离出的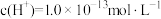 |
| D.常温下,pH=4的CH3COOH溶液与pH=10的NaOH溶液等体积混合后,溶液的pH=7 |
您最近半年使用:0次
名校
解题方法
9 . 常温下将NaOH溶液滴加到 溶液中,混合溶液的pH与离子浓度变化的关系如图所示[纵坐标为
溶液中,混合溶液的pH与离子浓度变化的关系如图所示[纵坐标为 或
或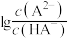 ]。下列叙述正确的是
]。下列叙述正确的是
 溶液中,混合溶液的pH与离子浓度变化的关系如图所示[纵坐标为
溶液中,混合溶液的pH与离子浓度变化的关系如图所示[纵坐标为 或
或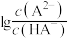 ]。下列叙述正确的是
]。下列叙述正确的是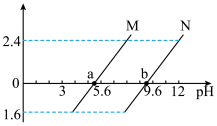
A.曲线N表示pH与 的关系 的关系 |
B.图中a点对应溶液中: |
C.NaHA溶液中: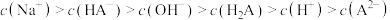 |
| D.溶液pH从5.6到9.6的过程中,水的电离程度先增大后减小 |
您最近半年使用:0次
昨日更新
|
460次组卷
|
6卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题江西省部分地区2023-2024学年高三下学期3月月考化学试题甘肃省酒泉市九师联盟2023-2024学年高三下学期3月月考化学试题(已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)河南省九师联盟2023-2024学年高三下学期3月质量检测理科综合化学试题湖北省九师联盟2024届高三下学期3月质量检测(W-G)化学试卷
名校
解题方法
10 . 25℃时,用0.1
 溶液滴定同浓度的
溶液滴定同浓度的 溶液,
溶液, 被滴定分数
被滴定分数 与
与 值、微粒分布分数
值、微粒分布分数 ,X表示
,X表示 、
、 或
或 ]的关系如图所示,下列说法正确的是
]的关系如图所示,下列说法正确的是

 溶液滴定同浓度的
溶液滴定同浓度的 溶液,
溶液, 被滴定分数
被滴定分数 与
与 值、微粒分布分数
值、微粒分布分数 ,X表示
,X表示 、
、 或
或 ]的关系如图所示,下列说法正确的是
]的关系如图所示,下列说法正确的是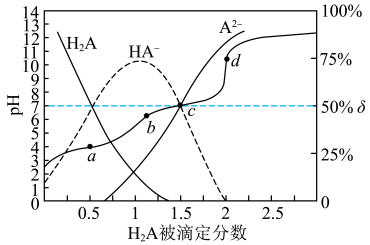
A.用 溶液滴定0.1 溶液滴定0.1 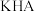 溶液可以用酚酞作指示剂 溶液可以用酚酞作指示剂 |
B.25℃时, 第二步电离平衡常数 第二步电离平衡常数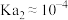 |
C.c点溶液中: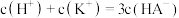 |
D.a、b、c、d四点溶液中水的电离程度: |
您最近半年使用:0次
昨日更新
|
267次组卷
|
3卷引用:云南省大理白族自治州2024届高三第二次复习统一检测理综-化学试卷



